Læringsmål
I slutningen af dette afsnit vil du kunne:
- Oplyse de almindelige stoffaser.
- Forklare de fysiske egenskaber ved faste stoffer, væsker og gasser.
- Beskriv atomernes placering i faste stoffer, væsker og gasser.

Figur 1. (a) Atomer i et fast stof har altid de samme naboer, der holdes tæt på hinanden af kræfter, som her er repræsenteret ved fjedre. Disse atomer er i det væsentlige i kontakt med hinanden. En sten er et eksempel på et fast stof. Denne sten bevarer sin form på grund af de kræfter, der holder dens atomer sammen. (b) Atomer i en væske er også i tæt kontakt, men kan glide over hinanden. Kræfterne mellem dem modstår kraftigt forsøg på at skubbe dem tættere sammen og holder dem også i tæt kontakt. Vand er et eksempel på en væske. Vand kan flyde, men det forbliver også i en åben beholder på grund af kræfterne mellem dets atomer. (c) Atomer i en gas er adskilt af afstande, der er betydeligt større end størrelsen af atomerne selv, og de bevæger sig frit rundt. En gas skal holdes i en lukket beholder for at forhindre den i at bevæge sig frit ud.
Atomer i faste stoffer er i tæt kontakt med hinanden, og der er kræfter mellem dem, som gør det muligt for atomerne at vibrere, men ikke at ændre position med naboatomer. (Disse kræfter kan opfattes som fjedre, der kan strækkes eller komprimeres, men som ikke let kan brydes). Et fast stof er således modstandsdygtigt over for alle former for spændinger. Et fast stof kan ikke let deformeres, fordi de atomer, der udgør det faste stof, ikke kan bevæge sig frit. Faste stoffer er også modstandsdygtige over for kompression, fordi deres atomer indgår i en gitterstruktur, hvor atomerne har en forholdsvis fast afstand til hinanden. Ved kompression ville atomerne blive presset ind i hinanden. De fleste af de eksempler, vi har studeret indtil nu, har handlet om faste genstande, som deformeres meget lidt, når de belastes.
Sammenhænge: Submikroskopisk forklaring af faste stoffer og væsker
Væsker deformeres derimod let ved belastning og springer ikke tilbage til deres oprindelige form, når kraften fjernes, fordi atomerne frit kan glide rundt og skifte naboer – dvs. de flyder (så de er en type væske), hvor molekylerne holdes sammen af deres indbyrdes tiltrækning. Når en væske anbringes i en beholder uden låg på, forbliver den i beholderen (forudsat at beholderen ikke har huller under væskens overflade!). Fordi atomerne er tæt pakket, modstår væsker, ligesom faste stoffer, kompression.
Atomer i gasser er adskilt af afstande, der er store i forhold til atomernes størrelse. Kræfterne mellem gasatomer er derfor meget svage, undtagen når atomerne kolliderer med hinanden. Gasser flyder derfor ikke blot (og betragtes derfor som væsker), men de er også relativt lette at komprimere, fordi der er meget plads og kun få kræfter mellem atomerne. Når gasser anbringes i en åben beholder, vil de, i modsætning til væsker, slippe ud. Den vigtigste forskel er, at gasser er lette at komprimere, mens væsker ikke er det. Vi vil generelt betegne både gasser og væsker blot som væsker og kun skelne mellem dem, når de opfører sig forskelligt.
PhET Explorations: Materiens stoftilstande – Grundlæggende
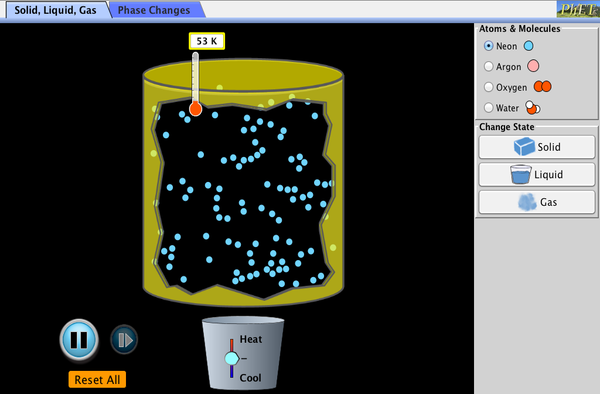
Klik for at downloade simuleringen. Kør ved hjælp af Java.
Sammenfatning af afsnittet
- En væske er en stoftilstand, der giver efter for sidelæns eller forskydningskræfter. Væsker og gasser er begge væsker. Fluidstatik er fysik for stationære fluider.
Begrebsspørgsmål
1. Hvilken fysisk egenskab adskiller en væske fra et fast stof?
2. Hvilke af følgende stoffer er væsker ved stuetemperatur: luft, kviksølv, vand, glas?
3. Hvorfor er gasser lettere at komprimere end væsker og faste stoffer?
4. Hvordan adskiller gasser sig fra væsker?
Glossar
væsker: væsker og gasser; en væske er en stoftilstand, der giver efter for forskydningskræfter