Die Begriffe Lumineszenz, Photolumineszenz, Fluoreszenz und Phosphoreszenz werden in Forschungsarbeiten routinemäßig verwendet, um die Emission von Licht aus einer Probe zu beschreiben. Diese mehrfache Benennung kann verwirrend sein, da einige der Begriffe austauschbar verwendet werden und Forscher mit unterschiedlichem wissenschaftlichem Hintergrund lieber eine Bezeichnung als eine andere verwenden. In diesem Artikel beantworten wir die Frage „Was ist der Unterschied zwischen Lumineszenz, Photolumineszenz, Fluoreszenz und Phosphoreszenz“.
Was ist Lumineszenz?
Lumineszenz ist jede Emission von Licht (elektromagnetische Wellen) aus einer Substanz, die nicht durch Erhitzung entsteht. Diese Definition unterscheidet die Lumineszenz von der Glut, die eine Lichtemission ist, die durch die erhöhte Temperatur einer Substanz entsteht, wie z. B. eine glühende Glut. Das Wort Lumineszenz leitet sich von dem lateinischen Wort für Licht, lumen, und dem lateinischen Wort escentia ab, das „der Vorgang“ bedeutet, und bezeichnet somit den Vorgang der Lichtabgabe.

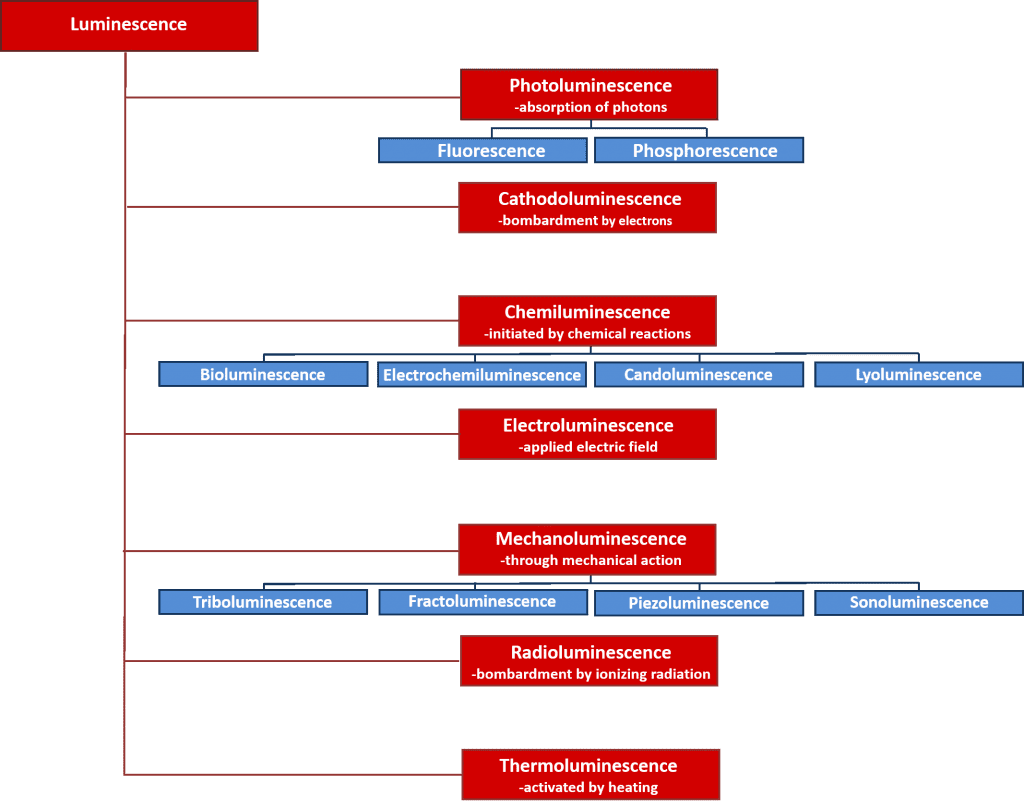
Es gibt viele Arten von Lumineszenz, die nach der Energiequelle klassifiziert werden können, die den Lumineszenzprozess auslöst. Eine Übersicht über die verschiedenen Arten von Lumineszenz und ihre Energiequellen ist in Abbildung 2 dargestellt. Viele dieser Lumineszenzprozesse haben wichtige wissenschaftliche und industrielle Anwendungen, wie z. B. die Elektrolumineszenz, bei der Licht durch die Rekombination von Elektronen und Löchern nach Anlegen eines elektrischen Feldes an ein Material emittiert wird und die das Funktionsprinzip von Leuchtdioden darstellt, und die Chemilumineszenz, bei der die Lichtemission durch eine chemische Reaktion ausgelöst wird und die in biologischen Tests verwendet wird und für das Leuchten von Leuchtstäben verantwortlich ist. Der Schwerpunkt dieses Artikels liegt jedoch auf der Photolumineszenz, die die Grundlage für die leistungsstarke, zerstörungsfreie spektroskopische Technik, die Photolumineszenzspektroskopie, bildet, die sowohl in der Wissenschaft als auch in der Industrie in großem Umfang eingesetzt wird.
Was ist Photolumineszenz?
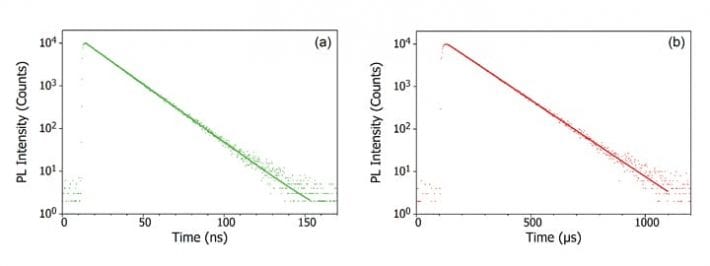
Photolumineszenz ist die Emission von Licht aus einem Material nach Absorption von Licht. Das Wort an sich ist interessant, da es sich aus dem lateinischen Wort luminescence und der griechischen Vorsilbe photo- für Licht zusammensetzt. Jede Lumineszenz, die durch die Absorption von Photonen hervorgerufen wird, nennt man Photolumineszenz. Dies könnte auch die Lichtemission eines organischen Farbstoffmoleküls in Lösung sein (Abbildung 3a) oder die Band-zu-Band-Rekombination von Elektronen und Löchern nach Photoanregung eines Halbleiters (Abbildung 3b).

Jede durch Photonenabsorption induzierte Lichtemission als Photolumineszenz zu bezeichnen, ist zutreffend; es ist jedoch gängige Praxis, insbesondere bei Chemikern, die Photolumineszenz weiter in Fluoreszenz und Phosphoreszenz zu unterteilen.
Was ist der Unterschied zwischen Fluoreszenz und Phosphoreszenz?
Es gibt verschiedene Definitionen von Fluoreszenz und Phosphoreszenz, wobei die einfachste besagt, dass Fluoreszenz eine sofortige Photolumineszenz ist, die sehr kurz nach der Photoanregung einer Substanz auftritt, während Phosphoreszenz eine langlebige Photolumineszenz ist, die lange nach dem Ende der Photoanregung anhält. Dies ist zwar eine einfache Definition, sie erklärt jedoch nicht, warum ein solcher Unterschied in den Zeitskalen der Photolumineszenz auftritt und einige Materialien in eine Grauzone zwischen den klassischen Fluoreszenz- und Phosphoreszenz-Zeitskalen fallen können. Eine genauere Definition muss auf der Quantenmechanik der am Emissionsprozess beteiligten angeregten und Grundzustände beruhen. Mit diesem Ansatz können Fluoreszenz und Phosphoreszenz als Photolumineszenz definiert werden, bei der der Strahlungsübergang keine Änderung der Spin-Multiplizität erfordert, bzw. als Photolumineszenz, bei der der Strahlungsübergang eine Änderung der Spin-Multiplizität erfordert.
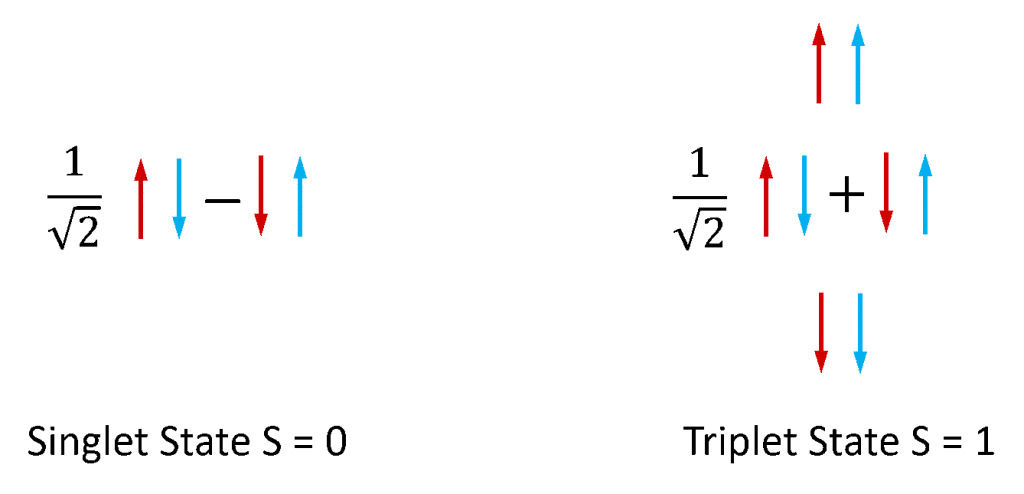
Fluoreszenz und Phosphoreszenz werden am häufigsten für die Photolumineszenz von molekularen Systemen verwendet. Elektronen in stabilen Molekülen liegen immer paarweise vor, da Moleküle mit ungepaarten Elektronen extrem reaktiv und instabil sind. Elektronen besitzen einen Eigendrehimpuls, der als „Spin“ bezeichnet wird, und ein Elektronenpaar kann sich in einem von zwei Gesamtspinzuständen befinden, je nach der relativen Symmetrie der Spins der beiden Elektronen. Wenn sich die beiden Spins in einer antisymmetrischen Konfiguration befinden, hat das Elektronenpaar einen Gesamtspin von Null (S = 0), während das Paar bei einer symmetrischen Konfiguration einen Gesamtspin von Eins (S = 1) hat. Wie in Abbildung 4 dargestellt, gibt es eine antisymmetrische Kombination von Elektronenspinpaarzuständen und drei symmetrische Kombinationen von Spinpaarzuständen; die Zustände S = 0 und S = 1 werden daher als Singulett bzw. Triplett bezeichnet.
Wenn ein Photon vom Molekül absorbiert wird, wird eines der Elektronen auf ein höheres Energieniveau gebracht, und das Molekül befindet sich nun in einem angeregten Zustand. Der Grundzustand eines Moleküls ist (fast) immer ein Singulett-Zustand (S0), und aufgrund der Drehimpulserhaltung muss der photoangeregte Zustand ebenfalls ein Singulett (S1) sein, wie im Jablonski-Diagramm unten dargestellt. Der Zerfall des S1-Zustands zurück in den S0-Zustand ist ein zulässiger Übergang (da beide Zustände die gleiche Spin-Multiplizität haben), der zu einer prompten Photolumineszenz führt, die auf der Zeitskala von Pikosekunden bis Nanosekunden auftritt und Fluoreszenz genannt wird.
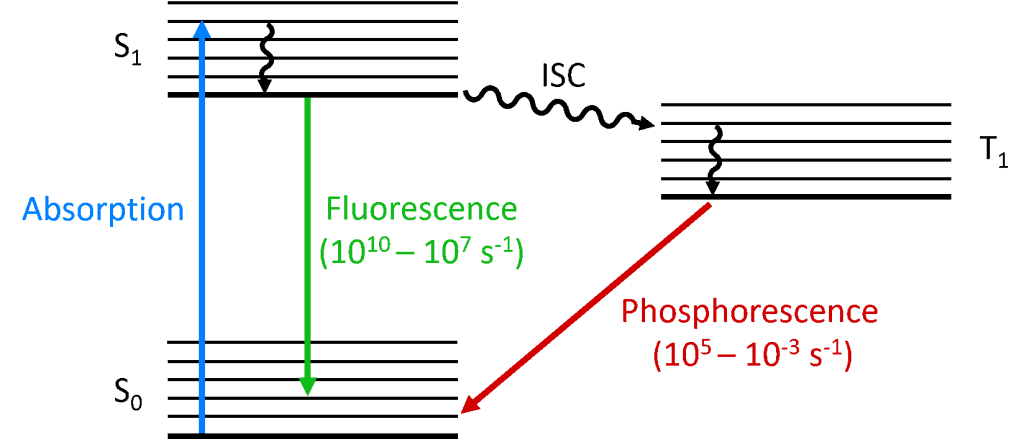
Alternativ kann das Molekül einen Intersystem-Crossing (ISC) in den angeregten Triplett-Zustand (T1) erfahren. ISC tritt typischerweise in Molekülen mit einem hohen Grad an Spin-Bahn-Kopplung auf, d. h. der Kopplung des Orbitaldrehimpulses und des Spindrehimpulses des Elektrons, die eine Umwandlung zwischen Singulett- und Triplett-Zustand ermöglicht. Die Stärke der Spin-Bahn-Kopplung nimmt mit der Masse des Atoms zu, so dass phosphoreszierende Moleküle Schwermetalle wie Europium und Iridium enthalten müssen. Der Zerfall des T1-Zustands zurück in den S0-Zustand ist ein verbotener Übergang, da die Zustände aufgrund der Drehimpulserhaltung unterschiedliche Spinmultiplikationen aufweisen. Durch die Spin-Bahn-Kopplung wird diese Einschränkung jedoch gelockert und ein Strahlungsübergang vom T1-Zustand zum S1-Zustand wird möglich. Da dieser „verboten“ ist, tritt die Photolumineszenz, die aus dem Übergang von T1 zu S0 resultiert, auf einer viel langsameren Zeitskala von Mikrosekunden bis zu Tausenden von Sekunden auf und wird als Phosphoreszenz bezeichnet.
Es sollte auch beachtet werden, dass die Emission von einigen Materialien nicht immer eindeutig in die eine oder andere Kategorie fällt. Ein Beispiel hierfür ist die thermisch aktivierte verzögerte Fluoreszenz (TADF). Bei der TADF liegen das S1- und das T1-Niveau energetisch nahe beieinander und sind stark gekoppelt, so dass eine umgekehrte ISC vom T1- zum S1-Niveau möglich ist. Dies führt zu einem verzögerten S1-zu-S0-Übergang, der zu einer Photolumineszenz auf einer Zeitskala zwischen Fluoreszenz und Phosphoreszenz führt, die als verzögerte Fluoreszenz bezeichnet wird. Weitere Informationen über TADF und seine Verwendung in hocheffizienten OLEDs finden Sie im Beitrag „Was ist TADF?“.
Wann man die Emission als Photolumineszenz oder als Fluoreszenz/Phosphoreszenz bezeichnet, ist letztlich eine Frage der persönlichen Vorliebe. Chemiker und Biologen, die in erster Linie molekulare Systeme untersuchen, bevorzugen die Verwendung von Fluoreszenz und Phosphoreszenz, da es in diesen stark lokalisierten molekularen Systemen unterschiedliche Singulett- und Triplett-Zustände gibt. Im Gegensatz dazu untersuchen Physiker vorwiegend Halbleitermaterialien, in denen die Elektronen stark delokalisiert sind und das Konzept von Singulett und Triplett häufig nicht mehr relevant ist. Dies ist einer der Gründe, warum Physiker dazu neigen, den umfassenderen Begriff Photolumineszenz zu verwenden, um die Lichtemission zu beschreiben.
Wie auch immer man es nennen mag: Photolumineszenz, Fluoreszenz und Phosphoreszenz können eine Fülle von Informationen über die Eigenschaften von Molekülen und Materialien liefern; sie reichen von der Bestimmung der Ladungsträgerlebensdauer in Solarzellen bis zur Messung der Solvatationsdynamik um Mizellen in lebenden Zellen.
Produkte für Lumineszenz, Photolumineszenz, Fluoreszenz und Phosphoreszenz
Für die Messung der Photolumineszenz ist ein Photolumineszenzspektrometer erforderlich. Edinburgh Instruments bietet eine Reihe von Photolumineszenzspektrometern mit Einzelphotonenzählung an, mit denen Photolumineszenzspektren, Lebensdauern, Anisotropie und Quantenausbeuten Ihrer Proben gemessen werden können.
Keep in Touch
Wenn Ihnen die Lektüre dieses Artikels gefallen hat und Sie als Erster über die neuesten Nachrichten, Anwendungen und Produktinformationen von Edinburgh Instruments informiert werden möchten, dann melden Sie sich über den roten Anmeldebutton unten für unseren unregelmäßigen Newsletter an und folgen Sie uns in den sozialen Medien.