La anemia hemolítica autoinmune (AIHA) está mediada por anticuerpos, y en la mayoría de los casos la inmunoglobulina (Ig) G es el anticuerpo mediador. Este tipo de AIHA se denomina AIHA «caliente» porque los anticuerpos IgG se unen mejor a la temperatura corporal. La AIHA «fría» está mediada por anticuerpos IgM, que se unen al máximo a temperaturas inferiores a 37°C. La AHA causada por una reacción a un fármaco es rara, con una incidencia anual estimada de 1:1.000.000 para la AHA grave relacionada con fármacos.1 Este artículo revisa el tratamiento de los tipos más comunes de AHA, centrándose en la AHA caliente, fría e inducida por fármacos; la evaluación y el diagnóstico de la AHA se revisan en un artículo separado.
Anemia hemolítica autoinmune caliente
En la AHA, la hemólisis está mediada por anticuerpos que se unen a la superficie de los glóbulos rojos. La AIHA en la que los anticuerpos IgG son los anticuerpos agresores se denomina AIHA caliente. El término «caliente» hace referencia al hecho de que el anticuerpo se une mejor a la temperatura corporal (37 °C). En la AIHA caliente, las pruebas mostrarán moléculas IgG adheridas a la superficie de los glóbulos rojos, y el 50% de los pacientes también mostrarán C3. Entre el 50% y el 90% de los casos de AIHA se deben a los anticuerpos calientes.2,3 La incidencia de la AIHA caliente varía según las series, pero es de aproximadamente 1 caso por cada 100.000 pacientes al año; esta forma de hemólisis afecta con más frecuencia a las mujeres que a los hombres.4,5
Opciones terapéuticas
Primera línea
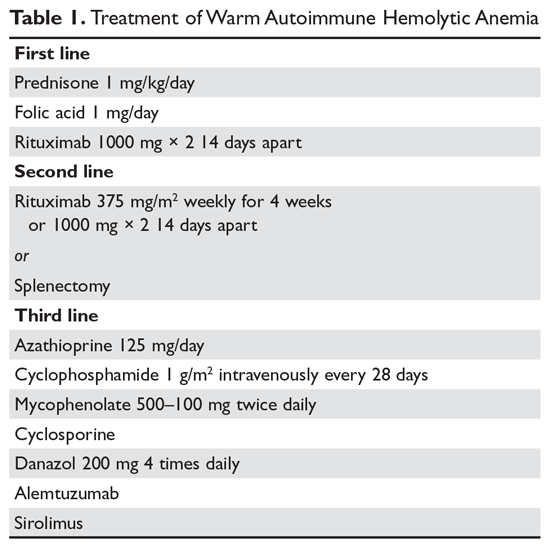
Esteroides. El objetivo de la terapia en la AIHA caliente puede ser difícil de definir. Sin embargo, la mayoría estaría de acuerdo en que un hematocrito superior al 30% (o superior para prevenir los síntomas) con un aumento mínimo del recuento de reticulocitos -que refleja un proceso hemolítico significativamente ralentizado- es un objetivo razonable. El tratamiento inicial de la AIHA caliente es la prednisona a una dosis estándar de 1 mg/kg diario (Tabla 1).6,7 Los pacientes también deben empezar a recibir inhibidores de la bomba de protones para prevenir las úlceras. Los pacientes pueden tardar hasta 3 semanas en responder al tratamiento con prednisona. Una vez que el hematocrito del paciente supera el 30%, la prednisona se reduce lentamente. Aunque aproximadamente el 80% de los pacientes responden a los esteroides, sólo el 30% puede dejar de tomarlos por completo. Para los pacientes que pueden mantenerse con una dosis diaria de esteroides de 10 mg o menos, los esteroides pueden ser el tratamiento más razonable a largo plazo. Además, dado que la hemólisis activa provoca un aumento de la demanda de ácido fólico, a los pacientes con AIHA caliente se les suele recetar ácido fólico 1 mg diario para prevenir la anemia megaloblástica debida a la deficiencia de ácido fólico.
Rituximab. Cada vez más, el tratamiento con rituximab (anti-CD20) se añade a los esteroides iniciales. Dos ensayos clínicos mostraron un aumento de las respuestas a largo y corto plazo con el uso de rituximab.8,9 Una consideración importante es que la mayoría de los pacientes responden gradualmente al rituximab durante semanas, por lo que no debe esperarse una respuesta rápida. La mayoría de los estudios han utilizado la dosis tradicional de 375 mg/m2 semanalmente durante 4 semanas. Estas respuestas parecen ser duraderas, pero al igual que en la trombocitopenia inmunitaria (PTI), la repetición del tratamiento con rituximab es eficaz.
Los principales efectos secundarios del rituximab son las reacciones a la infusión, que suelen empeorar con la primera dosis. Estas reacciones pueden controlarse con antihistamínicos, esteroides y, para los rigores graves, meperidina. En raras ocasiones, los pacientes pueden desarrollar neutropenia (aproximadamente 1:500) que parece ser de naturaleza autoinmune. Las infecciones parecen aumentar mínimamente con el uso de rituximab.10 Un grupo de riesgo es el de los portadores crónicos del virus de la hepatitis B, que pueden experimentar una reactivación del virus que puede ser mortal. Por lo tanto, los pacientes a los que se les está considerando administrar rituximab deben ser examinados para determinar si son portadores del virus de la hepatitis B.11 Los pacientes que reciben rituximab corren un riesgo muy leve de padecer leucoencefalopatía multifocal progresiva, que es más común en pacientes con cáncer y en pacientes muy inmunodeprimidos. El riesgo global se desconoce, pero es inferior a 1:50.000.