Los términos luminiscencia, fotoluminiscencia, fluorescencia y fosforescencia se utilizan habitualmente en los trabajos de investigación para describir la emisión de luz de una muestra. Esta multiplicidad de denominaciones puede resultar confusa, ya que varios de los términos se utilizan indistintamente y los investigadores de distintos ámbitos científicos prefieren utilizar una denominación en lugar de otra. En este artículo respondemos a la pregunta «¿Cuál es la diferencia entre luminiscencia, fotoluminiscencia, fluorescencia y fosforescencia?».
¿Qué es la luminiscencia?
La luminiscencia es cualquier emisión de luz (ondas electromagnéticas) de una sustancia que no se produce por calentamiento. Esta definición distingue la luminiscencia de la incandescencia, que es la emisión de luz debida a la elevada temperatura de una sustancia, como una brasa caliente. La palabra luminiscencia deriva de la palabra latina para luz, lumen, y del latín, escentia, que significa ‘el proceso de’ y, por tanto, es el proceso de emisión de luz.

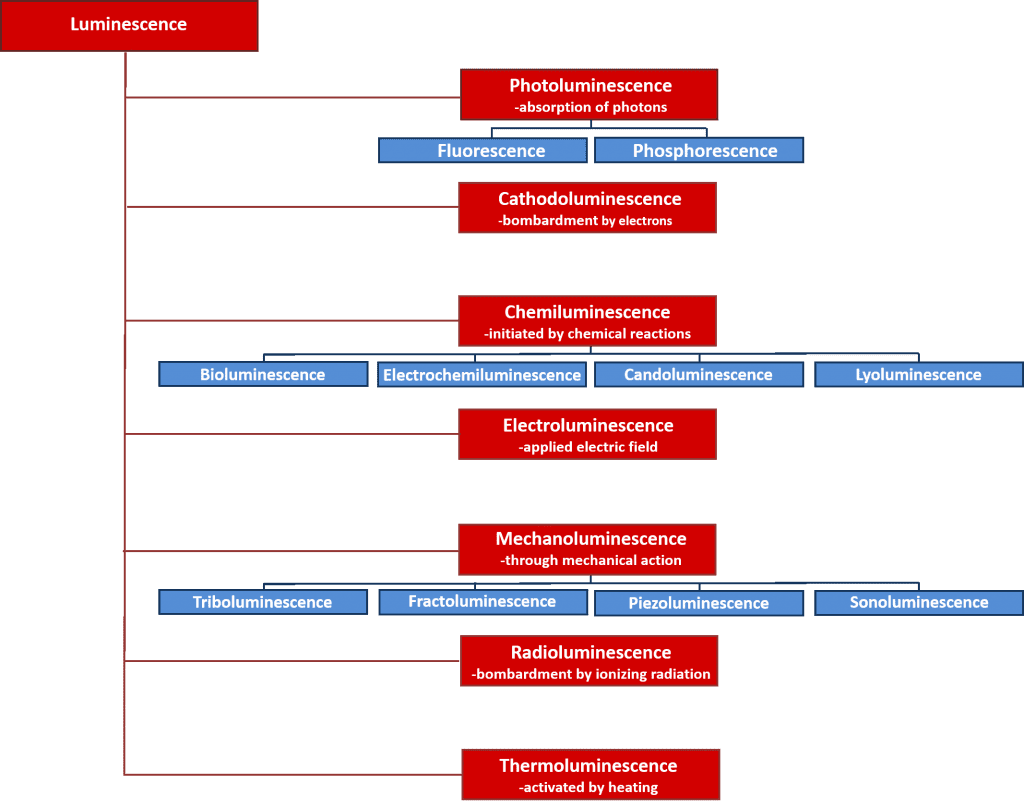
Hay muchos tipos de luminiscencia que pueden clasificarse según la fuente de energía que inicia el proceso de luminiscencia. En la figura 2 se ofrece un resumen de los distintos tipos de luminiscencia y sus fuentes de energía. Muchos de estos procesos de luminiscencia tienen importantes aplicaciones científicas e industriales, como la electroluminiscencia, en la que la luz se emite tras la recombinación de electrones y huecos después de aplicar un campo eléctrico a través de un material, y que es el principio de funcionamiento de los diodos emisores de luz; y la quimioluminiscencia, en la que la emisión de luz se inicia por una reacción química y se utiliza en ensayos biológicos, y es responsable del brillo de las barras luminosas. Sin embargo, este artículo se centra en la fotoluminiscencia, que constituye la base de la potente técnica espectroscópica no destructiva, la espectroscopia de fotoluminiscencia, que se utiliza ampliamente tanto en el ámbito académico como en el industrial.
¿Qué es la fotoluminiscencia?
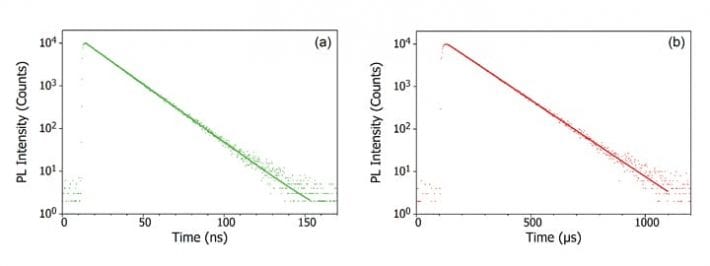
La fotoluminiscencia es la emisión de luz de un material tras la absorción de luz. La palabra en sí misma es interesante ya que es la combinación de la palabra derivada del latín luminiscencia y el prefijo griego, foto-, para luz. Cualquier luminiscencia inducida por la absorción de fotones se denomina fotoluminiscencia. Puede tratarse igualmente de la emisión de luz de una molécula de colorante orgánico en solución (Figura 3a), o de la recombinación banda a banda de electrones y huecos tras la fotoexcitación de un semiconductor (Figura 3b).

Describir cualquier emisión de luz inducida por la absorción de fotones como fotoluminiscencia es correcto; sin embargo, es una práctica común, sobre todo entre los químicos, subdividir la fotoluminiscencia en fluorescencia y fosforescencia.
¿Cuál es la diferencia entre fluorescencia y fosforescencia?
Hay varias definiciones de fluorescencia y fosforescencia, siendo la más sencilla que la fluorescencia es una fotoluminiscencia rápida que se produce muy poco después de la fotoexcitación de una sustancia, mientras que la fosforescencia es una fotoluminiscencia de larga duración que continúa mucho después de que la fotoexcitación haya cesado. Aunque se trata de una definición sencilla, no explica por qué se produce tal diferencia en las escalas de tiempo de la fotoluminiscencia y algunos materiales pueden caer en una zona gris entre las escalas de tiempo clásicas de la fluorescencia y la fosforescencia. Una definición más exhaustiva debe basarse en la mecánica cuántica de los estados excitados y molidos que intervienen en el proceso de emisión. Utilizando este enfoque, la fluorescencia y la fosforescencia pueden definirse como fotoluminiscencia cuando la transición radiativa no requiere un cambio en la multiplicidad de espín y fotoluminiscencia cuando la transición radiativa implica un cambio en la multiplicidad de espín, respectivamente.
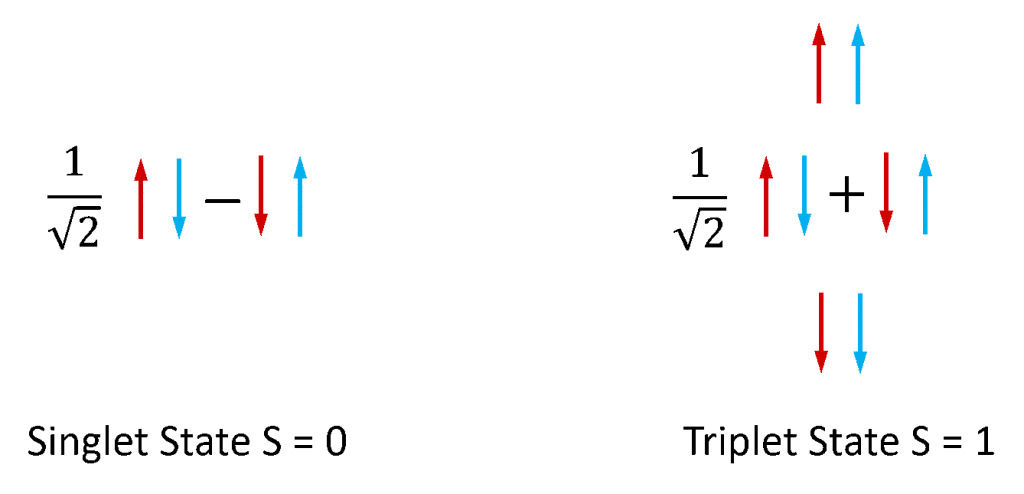
La fluorescencia y la fosforescencia se utilizan más comúnmente para referirse a la fotoluminiscencia de los sistemas moleculares. Los electrones en las moléculas estables siempre existen en pares, ya que las moléculas con electrones no apareados son extremadamente reactivas e inestables. Los electrones poseen un momento angular intrínseco conocido como «espín» y un par de electrones puede existir en uno de dos estados de espín total, dependiendo de la simetría relativa de los espines de los dos electrones. Si los dos espines están en una configuración antisimétrica, el par de electrones tiene un espín total de cero (S = 0), mientras que si están en una configuración simétrica, el par tiene un espín total de uno (S = 1). Como se ilustra en la figura 4, hay una combinación de estados de pares de espín de electrones que es antisimétrica y tres combinaciones de estados de pares de espín que son simétricos, por lo que los estados S = 0 y S = 1 se denominan singlete y triplete, respectivamente.
Cuando un fotón es absorbido por la molécula, uno de los electrones es promovido a un nivel de energía superior y la molécula se encuentra ahora en un estado excitado. El estado básico de una molécula es (casi) siempre un estado singlete (S0) y, debido a la conservación del momento angular, el estado fotoexcitado debe ser también un singlete (S1), como se muestra en el diagrama de Jablonski. El decaimiento del estado S1 de vuelta al S0 es una transición permitida (ya que ambos estados tienen la misma multiplicidad de espín) dando lugar a la fotoluminiscencia inmediata que se produce en la escala de tiempo de picosegundos a nanosegundos y se llama fluorescencia.
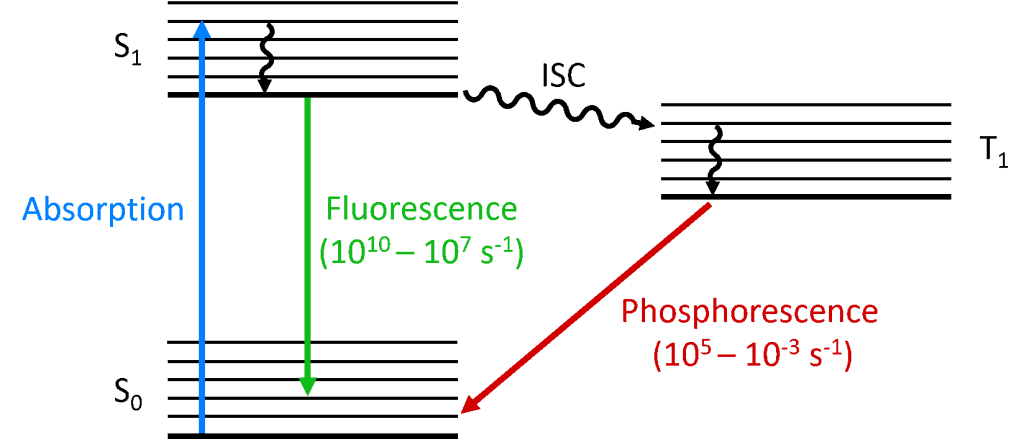
Alternativamente, la molécula puede sufrir un cruce intersistémico (ISC) al estado triplete excitado (T1). El ISC suele ocurrir en moléculas con un alto grado de acoplamiento espín-órbita, el acoplamiento del momento angular orbital y el momento angular de espín del electrón, que permite la conversión entre los estados singlete y triplete. La fuerza del acoplamiento espín-órbita aumenta con la masa del átomo, por lo que las moléculas fosforescentes deben contener metales pesados como el europio y el iridio. El decaimiento del estado T1 de vuelta al S0 es una transición prohibida ya que los estados tienen diferente multiplicidad de espín, debido a la conservación del momento angular. Sin embargo, el acoplamiento espín-órbita relaja esta restricción y es posible una transición radiativa del T1 al S1. Dado que está «prohibida», la fotoluminiscencia que resulta de la transición de T1 a S0 se produce en una escala de tiempo mucho más lenta, de microsegundos a miles de segundos, y se denomina fosforescencia.
También hay que tener en cuenta que la emisión de algunos materiales no siempre cae claramente en una categoría o en otra. Un ejemplo de esto es la fluorescencia retardada activada térmicamente (TADF). En la TADF los niveles S1 y T1 están próximos en energía y fuertemente acoplados, por lo que es posible una ISC inversa desde el T1 al S1. Esto da lugar a una transición retardada de S1 a S0 que da lugar a la fotoluminiscencia en una escala de tiempo entre la fluorescencia y la fosforescencia, conocida como fluorescencia retardada. Para obtener más información sobre la TADF y su uso en los OLED de alta eficiencia, lea el post sobre «¿Qué es la TADF?».
Cuándo describir la emisión como fotoluminiscencia frente a la fluorescencia/fosforescencia depende en última instancia de las preferencias personales. Los químicos y los biólogos, que estudian principalmente sistemas moleculares, prefieren utilizar la fluorescencia y la fosforescencia, ya que en estos sistemas moleculares altamente localizados existen estados singlete y triplete distintos. Por el contrario, los físicos estudian principalmente materiales semiconductores en los que los electrones están muy deslocalizados y el concepto de singlete y triplete suele dejar de ser relevante. Esta es una de las razones por las que los físicos tienden a utilizar el término más amplio de fotoluminiscencia para describir la emisión de luz.
Decida lo que decida llamar, la fotoluminiscencia, la fluorescencia y la fosforescencia pueden proporcionar una gran cantidad de información sobre las propiedades de las moléculas y los materiales, que van desde la determinación del tiempo de vida de los portadores de carga en las células solares hasta la medición de la dinámica de solvatación alrededor de las micelas en las células vivas.
Productos para luminiscencia, fotoluminiscencia, fluorescencia y fosforescencia
Para medir la fotoluminiscencia se necesita un espectrómetro de fotoluminiscencia y Edinburgh Instruments ofrece una gama de espectrómetros de fotoluminiscencia de recuento de fotones individuales para medir los espectros de fotoluminiscencia, los tiempos de vida, la anisotropía y los rendimientos cuánticos de sus muestras.
Manténgase en contacto
Si ha disfrutado de la lectura de este artículo y le gustaría ser el primero en ver las últimas noticias, aplicaciones e información de productos de Edinburgh Instruments, suscríbase a nuestro boletín infrecuente a través del botón rojo de suscripción que aparece a continuación, y síganos en las redes sociales.