En química, la geometría molecular en forma de T describe las estructuras de algunas moléculas en las que un átomo central tiene tres ligandos. Normalmente, los compuestos de tres coordenadas adoptan geometrías trigonales planas o piramidales. Ejemplos de moléculas en forma de T son los trifluoruros de halógeno, como el ClF3.
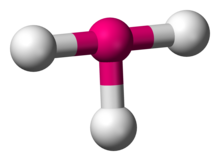
ClF3
C2v
90°, 180°
>0

De acuerdo con la teoría VSEPR, la geometría en forma de T resulta cuando tres ligandos y dos pares de electrones solitarios se unen al átomo central, escrito en notación AXE como AX3E2. La geometría en forma de T está relacionada con la geometría molecular bipiramidal trigonal para moléculas AX5 con tres ligandos ecuatoriales y dos axiales. En una molécula AX3E2, los dos pares solitarios ocupan dos posiciones ecuatoriales, y los tres átomos del ligando ocupan las dos posiciones axiales además de una posición ecuatorial. Los tres átomos se enlazan en ángulos de 90° a un lado del átomo central, produciendo la forma de T.
El anión trifluoroxenato(II), XeF-
3, se ha investigado como un posible primer ejemplo de una molécula AX3E3, que podría esperarse por el razonamiento VSEPR que tuviera seis pares de electrones en una disposición octaédrica con los tres pares solitarios y los tres ligandos en orientaciones en forma de mer o T. Aunque este anión se ha detectado en la fase gaseosa, los intentos de síntesis en solución y la determinación experimental de la estructura no tuvieron éxito. Un estudio de química computacional mostró una geometría planar distorsionada en forma de Y con el menor ángulo de enlace F-Xe-F igual a 69°, en lugar de 90° como en una geometría en forma de T.