Nombre genérico: poliestireno sulfonato de sodio
Forma farmacéutica: suspensión oral/rectal
Revisado médicamente por Drugs.com. Actualizado por última vez el 22 de julio de 2020.
- Descripción general
- Efectos secundarios
- Dosificación
- Profesional
- Interacciones
- Más
- Indicaciones y uso de Kionex
- Dosis y administración de Kionex
- Información general
- Dosificación recomendada
- Preparación y administración
- Formas de dosificación y concentraciones
- Contraindicaciones
- Advertencias y precauciones
- Necrosis intestinal
- Alteraciones electrolíticas
- Sobrecarga de líquidos en pacientes sensibles a la ingesta elevada de sodio
- Riesgo de aspiración
- Unión a otros medicamentos administrados por vía oral
- Reacciones adversas
- Interacciones con otros medicamentos
- Interacciones generales
- Antácidos donadores de cationes
- Sorbitol
- USO EN POBLACIONES ESPECÍFICAS
- Embarazo
- Lactancia
- Uso pediátrico
- Sobredosificación
- Descripción de Kionex
- Kionex – Farmacología clínica
- Mecanismo de acción
- Farmacodinámica
- Farmacocinética
- Toxicología no clínica
- Carcinogénesis, mutagénesis, alteración de la fertilidad
- Cómo se suministra/almacenamiento y manipulación
- Información de asesoramiento al paciente
- PACKAGE/LABEL PRINCIPAL
- Más información sobre Kionex (poliestireno sulfonato de sodio)
- Recursos para el consumidor
- Recursos para profesionales
- Guías de tratamiento relacionadas
Indicaciones y uso de Kionex
Kionexis indicado para el tratamiento de la hipercalemia.
Limitación de uso:
Kionex no debe utilizarse como tratamiento de urgencia para la hiperpotasemia potencialmente mortal debido a su retraso en el inicio de acción.
Dosis y administración de Kionex
Información general
Administrar Kionex al menos 3 horas antes o 3 horas después de otros medicamentos orales. Los pacientes con gastroparesia pueden requerir una separación de 6 horas
Dosificación recomendada
La intensidad y la duración del tratamiento dependen de la gravedad y la resistencia de la hiperpotasemia.
Oral
La dosis total media diaria de Kionex para adultos es de 15 g a 60 g, administrada como una dosis de 15 g (cuatro cucharaditas rasas), de una a cuatro veces al día.
Rectal
La dosis media para adultos es de 30 g a 50 g cada seis horas.
Preparación y administración
Preparar la suspensión en fresco y utilizarla antes de 24 horas.
No calentar Kionex ya que podría alterar las propiedades de intercambio de la resina.
Una cucharadita rasa contiene aproximadamente 3,5 g de Kionex y 15 mEq de sodio.
Suspensión oral
Suspender cada dosis en una pequeña cantidad de agua o jarabe, aproximadamente 3 a 4 mL de líquido por gramo de resina. Administrar con el paciente en posición vertical.
Enema
Después de un enema de limpieza inicial, insertar un tubo de goma suave de tamaño grande (francés 28) en el recto a una distancia de unos 20 cm, con la punta bien metida en el colon sigmoide, y pegar con cinta adhesiva.
Administrar como una emulsión tibia (temperatura corporal) en 100 mL de vehículo acuoso y enjuagar con 50 a 100 ml de líquido. Puede utilizarse una suspensión algo más espesa, pero no formar una pasta.
Agitar la emulsión suavemente durante la administración. La resina debe retenerse durante el mayor tiempo posible y seguir con un enema de limpieza con una solución que no contenga sodio. Asegúrese de que se utiliza un volumen adecuado de solución de limpieza (hasta 2 litros).
Formas de dosificación y concentraciones
Kionex es un polvo de color crema a marrón claro, finamente molido y está disponible en tarros de 454 g.
Contraindicaciones
Kionex está contraindicado en pacientes con las siguientes condiciones:
– Hipersensibilidad a las resinas de sulfonato de poliestireno – Enfermedad intestinal obstructiva – Neonatos con motilidad intestinal reducida
Advertencias y precauciones
Necrosis intestinal
Se han notificado casos de necrosis intestinal, algunos mortales, y otros acontecimientos adversos gastrointestinales graves (hemorragia, colitis isquémica, perforación) en asociación con el uso de Kionex. En la mayoría de estos casos se informó del uso concomitante de sorbitol. Los factores de riesgo para los efectos adversos gastrointestinales estaban presentes en muchos de los casos, incluyendo la prematuridad, los antecedentes de enfermedad o cirugía intestinal, la hipovolemia y la insuficiencia e insuficiencia renal. No se recomienda la administración concomitante de sorbitol.
– Utilizar sólo en pacientes que tengan una función intestinal normal. Evitar su uso en pacientes que no hayan tenido una evacuación intestinal en el postoperatorio. – Evitar su uso en pacientes con riesgo de desarrollar estreñimiento o impactación (incluyendo aquellos con antecedentes de impactación, estreñimiento crónico, enfermedad inflamatoria intestinal, colitis isquémica, aterosclerosis intestinal vascular, resección intestinal previa u obstrucción intestinal). Suspender el uso en pacientes que desarrollen estreñimiento.
Alteraciones electrolíticas
Monitorear el potasio sérico durante la terapia porque puede ocurrir una hipocalemia severa.
Kionex no es totalmente selectivo para el potasio, y también se pueden perder pequeñas cantidades de otros cationes como el magnesio y el calcio durante el tratamiento. Vigilar el calcio y el magnesio en los pacientes que reciben Kionex.
Sobrecarga de líquidos en pacientes sensibles a la ingesta elevada de sodio
Cada dosis de 15 g de Kionex contiene 1500 mg (60 mEq) de sodio. Vigilar a los pacientes sensibles a la ingesta de sodio (insuficiencia cardíaca, hipertensión, edema) para detectar signos de sobrecarga de líquidos. Puede ser necesario ajustar otras fuentes de sodio.
Riesgo de aspiración
Se han notificado casos de bronquitis aguda o bronconeumonía causados por la inhalación de partículas de poliestireno sulfonato sódico. Los pacientes con reflejo nauseoso deteriorado, nivel de conciencia alterado o pacientes propensos a la regurgitación pueden estar en mayor riesgo. Administrar Kionex con el paciente en posición erguida.
Unión a otros medicamentos administrados por vía oral
Kionex puede unirse a medicamentos administrados por vía oral, lo que podría disminuir su absorción gastrointestinal y conducir a una eficacia reducida. Administrar otros medicamentos orales al menos 3 horas antes o 3 horas después de Kionex. Los pacientes con gastroparesia pueden requerir una separación de 6 horas. .
Reacciones adversas
Las siguientes reacciones adversas se discuten en otra parte del etiquetado:
– Necrosis intestinal – Alteraciones electrolíticas – Aspiración
Las siguientes reacciones adversas se han identificado durante el uso posterior a la aprobación de Kionex. Debido a que estas reacciones se notifican voluntariamente a partir de una población de tamaño incierto, no siempre es posible estimar su frecuencia de forma fiable o establecer una relación causal con la exposición al medicamento.
Gastrointestinales: anorexia, estreñimiento, diarrea, impactación fecal, concreciones gastrointestinales (bezoares), colitis isquémica, náuseas, ulceraciones, vómitos, irritación gástrica, obstrucción intestinal (debido a la concentración de hidróxido de aluminio)
Metabólicas: alcalosis sistémica
Interacciones con otros medicamentos
Interacciones generales
No se han realizado estudios formales de interacción con otros medicamentos en humanos.
Kionex tiene el potencial de unirse a otros medicamentos. En estudios de unión in vitro, se demostró que Kionex se une significativamente a los medicamentos orales (n=6) que se probaron. También se ha notificado una disminución de la absorción de litio y tiroxina con la coadministración de Kionex. La unión de Kionex a otros medicamentos orales podría causar una disminución de la absorción gastrointestinal y la pérdida de eficacia cuando se toma cerca del momento en que se administra Kionex. Administrar Kionex al menos 3 horas antes o 3 horas después de otros medicamentos orales. Los pacientes con gastroparesia pueden requerir una separación de 6 horas. Vigilar la respuesta clínica y/o los niveles sanguíneos cuando sea posible.
Antácidos donadores de cationes
La administración oral simultánea de Kionex con antiácidos donadores de cationes no absorbibles y laxantes puede reducir la capacidad de intercambio de potasio de la resina y aumentar el riesgo de alcalosis sistémica.
Sorbitol
El sorbitol puede contribuir al riesgo de necrosis intestinal y no se recomienda su uso concomitante.
USO EN POBLACIONES ESPECÍFICAS
Embarazo
Resumen de riesgos
Kionex no se absorbe sistémicamente tras su administración oral o rectal y no se espera que su uso por parte de la madre provoque riesgo fetal.
Lactancia
Resumen de riesgos
Kionex no se absorbe sistémicamente por la madre, por lo que no se espera que la lactancia suponga un riesgo para el lactante.
Uso pediátrico
No se han realizado estudios de seguridad y eficacia en pacientes pediátricos.
En los pacientes pediátricos, al igual que en los adultos, se espera que Kionex fije el potasio a la relación de intercambio práctica de 1mEq de potasio por 1 gramo de resina.
En los neonatos, Kionex no debe administrarse por vía oral. Tanto en niños como en neonatos, una dosis excesiva o una dilución inadecuada podría provocar la impactación de la resina. Los bebés prematuros o de bajo peso al nacer pueden tener un mayor riesgo de efectos adversos gastrointestinales con Kionex. uso.
Sobredosificación
La sobredosificación puede dar lugar a alteraciones electrolíticas, incluyendo hipopotasemia, hipocalcemia e hipomagnesemia. Deben tomarse las medidas apropiadas para corregir los electrolitos séricos (potasio, calcio, magnesio), y la resina debe eliminarse del tracto alimentario mediante el uso apropiado de laxantes o enemas.
Descripción de Kionex
Kionex es un polímero de benceno, dietileno, con etilbenceno, sulfonado, sal de sodio y tiene la siguiente fórmula estructural:
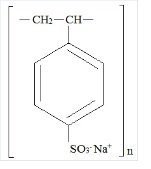
El medicamento es una forma de polvo de color crema a marrón claro, finamente molido, de poliestireno sulfonato de sodio, una resina de intercambio catiónico preparada en la fase sódica con una capacidad de intercambio in vitro de aproximadamente 3.1 mEq (in vivo aproximadamente 1 mEq) de potasio por gramo. El contenido de sodio es de aproximadamente 100 mg (4,1 mEq) por gramo de la droga. Puede administrarse por vía oral o rectal en forma de enema.
Un gramo de Kionex contiene 4,1 mEq de sodio.
Kionex – Farmacología clínica
Mecanismo de acción
Kionex es un polímero de intercambio catiónico no absorbido que contiene un contraión de sodio.
Kionex aumenta la excreción fecal de potasio a través de la unión del potasio en la luz del tracto gastrointestinal. La unión del potasio reduce la concentración de potasio libre en el lumen gastrointestinal, dando como resultado una reducción de los niveles de potasio en suero. La relación de intercambio práctica es de 1 mEq K por 1 gramo de resina.
A medida que la resina pasa a lo largo del intestino o es retenida en el colon tras su administración por enema, los iones de sodio se liberan parcialmente y son sustituidos por iones de potasio. Esta acción ocurre principalmente en el intestino grueso, que excreta iones de potasio en mayor medida que el intestino delgado. La eficacia de este proceso es limitada e impredeciblemente variable.
Farmacodinámica
La disminución efectiva del potasio sérico con Kionex puede tardar de horas a días.
Farmacocinética
La eficacia in vivo de las resinas de intercambio sodio-potasio es de aproximadamente el 33 por ciento; por lo tanto, aproximadamente un tercio del contenido real de sodio de la resina se entrega al organismo.
Kionex no se absorbe sistémicamente.
Interacciones con otros medicamentos
Los estudios de unión in vitro mostraron que Kionex se unió significativamente a los siguientes medicamentos probados: warfarina, metoprolol, fenitoína, furosemida, amlodipino y amoxicilina.
Toxicología no clínica
Carcinogénesis, mutagénesis, alteración de la fertilidad
No se han realizado estudios.
Cómo se suministra/almacenamiento y manipulación
Kionex se presenta como un polvo de color crema a marrón claro, finamente molido, en tarros de 1 libra (454 g), NDC 0574-2004-16.
Conservar a 20° a 25°C (68° a 77°F) .
Información de asesoramiento al paciente
Interacciones con otros medicamentos
Aconsejar a los pacientes que estén tomando otra medicación oral que separen la dosis de Kionex al menos 3 horas (antes o después)
Sólo con receta
Envasado por
Perrigo
Minneapolis, MN 55427
Revisado el 08/2017
PACKAGE/LABEL PRINCIPAL
Rx Only
NDC 0574-2004-16
Kionex®
Sodium Polystyrene Sulfonate for Suspension
AVERAGE ADULT DOSE: 15 g (aproximadamente 4 cucharaditas rasas) de una a cuatro veces al día en agua. Ver información de prescripción completa.
El efecto debe ser cuidadosamente controlado mediante determinaciones frecuentes de potasio sérico en cada período de 24 horas. El contenido de sodio es de aproximadamente 60 mEq por 15 g.
La suspensión debe estar recién preparada y no debe almacenarse más de 24 horas. Dispensar en envases herméticos y resistentes a la luz como se define en la USP.
ALMACENAMIENTO: Almacenar entre 20° y 25°C (68° y 77°F).
Leer el prospecto.
454 gramos (1 LB)
| Poliestireno sulfonato de sodio en polvo Kionex , para suspensión |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Etiquetador – Laboratorios Paddock, LLC (967694121)
Más información sobre Kionex (poliestireno sulfonato de sodio)
- Efectos secundarios
- Durante el embarazo o la lactancia
- Información sobre la dosis
- Interacciones con otros medicamentos
- En español
- 4 Reseñas
- Clase de medicamentos: resinas de intercambio catiónico
- Alertas de la FDA (2)
Recursos para el consumidor
- Información para el paciente
- Kionex (lectura avanzada)
Recursos para profesionales
- Información para la prescripción
- Poliestireno Sulfonato de sodio en polvo oral (FDA)
Otras marcas Kayexalate, Kalexate
Guías de tratamiento relacionadas
- Hiperpotasemia
Aviso médico