Autorregulación del flujo sanguíneo cerebral
La autorregulación del flujo sanguíneo cerebral es la capacidad del cerebro para mantener un flujo sanguíneo relativamente constante a pesar de los cambios en la presión de perfusión . La autorregulación está presente en muchos lechos vasculares, pero está particularmente bien desarrollada en el cerebro, probablemente debido a la necesidad de un suministro constante de sangre y a la homeostasis del agua. En adultos normotensos, el flujo sanguíneo cerebral se mantiene en ~50 mL por 100 g de tejido cerebral por minuto, siempre que la PPC esté en el rango de ~60 a 160 mmHg . Por encima y por debajo de este límite, la autorregulación se pierde y el flujo sanguíneo cerebral pasa a depender de la presión arterial media de forma lineal . Cuando la PPC cae por debajo del límite inferior de la autorregulación, se produce una isquemia cerebral. La reducción del flujo sanguíneo cerebral se compensa con un aumento de la extracción de oxígeno de la sangre. Los signos o síntomas clínicos de isquemia no se observan hasta que la disminución de la perfusión supera la capacidad del aumento de la extracción de oxígeno para satisfacer las necesidades metabólicas. En este punto, se producen signos clínicos de hipoperfusión, como mareos, alteración del estado mental y, finalmente, daño tisular irreversible (infarto).
Los mecanismos de autorregulación en el cerebro no se conocen por completo y probablemente difieren con los aumentos frente a las disminuciones de presión. Aunque resulta atractiva la participación de las neuronas en la autorregulación, los estudios han demostrado que la autorregulación del flujo sanguíneo cerebral se conserva en animales denervados simpática y parasimpáticamente, lo que indica que es improbable una contribución importante de los factores neurogénicos extrínsecos a la autorregulación del flujo sanguíneo cerebral (véase Inervación perivascular). Recientemente, se ha demostrado el papel del óxido nítrico neuronal en la modulación de la autorregulación del flujo sanguíneo cerebral, lo que sugiere que, aunque la inervación extrínseca no esté implicada, la inervación intrínseca puede tener un papel . También se ha propuesto que los biproductos del metabolismo desempeñen un papel en la autorregulación . Las reducciones del flujo sanguíneo cerebral estimulan la liberación de sustancias vasoactivas del cerebro que provocan la dilatación arterial. Los candidatos a estas sustancias vasoactivas incluyen H+, K+, O2, adenosina y otros. La autorregulación del flujo sanguíneo cerebral cuando la presión fluctúa en el extremo superior de la curva de autorregulación se debe muy probablemente al comportamiento miogénico del músculo liso cerebral que se constriñe en respuesta a la presión elevada y se dilata en respuesta a la presión reducida . La importante contribución de la actividad miogénica a la autorregulación está demostrada in vitro en arterias cerebrales aisladas y presurizadas que se constriñen en respuesta a la presión elevada y se dilatan en respuesta a la presión reducida (véase Respuesta miogénica). La autorregulación a presiones por debajo del rango de presión miogénica probablemente implique la hipoxia y la liberación de factores metabólicos.
La importancia de la autorregulación en la función cerebral normal se pone de manifiesto por el hecho de que se produce una lesión cerebral significativa cuando se pierden los mecanismos de autorregulación. Por ejemplo, durante la hipertensión aguda a presiones superiores al límite de autorregulación, la constricción miogénica del músculo liso vascular es superada por la excesiva presión intravascular y se produce una dilatación forzada de los vasos cerebrales . La pérdida del tono miogénico durante la dilatación forzada disminuye la resistencia cerebrovascular, un resultado que puede producir un gran aumento del flujo sanguíneo cerebral (300-400%), conocido como ruptura autorreguladora (Figura 16). Además, la disminución de la resistencia cerebrovascular aumenta la presión hidrostática sobre el endotelio cerebral, provocando la formación de edema , la causa subyacente de afecciones como la encefalopatía hipertensiva, el síndrome de encefalopatía posterior reversible (PRES) y la eclampsia (véase Formación de edema vasogénico).
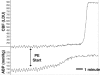
Figura 16
Rastreo del CBF (en unidades Doppler láser) y la ABP (en mmHg) en respuesta a dosis crecientes de PE. En este experimento, el CBF aumentó cuatro veces más que la línea de base a medida que la ABP aumentó de 140 a 210 mmHg, lo que demuestra la ruptura autorreguladora. Utilizado (más…)
Aunque poco frecuente desde la aparición de un tratamiento antihipertensivo eficaz, la encefalopatía hipertensiva se produce como resultado de un aumento repentino y sostenido de la presión arterial suficiente para superar el límite superior de la autorregulación del flujo sanguíneo cerebral (>160 mmHg) . Los primeros estudios sobre la reacción de los vasos cerebrales a la presión arterial elevada dieron lugar al concepto de vasoespasmo hipertensivo. Se pensaba que la encefalopatía hipertensiva aguda era el resultado de un espasmo -definido como una vasoconstricción incontrolada- de las arterias cerebrales, que provocaba una isquemia del tejido cerebral. Este concepto se originó a partir de las observaciones de Byrom, quien produjo una hipertensión renal experimental y descubrió que el 90 % de las ratas hipertensas con manifestaciones neurológicas mostraban múltiples manchas corticales de extravasación de azul tripán, mientras que las ratas sin síntomas cerebrales parecían tener una permeabilidad cerebrovascular normal. También observó lo que denominó una alternancia de vasoconstricción/vasodilatación en los vasos piales, un fenómeno conocido como apariencia de «cuerda de salchicha». Esta observación le llevó a la conclusión de que el vasoespasmo cerebral causaba isquemia y formación de edema en respuesta a la hipertensión aguda. Más tarde, Byrom modificó su punto de vista y se refirió a un hallazgo en la circulación mesentérica de que los vasos con este aspecto de «cuerda de salchicha» tenían fugas de proteínas sólo en las partes dilatadas de los vasos… Desde entonces, se ha establecido que la presión arterial alta provoca un aumento del flujo sanguíneo cerebral y la «ruptura de la autorregulación». Otros experimentos confirmaron que la pérdida de la vasoconstricción miogénica durante la dilatación forzada, y no el espasmo, es el acontecimiento crítico en la encefalopatía hipertensiva.