L’anemia emolitica autoimmune (AIHA) è mediata da anticorpi, e nella maggior parte dei casi l’immunoglobulina (Ig) G è l’anticorpo mediatore. Questo tipo di AIHA viene definito AIHA “caldo” perché gli anticorpi IgG si legano meglio alla temperatura del corpo. L’AIHA “freddo” è mediato dagli anticorpi IgM, che si legano al massimo a temperature inferiori a 37°C. L’AIHA causata da una reazione ai farmaci è rara, con un’incidenza annuale stimata di 1:1.000.000 per l’AIHA grave correlata ai farmaci.1 Questo articolo passa in rassegna la gestione dei tipi più comuni di AIHA, con particolare attenzione all’AIHA calda, fredda e indotta dai farmaci; la valutazione e la diagnosi dell’AIHA sono esaminate in un articolo separato.
Anemia emolitica autoimmune calda
Nell’AIHA, l’emolisi è mediata da anticorpi che si legano alla superficie dei globuli rossi. L’AIHA in cui gli anticorpi IgG sono gli anticorpi incriminati viene definita AIHA calda. “Caldo” si riferisce al fatto che l’anticorpo si lega meglio alla temperatura corporea (37°C). Nell’AIHA caldo, i test mostreranno molecole IgG attaccate alla superficie dei globuli rossi, e il 50% dei pazienti mostrerà anche C3. Tra il 50% e il 90% dei casi di AIHA sono dovuti ad anticorpi caldi.2,3 L’incidenza dell’AIHA caldo varia a seconda delle serie, ma è di circa 1 caso ogni 100.000 pazienti all’anno; questa forma di emolisi colpisce le donne più frequentemente degli uomini.4,5
Opzioni terapeutiche
Prima linea
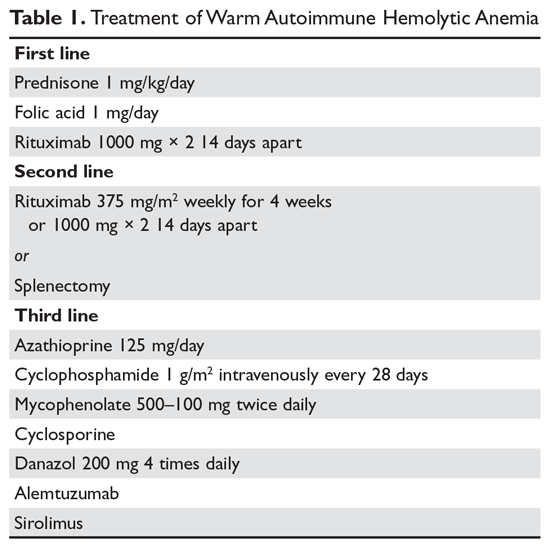
Steroidi. L’obiettivo della terapia nell’AIHA caldo può essere difficile da definire. Tuttavia, la maggior parte concorda sul fatto che un ematocrito superiore al 30% (o superiore per prevenire i sintomi) con un aumento minimo della conta dei reticolociti – che riflette un processo emolitico significativamente rallentato – è un obiettivo ragionevole. La gestione iniziale dell’AIHA caldo è il prednisone alla dose standard di 1 mg/kg al giorno (Tabella 1).6,7 I pazienti devono anche iniziare a prendere inibitori della pompa protonica per prevenire le ulcere. I pazienti possono impiegare fino a 3 settimane per rispondere alla terapia con prednisone. Una volta che l’ematocrito del paziente è superiore al 30%, il prednisone viene lentamente ridotto. Anche se circa l’80% dei pazienti risponde agli steroidi, solo il 30% può essere completamente eliminato dagli steroidi. Per i pazienti che possono essere mantenuti con una dose giornaliera di steroidi di 10 mg o meno, gli steroidi possono essere la terapia a lungo termine più ragionevole. Inoltre, poiché l’emolisi attiva porta a una maggiore richiesta di acido folico, ai pazienti con AIHA caldo viene spesso prescritto acido folico 1 mg al giorno per prevenire l’anemia megaloblastica dovuta alla carenza di acido folico.
Rituximab. Sempre più spesso, la terapia con rituximab (anti-CD20) viene aggiunta agli steroidi iniziali. Due studi clinici hanno mostrato un aumento delle risposte sia a lungo che a breve termine con l’uso del rituximab.8,9 Una considerazione importante è che la maggior parte dei pazienti risponde gradualmente al rituximab nel corso di settimane, quindi non ci si deve aspettare una risposta rapida. La maggior parte degli studi ha utilizzato il dosaggio tradizionale di 375 mg/m2 settimanali per 4 settimane. Queste risposte sembrano essere durevoli, ma come nella trombocitopenia immune (ITP), il trattamento ripetuto con rituximab è efficace.
I principali effetti collaterali del rituximab sono le reazioni all’infusione, che sono spesso peggiori con la prima dose. Queste reazioni possono essere controllate con antistaminici, steroidi e, per rigori gravi, meperidina. Raramente, i pazienti possono sviluppare neutropenia (circa 1:500) che sembra essere di natura autoimmune. Le infezioni sembrano essere solo minimamente aumentate con l’uso di rituximab.10 Un gruppo a rischio sono i portatori cronici del virus dell’epatite B, che possono avere una riattivazione del virus che può essere fatale. Pertanto, i pazienti considerati per il rituximab devono essere sottoposti a screening per lo stato di portatore del virus dell’epatite B.11 I pazienti che ricevono rituximab sono a rischio molto lieve di leucoencefalopatia multifocale progressiva, che è più comune nei pazienti con cancro e nei pazienti fortemente immunosoppressi. Il rischio complessivo non è noto ma è inferiore a 1:50.000.
.