Introduzione
Il cancro del pancreas si riferisce tipicamente al carcinoma duttale del pancreas, che comprende fino al 90% dei tumori primari del pancreas. Il numero rimanente può essere diviso in tumori esocrini (come il carcinoma cistico del pancreas) e tumori endocrini (derivati dalle cellule delle isole del pancreas).
Il cancro del pancreas ha un alto tasso di mortalità, essendo la quarta causa più comune di morte per cancro nel Regno Unito. È raro sotto i 40 anni di età, con l’80% dei casi che si verificano tra i 60-80 anni. Raramente viene diagnosticato abbastanza presto per un trattamento curativo.
In questo articolo, vedremo i fattori di rischio, le indagini e la gestione di un paziente con cancro pancreatico.
Patofisiologia
Il tipo più comune di cancro pancreatico è il carcinoma duttale (90% dei tumori maligni pancreatici primari). Altre forme più rare includono tumori cistici, tumori a cellule ampollari e tumori a cellule isolate, che spesso hanno tutti una prognosi molto migliore.
Quando il cancro si diffonde, l’invasione diretta delle strutture locali coinvolge tipicamente la milza, il colon trasverso e le ghiandole surrenali. Le metastasi linfatiche coinvolgono tipicamente i linfonodi regionali, il fegato, i polmoni e il peritoneo. Le metastasi sono comuni al momento della diagnosi.
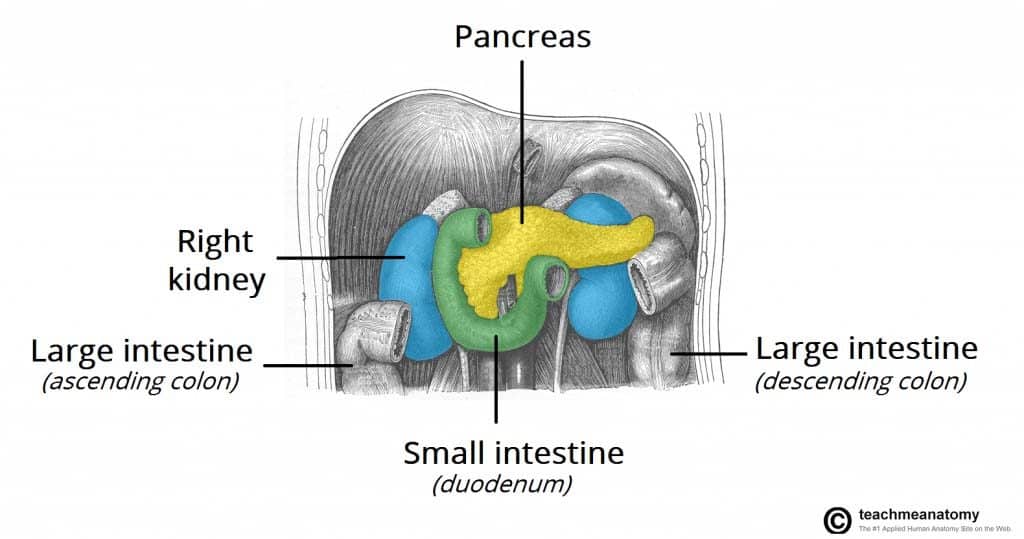 Figura 1 – Il cancro del pancreas può diffondersi direttamente alle strutture circostanti, come la milza, il colon trasverso e la ghiandola surrenale.
Figura 1 – Il cancro del pancreas può diffondersi direttamente alle strutture circostanti, come la milza, il colon trasverso e la ghiandola surrenale.Fattori di rischio
Ci sono pochi chiari fattori di rischio per lo sviluppo del carcinoma del pancreas. Quelli che sono stati identificati includono il fumo e la pancreatite cronica. Ci può essere anche un elemento ereditario, dato che il 7% dei pazienti ha una storia familiare della malattia.
Il diabete mellito ad insorgenza tardiva è un ulteriore fattore di rischio. Quelli con diagnosi di diabete >50 anni hanno un rischio 8 volte maggiore di sviluppare un carcinoma pancreatico nei tre anni successivi rispetto alla popolazione generale.
Presentazione clinica
Circa l’80% dei casi di carcinoma pancreatico non sono resecabili alla diagnosi, a testimonianza della natura tardiva e spesso vaga e aspecifica della sua presentazione.
Le caratteristiche cliniche specifiche* possono dipendere dalla sede del tumore:
- Ittero ostruttivo – dovuto alla compressione del dotto biliare comune (presente nel 90% dei casi al momento della diagnosi), tipicamente indolore
- Perdita di peso – dovuta agli effetti metabolici del cancro, o secondaria alla disfunzione esocrina
- Dolore addominale (aspecifico) – dovuto all’invasione del plesso celiaco o secondario alla pancreatite
Presentazioni meno comuni includono pancreatite acuta o tromboflebite migrans (una tromboflebite superficiale migratoria ricorrente, causata da uno stato paraneoplastico ipercoagulabile).
*I tumori della coda del pancreas hanno un decorso insidioso e spesso non sono sintomatici fino ad uno stadio avanzato
All’esame, i pazienti possono apparire cachettici, malnutriti e itterici. Alla palpazione, si può sentire una massa addominale nella regione epigastrica, così come una cistifellea ingrossata (come da legge di Courvoisier)
Legge di Courvoisier
La legge di Courvoisier afferma che in presenza di ittero e cistifellea ingrossata/palpabile, la malignità dell’albero biliare o del pancreas dovrebbe essere fortemente sospettata, dato che è improbabile che la causa siano i calcoli biliari.
Questo segno può essere presente se il tumore che ostruisce è distale al dotto cistico. In realtà una cistifellea ingrossata è presente in meno del 25% dei pazienti con cancro pancreatico.
Diagnosi differenziale
Il cancro pancreatico si presenta spesso con caratteristiche vaghe e aspecifiche. Le diagnosi differenziali sono vaste e includono:
- Cause di ittero ostruttivo – malattia della colecisti, colangiocarcinoma, stenosi benigna della colecisti
- Cause di dolore addominale epigastrico – calcoli biliari, malattia dell’ulcera peptica, carcinoma gastrico, sindrome coronarica acuta
Indagini
Esami di laboratorio
Ogni sospetto di cancro al pancreas dovrebbe giustificare esami del sangue iniziali, tra cui FBC (anemia o trombocitopenia) e LFT (bilirubina, fosfatasi alcalina e gamma-GT elevati, che mostrano un quadro di ittero ostruttivo).
IlCA19-9 è un marcatore tumorale con un’alta sensibilità e specificità per il cancro pancreatico, ma il suo ruolo è nella valutazione della risposta al trattamento piuttosto che nella diagnosi iniziale.
Imaging
L’imaging iniziale per il cancro pancreatico è comunemente un’ecografia addominale, che può dimostrare una massa pancreatica o un albero biliare dilatato (così come potenziali metastasi epatiche e ascite se la malattia è in stadio molto avanzato).
La tomografia computerizzata (utilizzando un protocollo pancreatico, Fig. 2) è sia l’indagine più importante in termini di diagnosi, ma anche la più prognosticamente informativa in quanto può mettere in scena la progressione della malattia. Una TAC torace-addome-pelvi sarà ulteriormente necessaria una volta che il cancro pancreatico è stato diagnosticato per la stadiazione; una PET-CT può essere giustificata in quelli con malattia localizzata alla TAC che saranno sottoposti a trattamento oncologico
L’ecografia endoscopica (EUS) può essere successivamente utilizzata per guidare la biopsia con ago aspirato al fine di valutare istologicamente la lesione, se la diagnosi non è ancora chiara. L’ERCP può anche essere utilizzata per accedere alla lesione per la biopsia o la citologia, se in una posizione adatta*.
*Un brushing biliare per la citologia se l’ERCP viene utilizzata per alleviare l’ostruzione biliare e non c’è una diagnosi di tessuto.
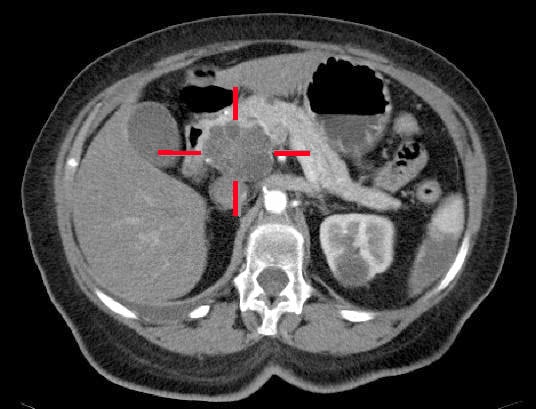 Figura 2 – Un adenocarcinoma situato nella testa del pancreas, identificato alla TAC
Figura 2 – Un adenocarcinoma situato nella testa del pancreas, identificato alla TACGestione
Chirurgia
L’unica opzione di gestione curativa è attualmente la resezione radicale:
- Per i pazienti con tumori della testa del pancreas, l’intervento più comune con intento curativo è la pancreaticoduodenectomia, nota anche come procedura di Whipple
- Per i pazienti con tumori del corpo o della coda del pancreas, in alcuni casi si può tentare una resezione conservativa del piloro
- , una pancreatectomia distale può spesso essere eseguita
Le controindicazioni assolute alla chirurgia includono metastasi peritoneali, epatiche e a distanza. C’è un’alta morbilità associata a queste procedure (fino al 40%) e le complicazioni specifiche includono la formazione di una fistola pancreatica, lo svuotamento gastrico ritardato e l’insufficienza pancreatica.
Una revisione Cochrane ha trovato che la resezione pancreatica aumenta la sopravvivenza e riduce i costi rispetto ai trattamenti palliativi nei pazienti con cancro pancreatico localmente avanzato e coinvolgimento venoso, assumendo che ci sia sufficiente esperienza clinica disponibile.
Procedura di Whipple
La procedura di Whipple prevede la rimozione della testa del pancreas, dell’antrum dello stomaco, della prima e seconda parte del duodeno, del dotto biliare comune e della cistifellea.
Tutti i visceri rimossi nell’operazione lo fanno a causa del loro approvvigionamento arterioso comune (l’arteria gastroduodenale), condiviso dalla testa del pancreas e dal duodeno.
In seguito, la coda del pancreas e il dotto epatico vengono attaccati al digiuno, permettendo il drenaggio della bile e dei succhi pancreatici nell’intestino, mentre lo stomaco viene successivamente anastomizzato con il digiuno permettendo il passaggio del cibo.
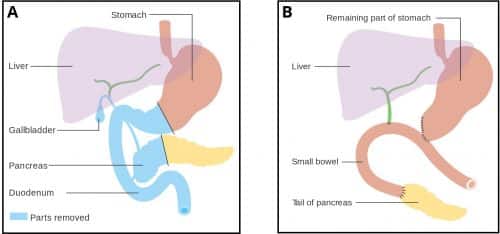 Figura 3 – Pancreaticoduodenectomia (procedura di Whipple). A: Pre-procedura, B: Post-procedura
Figura 3 – Pancreaticoduodenectomia (procedura di Whipple). A: Pre-procedura, B: Post-procedura
Chemotherapy
La chemioterapia adiuvante, generalmente con 5-flourouracil, è raccomandata dopo l’intervento in quanto è stato dimostrato che migliora la sopravvivenza in seguito al trial ESPAC-1*.
Nella malattia metastatica l’uso del regime FOLFIRINOX (acido folinico, 5-fluorouracile, irinotecan e oxaliplatino) è consigliato in coloro che hanno un buon performance status, tuttavia ha prodotto solo modesti miglioramenti nella sopravvivenza; la terapia con gemcitabina può essere considerata per le persone con cancro pancreatico localmente avanzato che non stanno abbastanza bene da tollerare FOLFIRINOX.
*ESPAC-1 ha anche dimostrato che i pazienti trattati con chemioradioterapia adiuvante hanno avuto esiti complessivi peggiori di quelli trattati con la sola chemioterapia adiuvante.
Cure palliative
La maggior parte dei pazienti con carcinoma pancreatico non sono candidati alla chirurgia curativa, ma richiedono invece il coinvolgimento delle cure palliative.
L’ittero ostruttivo e la prurite associata possono essere alleviati con l’inserimento di uno stent biliare, sia tramite ERCP che per via percutanea.
La chemioterapia palliativa, come quella basata sulla gemcitabina, può essere provata nei pazienti con un performance status ragionevole.
L’insufficienza ocrina è comune nella malattia avanzata o in coloro che hanno subito un’escissione significativa del pancreas, e porta a malassorbimento e steatorrea; questo può essere inizialmente trattato con sostituti enzimatici (comprese le lipasi), come Creon®.
Prognosi
Il cancro pancreatico ha un’alta capacità metastatica anche nei tumori piccoli. La prognosi del cancro del pancreas rimane molto scarsa, con un tasso di sopravvivenza globale a 5 anni <5%.
Punti chiave
- Il cancro pancreatico si presenta spesso con una combinazione di ittero ostruttivo, dolore addominale o perdita di peso
- La maggior parte dei casi sono inizialmente rilevati sulla TAC, tuttavia richiedono una diagnosi su tessuto tramite biopsia; Il CA19-9 è un marker tumorale usato per monitorare la progressione della malattia
- La gestione definitiva è la resezione chirurgica, spesso con chemioterapia adiuvante
- Il cancro del pancreas ha un tasso di sopravvivenza a 5 anni inferiore al 5%
Tumori endocrini del pancreas
I tumori endocrini del pancreas possono essere funzionali o non funzionali. I tumori funzionali secernono attivamente ormoni e i loro segni e sintomi sono legati a questo, mentre i tumori non funzionali non secernono ormoni attivi e le caratteristiche cliniche sono legate esclusivamente alla loro diffusione maligna.
I tumori endocrini del pancreas sono spesso associati alla sindrome della neoplasia endocrina multipla 1 (MEN1); MEN1 consiste tipicamente di iperparatiroidismo, tumori endocrini del pancreas e tumori ipofisari (più comunemente prolattinomi).
Caratteristiche cliniche
| Tipo di cellula | Ormone secreto (nome del tumore) | Funzione fisiologica normale | Caratteristiche del tumore funzionale |
| Cellule G | Gastrina (gastrinoma) | Stimola il rilascio di acido gastrico | Zollinger-Sindrome di Ellison, con conseguente ulcera peptica grave, refrattaria al trattamento medico, con diarrea e steatorrea |
| α Cellule | Glucagone (Glucagonoma) | Aumenta la concentrazione di glucosio nel sangue | Iperglicemia, diabete mellito, ed eritema migratorio necrolitico |
| Celluleβ | Insulina (insulinoma) | Riduzione della concentrazione di glucosio nel sangue | Ipoglicemia sintomatica, come sudorazione o cambiamento dello stato mentale, migliorando con il consumo di carboidrati |
| Celluleδ | Somatostatina (Somatostatinoma) | Inibisce il rilascio di GH, TSH e prolattina dall’ipofisi anteriore, e di gastrina | Diabete mellito, steatorrea, calcoli biliari (dovuti all’inibizione della colecistochinina), perdita di peso, e acloridria (a causa dell’inibizione della gastrina) |
| Cellule non isolanti | Peptide intestinale vasodilatatore (VIPoma) | Secrezione di acqua ed elettroliti nell’intestino. Rilassamento della muscolatura liscia enterica. | Diarrea acquosa profusa e prolungata, grave ipokaliemia e disidratazione (nota anche come sindrome di Verner-Morrison) |
Tabella 1 – Tumori endocrini del pancreas
Indagine
Tutti i casi dovrebbero essere discussi in una riunione multidisciplinare del team dove la gestione può essere guidata. Alcuni esami del sangue possono essere inviati, a seconda del sottotipo sospetto (Tabella 1)
I NET pancreatici sono meglio indagati con una combinazione di imaging CT, imaging MRI, e / o ecografia endoscopica. Anche il calcio intra-arterioso con angiografia a sottrazione digitale può essere usato nella localizzazione e valutazione di insulinomi e gastrinomi.
Gestione
I piccoli NET pancreatici ben differenziati non funzionali (<1cm) possono essere semplicemente osservati. I tumori più grandi o funzionanti sono resecati, con qualsiasi malattia metastatica distante anch’essa resecata se il tumore è di basso grado e le metastasi sono di basso volume.
Gli analoghi della somatostatina possono essere usati per controllare e migliorare gli effetti dell’ipersecrezione ormonale (anche nel caso dei somatostatinomi).
Si possono usare gli stessi metodi di trattamento dei NET.