Alcuni atomi sono più polari di altri a causa del fatto che sono più “avidi” di elettroni.
Dai un’occhiata alla tua tavola periodica, più vai a destra e verso l’alto più gli atomi diventano elettronegativi (esclusi i gas nobili perché hanno i gusci pieni e sono “felici” e non hanno bisogno di elettroni di valenza).
Credo che tutti abbiano sentito che il Floro (F), per esempio, è uno degli elementi più elettronegativi, strapperà letteralmente gli elettroni degli atomi di idrogeno o di carbonio. Così sarà Cloro (Cl)
Guarda questa immagine:
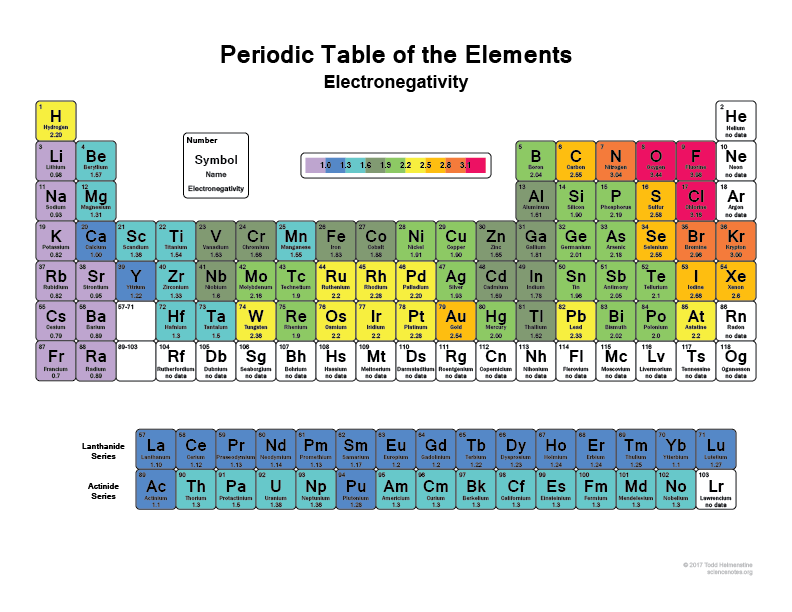
Ecco perché quando un legame alcune molecole hanno regioni super polari perché hanno qualcosa come l’idrogeno che si lega con qualcosa come la Farina che ha solo fondamentalmente gli elettroni con sé la maggior parte del tempo.
Questa domanda può anche essere spiegata dall’idea delle nuvole di elettroni e dal fatto che gli atomi più elettronegativi di solito hanno più elettroni che stanno con loro la maggior parte del tempo rispetto agli atomi non molto elettronegativi.

Questo si chiama momento di dipolo e senza entrare troppo nel merito si vede come la maggior parte degli elettroni sono più vicini all’ossigeno che all’idrogeno (perché l’ossigeno è più elettronegativo dell’idrogeno)
Tra l’altro la parola elettronegativo suona controintuitiva a volte ma è elettro-negativa invece che positiva perché in chimica gli atomi che guadagnano elettroni hanno un segno negativo (Es: #Cl^-# è un cloro che ha guadagnato un elettrone).