
Brønsted nel suo laboratorio
Secondo il concetto Brønsted-Lowry, il processo che prima era scritto come una semplice dissociazione di un generico acido HA (HA → H+ + A-) è più correttamente considerato come un processo di trasferimento protonico:
HA + H2O → A-+ H3O+(3-1)
L’idea, ancora una volta, è che il protone, una volta lasciato l’acido, deve finire attaccato a qualcosa (che chiamiamo una base;) non può semplicemente fluttuare come ione idrogeno libero.
- Coppie acido-base coniugate
- Acidi forti e acidi deboli
- Definizione di un acido “forte”
- L’effetto livellamento
- Acidi deboli
- Gli acidi forti hanno basi coniugate deboli
- I sali di acidi deboli si dissolvono per dare soluzioni alcaline
- Le uniche basi forti comuni sono gli idrossidi del gruppo 1
- I sali di basi deboli producono soluzioni acide
- Autoprotolisi
- Ampoliti
- Il sistema acido-base carbonato
Coppie acido-base coniugate
La reazione di un acido con una base è quindi una reazione di scambio protonico; se l’acido è indicato con AH e la base con B, allora possiamo scrivere una reazione acido-base generalizzata come
AH + B → A- + BH+(3-2)
Si noti che l’inverso di questa reazione,
BH+ + A- → B + AH(3-3)
è anche una reazione acido-base. Poiché le reazioni di trasferimento di protoni sono reversibili, ne consegue che il trasferimento di un protone da un acido a una base deve necessariamente creare una nuova coppia di specie che possono, almeno in linea di principio, costituire una coppia acido-base a sé stante, alla quale ci riferiamo come coppia acido-base coniugata:
Il termine coniugato significa “connesso con”, il che implica che i membri di qualsiasi coppia coniugata sono “connessi” dalla presenza o assenza di un protone.
Quali specie sono considerate “coniugate” dipende dalla direzione in cui è scritta la reazione, come mostrato di seguito per il trasferimento protonico di (3-1):


Similmente, per i trasferimenti protonici generalizzati (3-2) e (3-3), abbiamo


La tabella sottostante mostra le coppie coniugate di una serie di tipici sistemi acido-base.
| acido | base | ||
| acido cloridrico | HCl | ione cloruro | Cl- |
| acido acetico | CH3CH2COOH | ione acetato | CH3CH2COO- |
| acido nitrico | HNO3 | Ione nitrato | NO3- |
| Ione diidrogeno fosfato | H2PO4- | Ione monoidrogeno fosfato | HPO42- |
| Ione idrogeno solfato | HSO4- | Ione solfato | SO42- |
| idrogeno ione carbonato (“bicarbonato”) | HCO3- | ione carbonato | CO32- |
| ione ammonio | NH4+ | ammoniaca | NH3 |
| ione ferro (III) (“ferrico”) | Fe(H2O)63+ | pentaaquoironIII | Fe(H2O)5OH2+ |
| acqua | H2O | ione idrossido | OH- |
| ione idronio | H3O+ | acqua | H2O |
Acidi forti e acidi deboli
Possiamo considerare la reazione generalizzata acido-basebase generalizzata
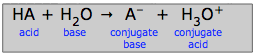
come una competizione di due basi per un protone:

Definizione di un acido “forte”
Se la base H2O vince in modo schiacciante questo tiro alla fune, allora si dice che l’acido HA è un acido forte. Questo è ciò che accade con l’acido cloridrico e gli altri comuni “acidi minerali” forti H2SO4, HNO3 e HClO4:
Le soluzioni di questi acidi in acqua sono in realtà soluzioni delle specie ioniche mostrate in grassetto sulla destra. Stando così le cose, ne consegue che ciò che chiamiamo una soluzione 1 M di “acido cloridrico” in acqua, per esempio, non contiene affatto una concentrazione significativa di HCl; l’unico vero acido presente in tale soluzione è H3O+!
Queste considerazioni danno luogo a due regole importanti che è necessario non solo conoscere, ma anche capire:
H3O+ è l’acido più forte che può esistere in acqua;
Tutti gli acidi forti sembrano essere altrettanto forti in acqua.
L’effetto livellamento
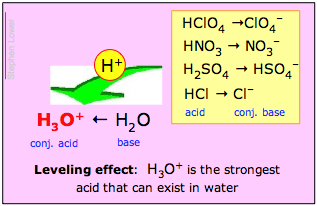
La seconda di queste affermazioni è chiamata effetto livellamento. Significa che anche se le forze intrinseche protone-donatore degli acidi forti differiscono, sono tutti completamente dissociati in acqua. I chimici dicono che le loro forze sono “livellate” dal solvente acqua.
Un effetto simile si vedrebbe se si tentasse di giudicare le forze di diversi adulti conducendo una serie di gare di tiro alla fune con un bambino piccolo. Ci si aspetterebbe che gli adulti vincessero in modo schiacciante ad ogni prova; la loro forza sarebbe stata “livellata” da quella del bambino.
Acidi deboli
La maggior parte degli acidi, tuttavia, sono in grado di trattenere i loro protoni più strettamente, quindi solo una piccola frazione dell’acido viene dissociata. Così l’acido cianidrico, HCN, è un acido debole in acqua perché il protone è in grado di condividere gli elettroni della coppia solitaria dello ione cianuro CN- più efficacemente di quanto possa fare con quelli dell’H2O, così la reazione
HCN + H2O → H3O+ + CN-
procede solo in misura molto piccola.
Siccome un acido forte lega il suo protone solo debolmente, mentre un acido debole lo lega strettamente, possiamo dire che
Gli acidi forti sono “deboli”; gli acidi deboli sono “forti”
Se sei capace di spiegare questo apparente paradosso, hai capito una delle idee più importanti della chimica acido-base!
|
reazione
|
acido
|
base
|
congiunto acido
|
base
|
| 1) autoionizzazione dell’acqua H2O | H2O | H2O | H3O+ | OH- |
| 2) ionizzazione dell’acido idrocianico HCN | HCN | H2O | H3O+ | CN- |
| 3) ionizzazione dell’ammoniaca NH3 in acqua | NH3 | H2O | NH4+ | OH- |
| 4) idrolisi del cloruro di ammonio NH4Cl | NH4+ | H2O | H3O+ | NH3 |
| 5) idrolisi dell’acetato di sodio CH3COO- Na+ | H2O | CH3COO- | CH3COOH | OH- |
| 6) neutralizzazione di HCl con NaOH | HCl | OH- | H2O | Cl- |
| 7) neutralizzazione di NH3 mediante acido acetico | CH3COOH | NH3 | NH4+ | CH3COO- |
| 8) dissoluzione di BiOCl (ossicloruro di bismuto) mediante HCl | 2 H3O+ | BiOCl | Bi(H2O)3+ | H2O, Cl- |
| 9) decomposizione di Ag(NH3)2+ da HNO3 | 2 H3O+ | Ag(NH3)2+ | NH4+ | H2O |
| 10) spostamento di HCN da CH3COOH | CH3COOH | CN- | HCN | CH3COO- |
Gli acidi forti hanno basi coniugate deboli
Questa è solo una ridichiarazione di ciò che è implicito in ciò che è stato detto sopra sulla distinzione tra acidi forti e acidi deboli. Il fatto che HCl sia un acido forte implica che la sua base coniugata Cl- è una base troppo debole per trattenere il protone in competizione con H2O o H3O+. Allo stesso modo, lo ione CN- si lega fortemente a un protone, rendendo l’HCN un acido debole.
I sali di acidi deboli si dissolvono per dare soluzioni alcaline
Il fatto che l’HCN sia un acido debole implica che lo ione cianuro CN- reagisce facilmente con i protoni, ed è quindi una base relativamente buona. Come prova di questo, un sale come il KCN, quando disciolto in acqua, produce una soluzione leggermente alcalina:
CN- + H2O → HCN + OH-
Questa reazione è ancora talvolta indicata con il suo vecchio nome idrolisi (“scissione dell’acqua”), che è letteralmente corretto ma tende ad oscurare la sua identità come un’altra reazione acido-base. Reazioni di questo tipo avvengono solo in piccola misura; una soluzione 0,1M di KCN è ancora, per tutti gli scopi pratici, 0,1M in ione cianuro.
Le uniche basi forti comuni sono gli idrossidi del gruppo 1
Le uniche basi veramente forti che è probabile incontrare nella chimica quotidiana sono gli idrossidi dei metalli alcalini come NaOH e KOH, che sono essenzialmente soluzioni dello ione idrossido (e, naturalmente, del catione.)
La maggior parte degli altri composti contenenti ioni idrossido come Fe(OH)3 e Ca(OH)2 non sono sufficientemente solubili in acqua per dare soluzioni altamente alcaline, quindi non sono solitamente considerati come basi forti.
Ci sono in realtà un certo numero di basi che sono più forti dello ione idrossido – i più noti sono lo ione ossido O2- e lo ione ammide NH2-, ma questi sono così forti che possono anche rubare all’acqua un protone:
O2- + H2O → 2 OH-
NH2- + H2O → NH3 + OH-
Questo dà luogo allo stesso tipo di effetto di livellamento che abbiamo descritto per gli acidi, con la conseguenza che
I sali di basi deboli producono soluzioni acide
L’esempio più comune è il cloruro di ammonio, NH4Cl, le cui soluzioni acquose sono decisamente acide:
NH4+ + H2O → NH3 + H3O+
Perché questa (e simili) reazioni avvengono solo in piccola misura, una soluzione di cloruro di ammonio sarà solo leggermente acida.
Autoprotolisi
Da alcuni degli esempi dati sopra, vediamo che l’acqua può agire come un acido
CN- + H2O → HCN + OH-
e come una base
NH4+ + H2O → NH3 + H3O+
Se è così, allora non c’è ragione per cui “l’acqua-acido” non possa donare un protone all'”acqua-base”:

Questa reazione è nota come autoprotolisi dell’acqua.
I chimici si riferiscono ancora spesso a questa reazione come “dissociazione” dell’acqua e usano l’equazione in stile Arrhenius H2O → H+ + OH- come una sorta di stenografia.
Come discusso nella lezione precedente, questo processo avviene solo in minima parte. Significa, tuttavia, che sia lo ione idronio che lo ione idrossido sono presenti in qualsiasi soluzione acquosa.
Altri liquidi possono mostrare autoprotolisi? La risposta è sì. L’esempio più noto è l’ammoniaca liquida:
2 NH3 → NH4+ + NH2-
Anche l’acido solforico liquido puro può giocare la partita:
2 H2SO4→ H3SO4+ + HSO4-
Ognuno di questi solventi può essere la base del proprio “sistema” acido-base, parallelo al familiare “sistema acqua”.
Ampoliti
L’acqua, che può agire sia come acido che come base, è detta anfiprotica: può “oscillare in entrambi i sensi”. Una sostanza come l’acqua che è anfiprotica è chiamata anfolitica.
Come indicato qui, lo ione idrossido può anche essere un anfolitico, ma non in soluzione acquosa in cui lo ione ossido non può esistere.
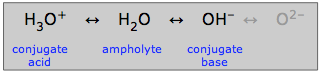
È naturalmente la natura anfiprotica dell’acqua che le permette di svolgere il suo ruolo speciale nella chimica acquatica ordinaria acido-base. Ma molte altre sostanze anfiprotiche possono esistere in soluti acquosi. Ogni sostanza di questo tipo avrà sempre un acido coniugato e una base coniugata, quindi se potete riconoscere questi due coniugati di una sostanza, saprete che è anfiprotica.
Il sistema acido-base carbonato
Per esempio, l’insieme delle triplette {acido carbonico, ione bicarbonato, ione carbonato} costituisce una serie anfiprotica in cui lo ione bicarbonato è l’anfolita, che differisce da uno dei suoi vicini per l’aggiunta o la rimozione di un protone:
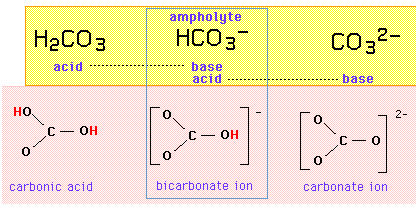
Se lo ione bicarbonato è sia un acido che una base, dovrebbe essere in grado di scambiare un protone con se stesso in una reazione di autoprotolisi:
HCO3- + HCO3- → H2CO3 + CO32-
La tua stessa vita dipende dalla reazione di cui sopra! La CO2, un sottoprodotto metabolico di ogni cellula del tuo corpo, reagisce con l’acqua per formare acido carbonico
H2CO3 che, se si accumulasse, renderebbe il tuo sangue fatalmente acido. Tuttavia, il sangue contiene anche ione carbonato, che reagisce secondo l’inverso dell’equazione di cui sopra per produrre bicarbonato che può essere tranquillamente trasportato dal sangue ai polmoni. Nei polmoni, la reazione di autoprotolisi va in avanti, producendo H2CO3 che perde acqua per formare CO2 che viene espulsa nel respiro. Lo ione carbonato viene riciclato di nuovo nel sangue per raccogliere un’altra molecola di CO2.