Nome generico: sodio polistirene sulfonato
Forma di dosaggio: sospensione orale/rettale
Rivista medica da Drugs.com. Ultimo aggiornamento il 22 luglio 2020.
- Panoramica
- Effetti collaterali
- Dosaggio
- Professionale
- Interazioni
- Più
- Indicazioni e uso per Kionex
- Kionex Dosaggio e amministrazione
- Informazioni generali
- Dosaggio consigliato
- Preparazione e amministrazione
- Forme di dosaggio e forze
- Contraindicazioni
- Avvertenze e precauzioni
- Necrosi intestinale
- Disturbi degli elettroliti
- Sovraccarico di fluido in pazienti sensibili all’assunzione di alto sodio
- Rischio di aspirazione
- Binding to Other Orally Administered Medications
- Reazioni avverse
- Interazioni farmacologiche
- Interazioni generali
- Attacidi che donano cationi
- Sorbitolo
- USO IN POPOLAZIONI SPECIFICHE
- Gravidanza
- Allattamento
- Uso pediatrico
- Sovradosaggio
- Kionex Descrizione
- Kionex – Farmacologia clinica
- Meccanismo di azione
- Farmacodinamica
- Farmacocinetica
- Tossicologia non clinica
- Carcinogenesi, mutagenesi, compromissione della fertilità
- Come viene fornito/conservazione e manipolazione
- Informazioni per il paziente
- PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
- Più informazioni su Kionex (sodio polistirene sulfonato)
- Risorse per i consumatori
- Risorse professionali
- Guide al trattamento correlate
Indicazioni e uso per Kionex
Kionexis indicato per il trattamento di iperkalemia.
Limitazione d’uso:
Kionex non deve essere usato come un trattamento di emergenza per iperkalemia pericolosa per la vita a causa della sua insorgenza ritardata di azione.
Kionex Dosaggio e amministrazione
Informazioni generali
Amministrare Kionex almeno 3 ore prima o 3 ore dopo altri farmaci per via orale. I pazienti con gastroparesi possono richiedere una separazione di 6 ore
Dosaggio consigliato
L’intensità e la durata della terapia dipendono dalla gravità e dalla resistenza dell’iperkalemia.
Orale
La dose media giornaliera totale per adulti di Kionex è di 15 g a 60 g, somministrata come una dose di 15 g (quattro cucchiaini rasi), una a quattro volte al giorno.
Rettale
La dose media per adulti è di 30 g a 50 g ogni sei ore.
Preparazione e amministrazione
Preparare la sospensione fresca e usare entro 24 ore.
Non riscaldare Kionex perché potrebbe alterare le proprietà di scambio della resina.
Un cucchiaino raso contiene circa 3,5 g di Kionex e 15 mEq di sodio.
Sospensione orale
Sospendere ogni dose in una piccola quantità di acqua o sciroppo, circa 3 a 4 mL di liquido per grammo di resina. Somministrare con il paziente in posizione eretta.
Enema
Dopo un clistere di pulizia iniziale, inserire un tubo di gomma morbido e di grandi dimensioni (French 28) nel retto per una distanza di circa 20 cm, con la punta ben dentro il colon sigmoide, e nastro adesivo in posizione.
Amministrare come emulsione calda (temperatura corporea) in 100 mL di veicolo acquoso e lavare con 50 a 100 ml di liquido. Una sospensione un po’ più spessa può essere usata, ma non formare una pasta.
Agitare delicatamente l’emulsione durante la somministrazione. La resina dovrebbe essere trattenuta il più a lungo possibile e seguita da un clistere di pulizia con una soluzione non contenente sodio. Assicurarsi che un volume adeguato di soluzione detergente (fino a 2 litri) sia utilizzato.
Forme di dosaggio e forze
Kionex è una polvere da crema a marrone chiaro, finemente macinata ed è disponibile in barattoli da 454 g.
Contraindicazioni
Kionex è controindicato nei pazienti con le seguenti condizioni:
– Ipersensibilità alle resine di polistirene sulfonato – Malattia intestinale ostruttiva – Neonati con ridotta motilità intestinale
Avvertenze e precauzioni
Necrosi intestinale
Casi di necrosi intestinale, alcuni fatali, e altri gravi eventi avversi gastrointestinali (sanguinamento, colite ischemica, perforazione) sono stati riportati in associazione all’uso di Kionex. La maggior parte di questi casi ha riportato l’uso concomitante di sorbitolo. I fattori di rischio per gli eventi avversi gastrointestinali erano presenti in molti dei casi, tra cui la prematurità, la storia di malattia intestinale o di chirurgia, l’ipovolemia e l’insufficienza e l’insufficienza renale. La somministrazione concomitante di sorbitolo non è raccomandata.
– Utilizzare solo in pazienti che hanno una normale funzione intestinale. Evitare l’uso in pazienti che non hanno avuto un movimento intestinale post-intervento. – Evitare l’uso in pazienti che sono a rischio di sviluppare costipazione o impattazione (compresi quelli con storia di impattazione, costipazione cronica, malattia infiammatoria intestinale, colite ischemica, aterosclerosi intestinale vascolare, precedente resezione intestinale o ostruzione intestinale). Interrompere l’uso in pazienti che sviluppano costipazione.
Disturbi degli elettroliti
Monitorare il potassio sierico durante la terapia perché può verificarsi grave ipokaliemia.
Kionex non è totalmente selettivo per il potassio, e piccole quantità di altri cationi come magnesio e calcio possono anche essere perse durante il trattamento. Monitorare il calcio e il magnesio nei pazienti che ricevono Kionex.
Sovraccarico di fluido in pazienti sensibili all’assunzione di alto sodio
Ogni dose di 15 g di Kionex contiene 1500 mg (60 mEq) di sodio. Monitorare i pazienti che sono sensibili all’assunzione di sodio (insufficienza cardiaca, ipertensione, edema) per i segni di sovraccarico di liquidi. Regolazione di altre fonti di sodio può essere richiesto.
Rischio di aspirazione
Casi di bronchite acuta o broncopolmonite causata da inalazione di particelle di sodio polistirene solfonato sono stati riportati. I pazienti con riflesso del vomito compromesso, livello di coscienza alterato o pazienti inclini al rigurgito possono essere a rischio aumentato. Somministrare Kionex con il paziente in posizione verticale.
Binding to Other Orally Administered Medications
Kionex può legare farmaci somministrati per via orale, che potrebbero diminuire il loro assorbimento gastrointestinale e portare ad una ridotta efficacia. Somministrare altri farmaci per via orale almeno 3 ore prima o 3 ore dopo Kionex. I pazienti con gastroparesi possono richiedere una separazione di 6 ore.
Reazioni avverse
Le seguenti reazioni avverse sono discusse altrove nell’etichettatura:
– Necrosi intestinale – Disturbi elettrolitici – Aspirazione
Le seguenti reazioni avverse sono state identificate durante l’uso post-approvazione di Kionex. Poiché queste reazioni sono segnalate volontariamente da una popolazione di dimensioni incerte, non è sempre possibile stimare la loro frequenza in modo affidabile o stabilire una relazione causale all’esposizione al farmaco.
Gastrointestinale: anoressia, costipazione, diarrea, impattazione fecale, concrezioni gastrointestinali (bezoari), colite ischemica, nausea, ulcerazioni, vomito, irritazione gastrica, ostruzione intestinale (dovuta alla concentrazione di idrossido di alluminio)
Metabolico: alcalosi sistemica
Interazioni farmacologiche
Interazioni generali
Nessuno studio formale di interazione farmacologica è stato condotto nell’uomo.
Kionex ha il potenziale di legare altri farmaci. In studi di legame in vitro, Kionex ha dimostrato di legare significativamente i farmaci orali (n=6) che sono stati testati. Una diminuzione dell’assorbimento di litio e tiroxina è stata riportata anche con la co-somministrazione di Kionex. Il legame di Kionex ad altri farmaci orali potrebbe causare un minore assorbimento gastrointestinale e la perdita di efficacia quando viene assunto vicino al momento della somministrazione di Kionex. Somministrare Kionex almeno 3 ore prima o 3 ore dopo altri farmaci orali. I pazienti con gastroparesi possono richiedere una separazione di 6 ore. Monitorare la risposta clinica e/o i livelli ematici dove possibile.
Attacidi che donano cationi
La somministrazione orale simultanea di Kionex con antiacidi che donano cationi non assorbibili e lassativi può ridurre la capacità di scambio di potassio della resina e aumentare il rischio di alcalosi sistemica.
Sorbitolo
Il sorbitolo può contribuire al rischio di necrosi intestinale e l’uso concomitante non è raccomandato.
USO IN POPOLAZIONI SPECIFICHE
Gravidanza
Riassunto del rischio
Kionex non è assorbito sistemicamente dopo somministrazione orale o rettale e non si prevede che l’uso materno comporti un rischio fetale.
Allattamento
Riepilogo del rischio
Kionex non viene assorbito sistematicamente dalla madre, quindi non ci si aspetta che l’allattamento al seno comporti rischi per il bambino.
Uso pediatrico
Studi di sicurezza ed efficacia non sono stati effettuati in pazienti pediatrici.
Nei pazienti pediatrici, come negli adulti, ci si aspetta che Kionex leghi il potassio al rapporto di scambio pratico di 1mEq di potassio per 1 grammo di resina.
Nei neonati, Kionex non deve essere dato per via orale. Sia nei bambini che nei neonati, un dosaggio eccessivo o una diluizione inadeguata potrebbero causare l’impattazione della resina. I neonati prematuri o i neonati di basso peso alla nascita possono avere un aumentato rischio di effetti avversi gastrointestinali con Kionex. uso .
Sovradosaggio
Il sovradosaggio può provocare disturbi elettrolitici tra cui ipokalemia, ipocalcemia e ipomagnesemia. Misure appropriate devono essere prese per correggere gli elettroliti del siero (potassio, calcio, magnesio), e la resina deve essere rimossa dal tratto alimentare con l’uso appropriato di lassativi o clisteri.
Kionex Descrizione
Kionex è un benzene, dietenil-polimero, con etenilbenzene, solfonato, sale di sodio e ha la seguente formula strutturale:
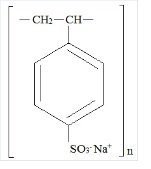
Il farmaco è una crema a marrone chiaro finemente macinato, forma in polvere di sodio polistirene solfonato, una resina di scambio cationico preparato in fase sodica con una capacità di scambio in vitro di circa 3.1 mEq (in vivo circa 1 mEq) di potassio per grammo. Il contenuto di sodio è di circa 100 mg (4,1 mEq) per grammo di farmaco. Può essere somministrato per via orale o rettale come clistere.
Un grammo di Kionex contiene 4,1 mEq di sodio.
Kionex – Farmacologia clinica
Meccanismo di azione
Kionex è un polimero a scambio cationico non assorbito che contiene un controione di sodio.
Kionex aumenta l’escrezione fecale di potassio attraverso il legame di potassio nel lume del tratto gastrointestinale. Il legame di potassio riduce la concentrazione di potassio libero nel lume gastrointestinale, con conseguente riduzione dei livelli di potassio nel siero. Il rapporto di scambio pratico è di 1 mEq K per 1 grammo di resina.
Quando la resina passa lungo l’intestino o viene trattenuta nel colon dopo la somministrazione per clistere, gli ioni di sodio vengono parzialmente rilasciati e vengono sostituiti da ioni di potassio. Questa azione avviene principalmente nell’intestino crasso, che espelle ioni di potassio in misura maggiore rispetto all’intestino tenue. L’efficienza di questo processo è limitata e imprevedibilmente variabile.
Farmacodinamica
L’effettivo abbassamento del potassio sierico con Kionex può richiedere da ore a giorni.
Farmacocinetica
L’efficienza in vivo delle resine di scambio sodio-potassio è circa il 33%; quindi, circa un terzo del contenuto effettivo di sodio della resina viene consegnato al corpo.
Kionex non viene assorbito sistematicamente.
Interazioni farmacologiche
Studi di legame in vitro hanno mostrato che Kionex si è legato significativamente ai seguenti farmaci testati – warfarin, metoprolol, fenitoina, furosemide, amlodipina e amoxicillina.
Tossicologia non clinica
Carcinogenesi, mutagenesi, compromissione della fertilità
Studi non sono stati effettuati.
Come viene fornito/conservazione e manipolazione
Kionex è disponibile come crema a marrone chiaro, polvere finemente macinata in barattoli da 1 libbra (454 g), NDC 0574-2004-16.
conservare a 20° a 25°C (68° a 77°F).
Informazioni per il paziente
Interazioni farmacologiche
Avvisare i pazienti che stanno assumendo altri farmaci orali di separare il dosaggio di Kionex di almeno 3 ore (prima o dopo)
Solo Rx
Confezionato da
Perrigo
Minneapolis, MN 55427
Revisionato 08/2017
PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
Rx Only
NDC 0574-2004-16
Kionex®
Sodium Polystyrene Sulfonate for Suspension
Dose media per adulti: 15 g (circa 4 cucchiaini rasi) da una a quattro volte al giorno in acqua. Vedere le informazioni complete sulla prescrizione.
L’effetto deve essere attentamente controllato da frequenti determinazioni del potassio sierico entro ogni periodo di 24 ore. Contenuto di sodio circa 60 mEq per 15 g.
La sospensione deve essere preparata di fresco e non conservata oltre le 24 ore. Dispensare in contenitori stretti e resistenti alla luce come definito nella USP.
CONSERVAZIONE: Conservare a 20° a 25°C (68° a 77°F).
Leggere il foglietto illustrativo.
454 grammi (1 LB)
| Kionex polistirene sulfonato di sodio in polvere, per sospensione |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Editore – Paddock Laboratories, LLC (967694121)
Più informazioni su Kionex (sodio polistirene sulfonato)
- Effetti collaterali
- Durante la gravidanza o l’allattamento
- Informazioni sul dosaggio
- Interazioni farmacologiche
- En Español
- 4 recensioni
- Classe del farmaco: resine a scambio cationico
- FDA Alerts (2)
Risorse per i consumatori
- Informazioni per i pazienti
- Kionex (lettura avanzata)
Risorse professionali
- Informazioni per il paziente
- Sodio polistirene sulfonato polvere orale (FDA)
Altre marche Kayexalate, Kalexate
Guide al trattamento correlate
- Iperkalemia
Discorso medico