
Brønsted in his laboratory
Brønsted-Lowry Conceptによれば、従来は一般酸HAの単純解離(HA → H+ + A-)として書かれていたが、プロトン移動過程と考える方が正確であると言うこと。
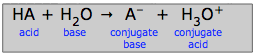
HA + H2O → A-+ H3O+(3-1)
この考え方は、プロトンが酸から離れたら、何か(私たちが塩基と呼ぶもの)に結合しなければならず、単に無料の水素イオンとして浮かんでいることはできない、ということである。
共役酸塩基対
酸と塩基の反応は、したがってプロトン交換反応である。 酸をAH、塩基をBとすると、一般的な酸塩基反応は
AH + B → A- + BH+(3-2)
この反応の逆、
BH+ + A- → B + AH(3-3)
もまた酸塩基反応であることに注意されたい。 プロトン移動反応は可逆的なので、酸から塩基へのプロトン移動は、少なくとも原理的には、それ自身の酸塩基対を構成できる新しい種の対を必ず生成しなければならず、これを共役酸塩基対と呼ぶ。
共役という言葉は「とつながっている」という意味で、どの共役対のメンバーも、プロトン1個の存在または不在によって「つながって」いるという意味である。
どの種が「共役」とみなされるかは、(3-1)のプロトン移動について以下に示すように、反応を書く方向に依存する:


同様に、一般化したプロトン移動 (3-2) と (3-3) について、


次の表は多くの典型的な酸塩基系での共役ペアを示したものだ。
| 酸 | 塩基 | |||
| 塩酸 | HCl | 塩化物イオン | Cl- | 塩化物イオン |
| 酢酸 | CH3CH2COOH | 酢酸イオン | CH3CH2COO- | |
| 硝酸 | HNO3(ニッケル酸 | 硝酸イオン | NO3- | |
| リン酸二水素イオン | H2PO4- | 一水素リン酸イオン HPO42- | ||
| 硫酸水素イオン | HSO4- | 硫酸イオン | SO42- | |
| 硫酸水素イオン 炭酸イオン | HCO3- | CO32- | ||
| アンモニウムイオン | NH4+ | NH3 | ||
| 鉄(III)(「鉄」)イオン | Fe(H2O)63+ | ペンタアコIII | PentaaquoironIII FE(H2O)5OH2+ | |
| 水 | H2O | OH- | ||
| ヒドロニウムイオン | H3O+ | H2O | ||
強酸と弱酸
一般化した酸-弱酸を見ることが出来る。塩基反応
は2つの塩基がプロトンを奪い合うことである。

Definition of a “strong” acid
この綱引きに圧倒的に塩基H2Oが勝つと、酸HAは強酸と言われます。 これは塩酸や他の一般的な強い「鉱酸」H2SO4、HNO3、HClO4で起こることです。
これらの酸の水中での溶液は、実際には右の太字で示されたイオン種の溶液となるのです。 この場合、たとえば「塩酸」の 1 M 水溶液と呼ばれるものは、実際にはかなりの濃度の HCl をまったく含んでいないことになり、そのような溶液に存在する唯一の真の酸は H3O+ です!
H3O+ は水中に存在しうる最強の酸である。
すべての強酸は水中で等しく強いと考えられる。
The leveling effect
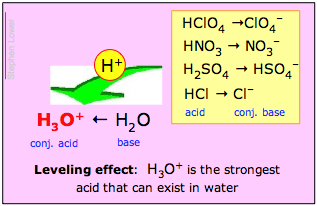
このうち2番目の記述をLeveling effectと呼びます。 強酸の固有のプロトン供与強度は異なるが、いずれも水中で完全に解離することを意味する。 化学者は、溶媒である水によって強度が「平準化」されると言います。
同様の効果は、幼い子供と一連の綱引き競争を行うことによって、数人の大人の強度を判断しようとした場合にも見られます。 大人たちの強さは子供の強さによって「平準化」されているため、各試行で大人が圧倒的に勝つと予想される。
弱い酸
しかし、ほとんどの酸はプロトンをより強く保持することができるので、酸のごく一部が解離するだけである。 たとえば青酸 HCN は水中では弱酸ですが、これはプロトンがシアン化物イオン CN- の孤立電子を H2O のそれよりも効果的に共有できるため、
HCN + H2O → H3O+ + CN-
という反応が非常にわずかしか進行しないためです。
強酸はプロトンを弱く結合し、弱酸は強く結合するので、
強酸は「弱い」、弱酸は「強い」
このパラドックスを説明できれば、酸塩基化学で最も重要な考えの1つを理解したことになります!
|
反応
|
酸
|
塩基
|
共役酸
|
共役塩基
|
||
| 1) 水の自己イオン化 H2O | H2O | H3O+ | OH- | |||
| 2) 青酸HCNのイオン化 | HCN | H2O | H3O+ | CN- | ||
| 3) 水中のアンモニアNH3のイオン化 | NH3 | H2O | NH4+ | OH- | H2O | NH4 |
| 4) 塩化アンモニウムの加水分解 NH4Cl | NH4+ | H2O | H3O+ | NH3 | ||
| 5) 酢酸ソーダの加水分解 CH3COO-… Na+ | H2O | CH3COO- | CH3COOH | OH- | ||
| 6) 中和作用 NaOHによるHClの中和 | HCl | OH- | H2O | Cl- | ||
| 7)中和 酢酸によるNH3 | CH3COOH | NH3 | NH4+ | CH3COO- | ||
| 8)。 BiOCl(オキシ塩化ビスマス)のHClによる溶解 | 2 H3O+ | BiOCl | H2O.HCl | Bi(H2O)2+ | Bi(H2O)3+ | H2O, Cl- |
| 9) HNO3 による Ag(NH3)2+ の分解 | 2 H3O+ | Ag(NH3)2+ | NH4+ | H2O | ||
| 10) HCN による変圧器 | CH3COOH | CN- | HCN | CH3COO- |
Strong acids have weak conjugate bases
this is just a re-jp…強酸と弱酸の区別について、これまで述べてきたことが暗黙の了解となっている。 HClが強酸であるということは、その共役塩基であるCl-はH2OやH3O+と競合してプロトンを保持するには弱すぎる塩基であることを意味する。 同様に、CN-イオンはプロトンと強く結合し、HCNは弱酸となる。
弱酸の塩は溶解してアルカリ溶液を与える
HCNが弱酸であるという事実は、シアン化物イオンCN-がプロトンと容易に反応し、したがって、比較的良いベースであることを示唆している。
CN- + H2O → HCN + OH-
この反応は今でも古い名前で呼ばれることがあるが、これは文字通り正しいが、単なる酸塩基反応であることが不明瞭になる傾向がある。 この種の反応はごくわずかしか起こらず、0.1MのKCN溶液は、実用上はまだ、シアン化物イオンで0.1Mである。
唯一の一般的な強塩基は1族の水酸化物
日々の化学で本当に強い塩基に出会う可能性があるのはNaOHやKOHといったアルカリ金属水酸化物で、これは本質的に水酸化物イオン(そしてもちろん陽イオンも)の溶液であり、この水酸化物もまた、アルカリの水溶液です。)
Fe(OH)3 や Ca(OH)2 などの水酸化物イオンを含む他のほとんどの化合物は、高アルカリ性溶液を与えるほど水に溶けないので、通常は強塩基とはみなされない。
実は水酸化物イオンより強い塩基はいくつかあり、酸化物イオンO2-やアミドイオンNH2-がよく知られているが、これらはプロトンさえ奪うことができるほど強力である。
O2- + H2O → 2 OH-
NH2- + H2O → NH3 + OH-
これは酸について述べたのと同じ種類の平衡効果をもたらし、結果として
弱塩基の塩は酸性溶液を生成する
この最も一般的な例は塩化アンモニウム、NH4Clで、その水溶液は明らかに酸性である:
NH4+ + H2O → NH3 + H3O+
この(および同様の)反応はほんの少ししか起こらないので、塩化アンモニウム溶液はわずかに酸性になるだけである。
Autoprotolysis
上に挙げたいくつかの例から。 6390>
CN- + H2O → HCN + OH-
NH4+ + H2O → NH3 + H3O+
もしそうなら、「酸である水」が「塩基である水」にプロトンを提供できないわけがないだろう。

この反応は水の自己水素化反応として知られています。
化学者は今でもこの反応を水の「解離」と呼ぶことが多く、一種の省略形としてアレニウス式の H2O → H+ + OH- という方程式を使用します。
前回の授業で説明したように、この過程はごくわずかしか起こりません。
他の液体も自己分解を起こすのですか。 答えはイエスである。 最もよく知られた例は液体アンモニアです:
2 NH3 → NH4+ + NH2-
純粋な液体硫酸でさえゲームをすることができます:
2 H2SO4→ H3SO4+ + HSO4-
これらの溶剤はそれぞれ、おなじみの「水のシステム」と平行して独自の酸-塩基「システム」の基盤となる可能性を持っています。
両性イオン
酸にも塩基にもなる水は両性イオンと呼ばれ、「どちらにも振れる」ことができる。
ここで示したように、水酸化物イオンも両性イオンとなり得るが、酸化物イオンが存在できない水溶液では両性イオンにならない。
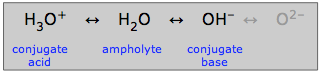
通常の水生酸塩基化学で特別な役割を果たすことができるのは、もちろん水の両性イオン的な性質によるものです。 しかし、他の多くの両親媒性物質も水性溶媒中に存在することができます。 このような物質には必ず共役の酸と共役の塩基があるので、この2つの共役を認識できれば、その物質が両親媒性であることが分かります。
炭酸酸塩基系
例えば、三重項集合{炭酸、重炭酸イオン、炭酸イオン}は、重炭酸イオンが両性体で、プロトン1個の付加または除去によって隣の物質のいずれとも異なる両性体の系列を構成している。
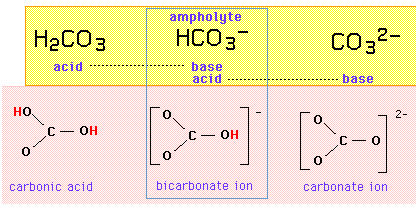
炭酸水素イオンが酸であり塩基でもある場合、自己分解反応によってプロトンを交換できるはずです:
HCO3- + HCO3- → H2CO3 + CO32-
あなたの生命活動は上記の反応にかかっているのですよ! 体内のあらゆる細胞の代謝副産物であるCO2は、水と反応して炭酸
H2CO3を形成し、これが蓄積されると血液を致命的な酸性にします。 しかし、血液中には炭酸イオンも含まれており、このイオンは上記の式の逆に従って反応し、重炭酸塩を生成するため、血液によって安全に肺に運ばれることができる。 肺では、自己分解反応が順方向に進み、H2CO3が生成され、水を失ってCO2となり、呼吸とともに排出される。 炭酸イオンは血液にリサイクルされ、最終的に別のCO2分子を拾います。