一般名:ポリスチレンスルホン酸ナトリウム
剤形:経口/直腸懸濁液
Drugs.com による医学的レビューです。 最終更新日:2020年7月22日
- 概要
- 副作用
- 用法用量
- その他
- キオネックスの効能・効果
- キオネックスの用法・用量
- 一般情報
- 推奨用量
- 調製・投与方法
- 剤形および強度
- 禁忌
- 警告と注意
- 腸管壊死
- 電解質異常
- 高ナトリウム摂取に敏感な患者における体液過剰
- 誤嚥のリスク
- 他の経口投与薬との結合
- 副作用
- 薬物相互作用
- 一般的な相互作用
- 陽イオン供与性制酸剤
- Sorbitol
- USE IN SPECIFIC POPULATIONS
- Pregnancy
- 授乳
- 過量投与
- キオネックスの概要
- Kionex – Clinical Pharmacology
- Mechanism of Action
- 薬力学
- 薬物動態
- 非臨床毒性
- 発がん性、変異原性、生殖能力障害
- How Supplied/Storage and Handling
- 患者相談情報
- PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
- キオネックス(ポリスチレンスルホン酸ナトリウム)の詳細
- Consumer resources
- 専門家向けリソース
- 関連治療ガイド
キオネックスの効能・効果
キオネックスの適応は「高カリウム血症の治療」になります。
使用上の制限:
キオネックスは作用発現が遅いため、生命を脅かす高カリウム血症の緊急治療には使用しない。
キオネックスの用法・用量
一般情報
他の内服薬の少なくとも3時間前または3時間後に投与すること。 胃不全麻痺の患者では、6時間の間隔が必要な場合がある。
推奨用量
治療の強度と期間は、高カリウム血症の重症度と耐性に依存する。
経口剤
成人1日平均総量として15g~60gを1日1~4回、15g(ティースプーン4杯)を投与し、
経口剤
成人平均総量として30g~50gを6時間おきに投与する。
調製・投与方法
懸濁液は新鮮なうちに調製し、24時間以内に使用する。
樹脂の交換特性を変えることがあるので、キオネックスを加熱しないこと。
ティースプーン1杯には、約3.5gのKionexと15mEqのナトリウムが含まれています。
口腔懸濁液
各用量を少量の水またはシロップ、樹脂1グラムあたり約3~4mLの液体に懸濁させます。
浣腸
最初の洗浄浣腸の後、柔らかい大型(仏式28号)のゴム管を直腸に約20cm挿入し、先端をS状結腸によく差し込み、テープ止めする。
100mLの水溶液に温かい(体温)乳液として投与し、50~100mLの液体で洗浄する。 9908><9261>投与中は乳剤を静かに攪拌する。 樹脂はできるだけ長く保持し、その後、非ナトリウム含有溶液で洗浄浣腸する必要がある。
剤形および強度
キオネックスはクリーム色から淡褐色の微粉末で、454gの瓶で提供されています。
禁忌
キオネックスは、以下の症状のある患者には禁忌である。
-ポリスチレンスルホン酸樹脂に対する過敏症 -閉塞性腸疾患 -腸管運動が低下している新生児
警告と注意
腸管壊死
Kionexの使用に関連して、腸管壊死 (一部は致命的) およびその他の重大な消化管有害事象 (出血、虚血性腸炎、穿孔) の例が報告されています。 これらの症例の多くは、ソルビトールの併用が報告されています。 消化器系有害事象の危険因子は、未熟児、腸管疾患・手術歴、血液量低下、腎不全・腎障害など、多くの症例に認められました。 ソルビトールの併用投与は推奨されない<9908> ・腸の機能が正常な患者のみに使用すること。 術後に排便のない患者への使用は避けること。 – 便秘やインパクションを起こすリスクのある患者(インパクションの既往、慢性便秘、炎症性腸疾患、虚血性大腸炎、血管性腸管動脈硬化症、腸切除歴、腸閉塞を含む)には使用を控える。 便秘を発症した患者には使用を中止してください。
電解質異常
重度の低カリウム血症が起こることがあるので、治療中は血清カリウムを監視すること。
キオネックスはカリウムに完全に選択的ではなく、治療中にマグネシウムやカルシウムなどの他のカチオンを少量喪失することもある。
高ナトリウム摂取に敏感な患者における体液過剰
キオネックスの各15g用量は、1500mg(60mEq)のナトリウムを含んでいる。 ナトリウム摂取に過敏な患者(心不全、高血圧、浮腫)の体液過剰の徴候を監視する。
誤嚥のリスク
ポリスチレンスルホン酸ナトリウム粒子の吸入による急性気管支炎または気管支肺炎の症例が報告されている。 嚥下反射が低下している患者、意識レベルが変化している患者、または逆流しやすい患者はリスクが高まる可能性があります。
他の経口投与薬との結合
キオネックスは経口投与薬と結合することがあり、消化管吸収を低下させ、有効性を低下させる可能性がある。 他の経口薬は、Kionexの少なくとも3時間前または3時間後に投与してください。 胃不全麻痺の患者は、6時間の間隔が必要な場合があります。 .
副作用
以下の副作用については、添付文書の他の箇所で説明しています。
– 腸管壊死 – 電解質異常 – 吸引
承認後のKionexの使用において、以下の副作用が確認されています。 これらの副作用は、規模が不明確な集団から自発的に報告されたものであるため、その頻度を確実に推定することや薬剤曝露との因果関係を確立することは必ずしも可能ではありません。
消化器:食欲不振、便秘、下痢、便閉、消化管コンクレット(ベゾアール)、虚血性大腸炎、悪心、潰瘍、嘔吐、胃刺激、腸閉塞(水酸化アルミニウムの濃度による)
代謝性:消化器:便秘、便閉、便閉(水酸化アルミニウム)、胃刺激、腸閉(水酸化アルミニウムの濃度による)代謝性(血糖値)
代謝性(水酸化アルミニウム)
薬物相互作用
一般的な相互作用
ヒトでの正式な薬物相互作用試験は実施されていない。
キオネックスは他の薬物と結合する可能性があります。 in vitroの結合試験において、キオネックスは試験対象となった経口薬(n=6)と有意に結合することが示されました。 また、キオネックスの同時投与により、リチウムとサイロキシンの吸収が低下することが報告されています。 キオネックスと他の内服薬との結合により、キオネックス投与時期の近くで服用した場合、消化管吸収の低下や効能の消失が起こる可能性があります。 キオネックスは、他の経口薬の少なくとも3時間前または3時間後に投与してください。 胃不全麻痺の患者は、6時間の間隔が必要な場合がある。
陽イオン供与性制酸剤
非吸収性陽イオン供与性制酸剤および下剤とキオネックスを同時に経口投与すると、樹脂のカリウム交換能力が低下し、全身性アルカローシスのリスクが増加する可能性があります。
Sorbitol
ソルビトールは腸管壊死のリスクを高める可能性があり、併用は推奨されない。
USE IN SPECIFIC POPULATIONS
Pregnancy
リスク概要
Kionexは経口または直腸投与後に全身吸収されず、母親の使用により胎児リスクが生じるとは予測されない。
授乳
リスクの概要
キオネックスは母親から全身に吸収されないため、授乳による乳児へのリスクはないと考えられている。
小児患者においても、成人と同様に、キオネックスは樹脂1gあたり1mEqの実用的な交換比率でカリウムを結合すると考えられる。
新生児では、キオネックスを経口投与してはならない。 小児および新生児の両方において、過剰な投与または不十分な希釈は、樹脂のインパクションを引き起こす可能性がある。 未熟児や低出生体重児は、キオネックスによる消化器系の副作用のリスクが高まる可能性があります。
過量投与
過量投与により、低カリウム血症、低カルシウム血症、低マグネシウム血症を含む電解質異常が生じることがあります。 血清電解質(カリウム、カルシウム、マグネシウム)の補正を行い、下剤や浣腸を適切に用いて消化管から樹脂を除去するなどの適切な処置を行う必要があります。
キオネックスの概要
キオネックスは、ベンゼン、ジエテニルポリマー、エテニルベンゼン、スルホン化、ナトリウム塩で、次の構造式を持っています:
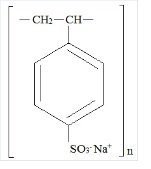
本剤は、ナトリウム相で調製したカチオン交換樹脂のクリーム~薄茶色の微粉末で、体外交換容量は約3.5mSvです。1gあたり1mEq(in vivoでは約1mEq)のカリウムを交換することができる。 ナトリウムは本剤1gあたり約100mg(4.1mEq)である。 経口投与または浣腸による直腸投与が可能です。
キオネックス1g中に4.1mEqのナトリウムを含みます。
Kionex – Clinical Pharmacology
Mechanism of Action
Kionex は非吸収型のカチオン交換ポリマーで、対イオンとしてナトリウムが含まれています。
キオネックスは、消化管内腔でカリウムと結合することにより、糞便中へのカリウム排泄を増加させる。 カリウムの結合により、消化管内腔の遊離カリウム濃度が低下し、その結果、血清カリウム濃度を低下させる。 実用的な交換比率は樹脂1gあたり1mEq Kです。
樹脂が腸を通過するとき、または浣腸による投与後に結腸に保持されるとき、ナトリウムイオンが一部放出されてカリウムイオンと置き換わります。 この作用は主に大腸で起こり、大腸は小腸よりもカリウムイオンを多く排泄する。
薬力学
キオネックスによる血清カリウムの効果的な低下には数時間から数日かかる場合があります。
薬物動態
ナトリウム-カリウム交換樹脂の生体内効率は約33%であり、樹脂の実際のナトリウム含有量の約1/3を体内に供給します。
キオネックスは全身に吸収されない。
薬物相互作用
試験管内結合試験では、キオネックスは次の試験薬物と有意に結合した。ワルファリン、メトプロロール、フェニトイン、フロセミド、アムロジピンおよびアモキシシリン。
非臨床毒性
発がん性、変異原性、生殖能力障害
試験は実施していない。
How Supplied/Storage and Handling
Kionexは、クリーム色から薄茶色の微粉末で、1ポンド(454g)の瓶に入っています(NDC 0574-2004-16.)
20°〜25°Cで保管してください。
患者相談情報
薬物相互作用
他の経口薬を服用している患者には、Kionexの投与を少なくとも3時間(前または後)に分けるように助言してください
Rx Only
パッケージ:
Perrigo
Minneapolis社(ミネアポリス)。 MN 55427
Revised 08/2017
PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
Rx Only
NDC 0574-2004-16
Kionex®
Sodium Polystyrene Sulfonate for Suspension
AVAGE大人用用量.NAVY
Rx専用
Rx専用 Rx専用 NAVY
Rx専用
AVAGE大人用用量.NAVY
この効果は、24時間以内に頻繁に血清カリウムを測定することにより、慎重にコントロールする必要があります。 ナトリウム含量は15gあたり約60mEqです。
懸濁液は新鮮なものを用意し、24時間を超えて保存しないようにしてください。 USPに規定されている密閉式耐光性容器に分注する。
保管。 20°~25°C (68°~77°F) で保存すること。
添付文書を読むこと。
454g (1 LB)
| Kionex sodium polystyrene sulfonate powder.を含む。 懸濁用 |
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
|
|||||||||||||||||
Labeler – (ラベル) パドックラボラトリーズ LLC (967694121)
キオネックス(ポリスチレンスルホン酸ナトリウム)の詳細
- 副作用
- 妊娠中または授乳中
- 用法用量
- 医薬品相互作用
- En Español
- 薬のクラス.Distribution(Drug class) 陽イオン交換樹脂
- FDA 警告 (2)
4 レビュー
Consumer resources
- 患者情報
- Kionex (Advanced Reading)
専門家向けリソース
- 処方情報
- Sodium Polystyrene Sulfonate Oral Powder (FDA)
他のブランド Kayexalate, カレキサート
関連治療ガイド
- 高カリウム血症
医学的免責事項