Chemische reacties van vetten en oliën
Vetten en oliën kunnen deelnemen aan een verscheidenheid van chemische reacties-bijvoorbeeld, omdat triglyceriden esters zijn, kunnen ze worden gehydrolyseerd in de aanwezigheid van een zuur, een base, of specifieke enzymen bekend als lipasen. De hydrolyse van vetten en oliën in aanwezigheid van een base wordt gebruikt om zeep te maken en wordt verzeping genoemd. Tegenwoordig wordt zeep meestal bereid door de hydrolyse van triglyceriden (vaak van talg, kokosolie, of beide) met water onder hoge druk en temperatuur. Natriumcarbonaat of natriumhydroxide wordt dan gebruikt om de vetzuren om te zetten in hun natriumzouten (zeepmoleculen):
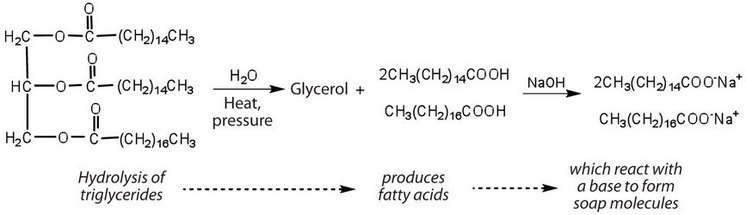
Nauwkeuriger kijken: Zeep
Ordinaire zeep is een mengsel van de natriumzouten van verschillende vetzuren, geproduceerd in een van de oudste organische syntheses die door de mens zijn beoefend (na de fermentatie van suikers om ethylalcohol te produceren). Zowel de Feniciërs (600 v. Chr.) als de Romeinen maakten zeep van dierlijk vet en houtas. Toch begon de productie van zeep pas in de jaren 1700 op grote schaal. Zeep werd traditioneel gemaakt door gesmolten reuzel of talg met een kleine overmaat alkali te behandelen in grote open vaten. Het mengsel werd verwarmd en er werd stoom door geblazen. Nadat de verzeping was voltooid, werd de zeep uit het mengsel geprecipiteerd door toevoeging van natriumchloride (NaCl), verwijderd door filtratie en verschillende malen met water gewassen. Vervolgens werd de zeep opgelost in water en opnieuw geprecipiteerd door toevoeging van meer NaCl. De bij de reactie geproduceerde glycerol werd ook teruggewonnen uit de waterige wasoplossingen.
Pumice of zand wordt toegevoegd om schuurzeep te produceren, terwijl ingrediënten zoals parfums of kleurstoffen worden toegevoegd om geurige, gekleurde zepen te produceren. Door lucht door gesmolten zeep te blazen ontstaat een drijvende zeep. Zachte zepen, gemaakt met kaliumzouten, zijn duurder maar geven een fijner schuim en zijn beter oplosbaar. Ze worden gebruikt in vloeibare zepen, shampoos en scheercrèmes.
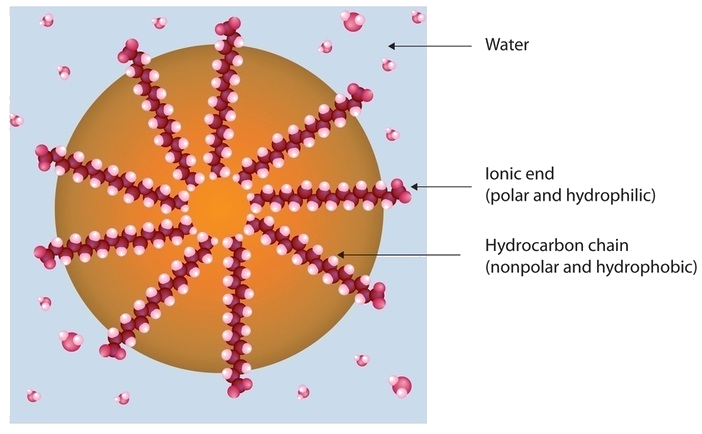
Vuil en vuil hechten zich meestal aan huid, kleding en andere oppervlakken door zich te vermengen met lichaamsoliën, bak- en braadvetten, smeervetten en soortgelijke stoffen die als lijm werken. Omdat deze stoffen niet mengbaar zijn in water, helpt wassen met water alleen weinig om ze te verwijderen. Zeep verwijdert ze echter wel, omdat zeepmoleculen een tweeledig karakter hebben. Het ene uiteinde, de kop genoemd, heeft een ionische lading (een carboxylaatanion) en lost daarom op in water; het andere uiteinde, de staart, heeft een koolwaterstofstructuur en lost op in oliën. De koolwaterstofstaarten lossen op in de bodem; de ionische koppen blijven in de waterige fase, en de zeep breekt de olie in kleine met zeep omhulde druppeltjes, micellen genaamd, die zich in de oplossing verspreiden. De druppeltjes stoten elkaar af vanwege hun geladen oppervlakken en smelten niet samen. Nu de olie het vuil niet langer aan het vervuilde oppervlak (huid, doek, schaal) “plakt”, kan het met zeep ingesloten vuil gemakkelijk worden weggespoeld.
De dubbele bindingen in vetten en oliën kunnen hydrogenatie en ook oxidatie ondergaan. De hydrogenering van plantaardige oliën tot halfvaste vetten is een belangrijk proces in de levensmiddelenindustrie. Chemisch gezien is het in wezen identiek aan de katalytische hydrogeneringsreactie die voor alkenen is beschreven.

In commerciële processen wordt het aantal dubbele bindingen dat wordt gehydrogeneerd zorgvuldig gecontroleerd om vetten met de gewenste consistentie (zacht en plooibaar) te produceren. Goedkope en overvloedige plantaardige oliën (canola, maïs, soja) worden zo omgezet in margarine en bak- en braadvetten. Bij de bereiding van margarine, bijvoorbeeld, worden gedeeltelijk gehydrogeneerde oliën gemengd met water, zout en vetvrije melk, samen met smaakstoffen, kleurstoffen, en vitamines A en D, die worden toegevoegd om het uiterlijk, de smaak en de voedingswaarde van boter te benaderen. (Er worden ook conserveringsmiddelen en antioxidanten toegevoegd.) In de meeste commerciële pindakaas is de pindaolie gedeeltelijk gehydrogeneerd om te voorkomen dat deze uitscheidt. Consumenten zouden de hoeveelheid verzadigd vet in hun dieet kunnen verminderen door de originele onbewerkte oliën op hun voedsel te gebruiken, maar de meeste mensen smeren liever margarine op hun toast dan er olie over te gieten.
Veel mensen zijn overgestapt van boter op margarine of plantaardige shortening vanwege de bezorgdheid dat verzadigde dierlijke vetten het cholesterolgehalte in het bloed kunnen verhogen en kunnen leiden tot dichtgeslibde slagaders. Bij de hydrogenering van plantaardige oliën treedt echter een isomerisatiereactie op waarbij de in het openingsessay genoemde transvetzuren ontstaan. Studies hebben echter aangetoond dat transvetzuren ook het cholesterolgehalte verhogen en het optreden van hartziekten doen toenemen. Transvetzuren hebben niet de kromming in hun structuur die bij cis-vetzuren optreedt en pakken zich dus net zo samen als de verzadigde vetzuren dat doen. Consumenten wordt nu geadviseerd meervoudig onverzadigde oliën en zachte of vloeibare margarine te gebruiken en hun totale vetconsumptie te beperken tot minder dan 30% van hun totale calorie-inname per dag.
Vetten en oliën die bij kamertemperatuur in contact komen met vochtige lucht ondergaan uiteindelijk oxidatie- en hydrolysereacties waardoor ze ranzig worden en een karakteristieke, onaangename geur krijgen. Een van de oorzaken van de geur is het vrijkomen van vluchtige vetzuren door hydrolyse van de esterbindingen. Boter, bijvoorbeeld, geeft stinkende boterzuur, caprylzuur en caprinezuur vrij. Micro-organismen die in de lucht aanwezig zijn, leveren lipasen die dit proces katalyseren. Hydrolytische ranzigheid kan gemakkelijk worden voorkomen door het vet of de olie af te dekken en in een koelkast te bewaren.
Een andere oorzaak van vluchtige, stinkende verbindingen is de oxidatie van de onverzadigde vetzuurcomponenten, met name de gemakkelijk geoxideerde structuureenheid

in meervoudig onverzadigde vetzuren, zoals linolzuur en linoleenzuur. Een bijzonder aanstootgevend product, gevormd door de oxidatieve splitsing van beide dubbele bindingen in deze eenheid, is een verbinding die malonaldehyde wordt genoemd.
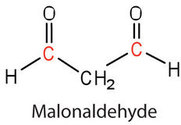
Ranzigheid is een grote zorg van de voedingsindustrie, en daarom zijn voedingschemici altijd op zoek naar nieuwe en betere antioxidanten, stoffen die in zeer kleine hoeveelheden (0,001%-0,01%) worden toegevoegd om oxidatie te voorkomen en zo ranzigheid te onderdrukken. Antioxidanten zijn verbindingen waarvan de affiniteit voor zuurstof groter is dan die van de lipiden in het levensmiddel; zij werken dus door bij voorkeur de toevoer van zuurstof die in het product wordt opgenomen, uit te putten. Omdat vitamine E antioxiderende eigenschappen heeft, helpt het de schade aan de lipiden in het lichaam te beperken, vooral aan de onverzadigde vetzuren die in de lipiden van de celmembranen voorkomen.