Kooldioxidegas wordt geproduceerd door de ademhaling van mensen en dieren, Het wordt geproduceerd door de verbranding van steenkool of koolwaterstoffen, de gisting van vloeistoffen, en Het is een kleurloos, smaakloos en reukloos gas.
Eigenschappen van kooldioxidegas
Kooldioxidegas (CO2) is een van de meest stabiele moleculen, omdat het bestaat uit een enkel koolstofatoom dat covalent gebonden is aan twee zuurstofatomen, en deze binding is zeer sterk, en het is een gas bij standaardtemperatuur en -druk.
Koolstofdioxidegas kan de pH van het water veranderen en het lost enigszins op in het water om een zwak zuur te vormen dat koolzuur wordt genoemd, en het is een broeikasgas aangezien het zichtbaar licht doorlaat maar het absorbeert sterk in het infrarood en nabij-infrarood. Koolzuurgas brandt niet en helpt niet bij het verbranden, dus wordt het gebruikt bij het blussen van branden, en het is zwaarder dan de lucht, dus wordt het opgevangen door opwaartse verplaatsing van lucht.

Eigenschappen van kooldioxidegas
De meeste kooldioxide-eenheden zijn van nature licht zuur, de zuurgraad kan worden gewijzigd door de moleculen in het water op te lossen, het is oplosbaar in ethanol en in aceton, het wordt gemakkelijk in het water opgelost, zodat het niet door de verplaatsing van water wordt opgevangen.
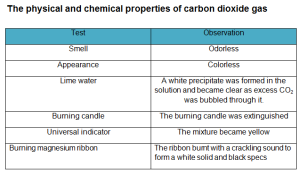
Koolstofdioxidegas eigenschappen.
Kooldioxidegas reageert met alkaliën om carbonaten en bicarbonaten te geven, het is een lineaire covalente molecule, het is een zuur oxide, en het reageert met het water om koolzuur te geven. Koolzuurgas reageert met magnesium tot magnesiumoxide (wit poeder) en koolstof of steenkool (zwarte substantie) die neerslaat op de wand van de cilinder.
Koolzuurgas wordt bereid door verdund zoutzuur toe te voegen aan calciumcarbonaat, het wordt bereid door opwaartse verplaatsing van lucht omdat het zwaarder is dan de lucht, en het wordt niet opgevangen door verplaatsing van water omdat het gemakkelijk oplost in het water, en het wordt ook bereid door citroensap of azijn toe te voegen aan natriumbicarbonaat (het ruggengraatpoeder).
Koolstofdioxidegas vormt een vaste stof bij temperaturen beneden -70 graden Celsius (-94° Fahrenheit), Het kan ook in een vloeistof veranderen wanneer het onder constante druk in het water wordt opgelost, het is zeer stabiel, en het is grotendeels onaangetast als het met veel andere materialen in de atmosfeer interageert.
Wanneer we kooldioxidegas inademen in concentraties die veel hoger zijn dan de gebruikelijke atmosferische niveaus, kan het een zure smaak in de mond en een prikkend gevoel in de neus en keel veroorzaken, omdat kooldioxidegas oplost in de slijmvliezen en het speeksel, en het vormt een zwakke oplossing van koolzuur.
Koolstofdioxidegasmolecule is matig reactief en is niet brandbaar, maar het ondersteunt de verbranding van metalen zoals magnesium, het bevat twee dubbele bindingen en het heeft een lineaire vorm, het heeft geen elektrische dipool, en het is volledig geoxideerd.