Generieke naam: natrium polystyreen sulfonaat
Doseringsvorm: orale / rectale suspensie
Medisch beoordeeld door Drugs.com. Laatst bijgewerkt op 22 jul 2020.
- Overzicht
- Bijwerkingen
- Dosering
- Professioneel
- Interacties
- Meer
- Indicaties en gebruik voor Kionex
- Kionex Dosering en toediening
- Algemene informatie
- Aanbevolen dosering
- Bereiding en toediening
- Doseringsvormen en sterktes
- Contra-indicaties
- Waarschuwingen en voorzorgsmaatregelen
- Intestinale necrose
- Electrolytstoornissen
- Vochtoverbelasting bij patiënten die gevoelig zijn voor hoge natriuminname
- Risico op Aspiratie
- Binding met andere oraal toegediende geneesmiddelen
- Bijwerkingen
- Gedragsinteracties
- Algemene interacties
- Kation-donerende antacida
- Sorbitol
- Gebruik IN SPECIFIEKE POPULATIES
- Zwangerschap
- Lactatie
- Pediatrisch gebruik
- Overdosering
- Kionex Beschrijving
- Kionex – Klinische farmacologie
- Werkingsmechanisme
- Pharmacodynamiek
- Pharmacokinetiek
- Nonklinische toxicologie
- Carcinogenese, Mutagenese, Vruchtbaarheidsaantasting
- Hoe te leveren/Verwerking en opslag
- Patient Counseling Information
- PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
- Meer over Kionex (natriumpolystyreensulfonaat)
- Consumer resources
- Professionele hulpbronnen
- Gerelateerde behandelingsgidsen
Indicaties en gebruik voor Kionex
Kionexis geïndiceerd voor de behandeling van hyperkaliëmie.
Gebruiksbeperking:
Kionex mag niet worden gebruikt als een noodbehandeling voor levensbedreigende hyperkaliëmie vanwege de vertraagde werking.
Kionex Dosering en toediening
Algemene informatie
Dien Kionex ten minste 3 uur vóór of 3 uur na andere orale medicatie toe. Bij patiënten met gastroparese kan een scheiding van 6 uur nodig zijn
Aanbevolen dosering
De intensiteit en duur van de therapie zijn afhankelijk van de ernst en de weerstand van de hyperkaliëmie.
Oraal
De gemiddelde totale dagelijkse dosis van Kionex voor volwassenen is 15 g tot 60 g, toegediend als een dosis van 15 g (vier afgestreken theelepels), één tot vier maal daags.
Rectaal
De gemiddelde dosis voor volwassenen is 30 g tot 50 g om de zes uur.
Bereiding en toediening
Suspensie vers bereiden en binnen 24 uur gebruiken.
Kionex niet verwarmen omdat dit de uitwisselingseigenschappen van de hars kan veranderen.
Een afgestreken theelepel bevat ongeveer 3,5 g Kionex en 15 mEq natrium.
Orale suspensie
Suspendeer elke dosis in een kleine hoeveelheid water of siroop, ongeveer 3 tot 4 mL vloeistof per gram hars. Toedienen terwijl de patiënt rechtop zit.
Enema
Na een eerste reinigend klysma brengt u een zachte rubberen buis van groot formaat (Frans 28) in het rectum in over een afstand van ongeveer 20 cm, met de punt goed in het sigmoïd colon, en plakt u hem vast.
Toedienen als een warme (lichaamstemperatuur) emulsie in 100 ml waterig medium en uitspoelen met 50 tot 100 ml vloeistof. Een iets dikkere suspensie kan worden gebruikt, maar vorm geen pasta.
Geweer de emulsie voorzichtig tijdens toediening. De hars moet zo lang mogelijk worden ingehouden en gevolgd worden door een reinigend klysma met een niet-natriumhoudende oplossing. Zorg voor een voldoende volume reinigingsoplossing (tot 2 liter).
Doseringsvormen en sterktes
Kionex is een crème tot lichtbruin, fijngemalen poeder en is verkrijgbaar in potten van 454 g.
Contra-indicaties
Kionex is gecontra-indiceerd bij patiënten met de volgende aandoeningen:
– Overgevoeligheid voor polystyreen sulfonaat harsen – Obstructieve darmziekte – Neonaten met verminderde darmmotiliteit
Waarschuwingen en voorzorgsmaatregelen
Intestinale necrose
Er zijn gevallen van intestinale necrose, sommige met dodelijke afloop, en andere ernstige gastro-intestinale bijwerkingen (bloedingen, ischemische colitis, perforatie) gemeld in verband met het gebruik van Kionex. In de meerderheid van deze gevallen werd melding gemaakt van gelijktijdig gebruik van sorbitol. Risicofactoren voor gastro-intestinale bijwerkingen waren in veel van de gevallen aanwezig, waaronder prematuriteit, een voorgeschiedenis van een darmziekte of -operatie, hypovolemie, en nierinsufficiëntie en -falen. Gelijktijdige toediening van sorbitol wordt niet aanbevolen.
– Alleen gebruiken bij patiënten met een normale darmfunctie. Vermijd gebruik bij patiënten die na de operatie geen stoelgang hebben gehad. – Vermijd gebruik bij patiënten met een risico op het ontwikkelen van constipatie of impactie (inclusief patiënten met een voorgeschiedenis van impactie, chronische constipatie, inflammatoire darmziekte, ischemische colitis, vasculaire intestinale atherosclerose, eerdere darmresectie, of darmobstructie). Staak het gebruik bij patiënten die constipatie ontwikkelen.
Electrolytstoornissen
Controleer het serumkalium tijdens de behandeling omdat ernstige hypokaliëmie kan optreden.
Kionex is niet volledig selectief voor kalium, en kleine hoeveelheden van andere kationen zoals magnesium en calcium kunnen ook verloren gaan tijdens de behandeling. Controleer calcium en magnesium bij patiënten die Kionex krijgen.
Vochtoverbelasting bij patiënten die gevoelig zijn voor hoge natriuminname
Elke dosis van 15 g Kionex bevat 1500 mg (60 mEq) natrium. Controleer patiënten die gevoelig zijn voor natriuminname (hartfalen, hypertensie, oedeem) op tekenen van vochtoverbelasting. Aanpassing van andere natriumbronnen kan nodig zijn.
Risico op Aspiratie
Gevallen van acute bronchitis of bronchopneumonie veroorzaakt door inhalatie van natriumpolystyreensulfonaatdeeltjes zijn gemeld. Patiënten met een verminderde kokhalsreflex, een veranderd bewustzijnsniveau of patiënten die gevoelig zijn voor regurgitatie kunnen een verhoogd risico lopen. Dien Kionex toe met de patiënt rechtop.
Binding met andere oraal toegediende geneesmiddelen
Kionex kan oraal toegediende geneesmiddelen binden, wat hun gastro-intestinale absorptie kan verminderen en kan leiden tot verminderde werkzaamheid. Dien andere orale medicatie ten minste 3 uur voor of 3 uur na Kionex toe. Bij patiënten met gastroparese kan een scheiding van 6 uur nodig zijn.
Bijwerkingen
De volgende bijwerkingen worden elders in de etikettering besproken:
– Darmnecrose – Elektrolytstoornissen – Aspiratie
De volgende bijwerkingen zijn vastgesteld tijdens post-goedkeuringsgebruik van Kionex. Omdat deze reacties vrijwillig worden gemeld uit een populatie van onzekere omvang, is het niet altijd mogelijk om de frequentie ervan betrouwbaar te schatten of een oorzakelijk verband met de blootstelling aan het geneesmiddel vast te stellen.
Gastro-intestinaal: anorexie, constipatie, diarree, fecale impactie, gastro-intestinale concreties (bezoars), ischemische colitis, misselijkheid, ulceraties, braken, maagirritatie, intestinale obstructie (als gevolg van de concentratie van aluminiumhydroxide)
Metabool: systemische alkalose
Gedragsinteracties
Algemene interacties
Er zijn geen formele interactiestudies met geneesmiddelen uitgevoerd bij mensen.
Kionex heeft het potentieel om andere geneesmiddelen te binden. In in vitro bindingsstudies werd aangetoond dat Kionex de orale geneesmiddelen (n=6) die werden getest significant bindt. Verminderde absorptie van lithium en thyroxine zijn ook gemeld bij gelijktijdige toediening van Kionex. Binding van Kionex aan andere orale geneesmiddelen kan leiden tot verminderde gastro-intestinale absorptie en verlies van werkzaamheid wanneer het middel wordt ingenomen vlak na de toediening van Kionex. Dien Kionex ten minste 3 uur vóór of 3 uur na andere orale medicatie toe. Bij patiënten met gastroparese kan een scheiding van 6 uur nodig zijn. Monitor waar mogelijk op klinische respons en/of bloedspiegels.
Kation-donerende antacida
De gelijktijdige orale toediening van Kionex met niet-absorbeerbare kation-donerende antacida en laxeermiddelen kan het kaliumuitwisselingsvermogen van de hars verminderen en het risico van systemische alkalose verhogen.
Sorbitol
Sorbitol kan bijdragen aan het risico van intestinale necrose en gelijktijdig gebruik wordt niet aanbevolen.
Gebruik IN SPECIFIEKE POPULATIES
Zwangerschap
Samenvatting van de risico’s
Kionex wordt niet systemisch geabsorbeerd na orale of rectale toediening en het is niet te verwachten dat maternaal gebruik leidt tot foetaal risico.
Lactatie
Risicosamenvatting
Kionex wordt niet systemisch door de moeder geabsorbeerd, zodat borstvoeding naar verwachting geen risico voor de zuigeling inhoudt.
Pediatrisch gebruik
Er zijn geen onderzoeken naar de veiligheid en werkzaamheid bij pediatrische patiënten uitgevoerd.
Bij pediatrische patiënten wordt, net als bij volwassenen, verwacht dat Kionex kalium bindt bij de praktische uitwisselingsratio van 1mEq kalium per 1 gram hars.
Bij neonaten dient Kionex niet oraal te worden toegediend. Zowel bij kinderen als bij neonaten kan een te hoge dosering of een onvoldoende verdunning leiden tot impactie van de hars. Premature zuigelingen of zuigelingen met een laag geboortegewicht kunnen een verhoogd risico hebben op gastro-intestinale bijwerkingen met Kionex. gebruik .
Overdosering
Overdosering kan leiden tot elektrolytstoornissen, waaronder hypokaliëmie, hypocalciëmie en hypomagnesiëmie. Passende maatregelen moeten worden genomen om serumelektrolyten (kalium, calcium, magnesium) te corrigeren, en de hars moet uit het spijsverteringskanaal worden verwijderd door het juiste gebruik van laxeermiddelen of klysma’s.
Kionex Beschrijving
Kionex is een benzeen, diethenyl-polymeer, met ethenylbenzeen, gesulfoneerd, natriumzout en heeft de volgende structuurformule:
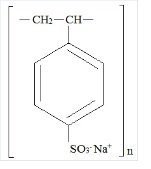
Het geneesmiddel is een crème tot lichtbruine fijngemalen, poedervorm van natriumpolystyreensulfonaat, een kationenuitwisselingshars bereid in de natriumfase met een in vitro uitwisselingscapaciteit van ongeveer 3.1 mEq (in vivo ongeveer 1 mEq) kalium per gram. Het natriumgehalte bedraagt ongeveer 100 mg (4,1 mEq) per gram van het geneesmiddel. Het kan oraal of rectaal als klysma worden toegediend.
Een gram Kionex bevat 4,1 mEq natrium.
Kionex – Klinische farmacologie
Werkingsmechanisme
Kionex is een niet-geabsorbeerd, kationuitwisselend polymeer dat een natrium-tegenion bevat.
Kionex verhoogt de uitscheiding van kalium in de feces door binding van kalium in het lumen van het maagdarmkanaal. Het binden van kalium verlaagt de concentratie van vrij kalium in het maagdarmlumen, wat resulteert in een verlaging van het serumkaliumgehalte. De praktische uitwisselingsratio is 1 mEq K per 1 gram hars.
Terwijl de hars door de darm passeert of in het colon wordt vastgehouden na toediening door middel van een klysma, komen de natriumionen gedeeltelijk vrij en worden vervangen door kaliumionen. Dit gebeurt voornamelijk in de dikke darm, die meer kaliumionen uitscheidt dan de dunne darm. De efficiëntie van dit proces is beperkt en onvoorspelbaar variabel.
Pharmacodynamiek
De effectieve verlaging van serumkalium met Kionex kan uren tot dagen duren.
Pharmacokinetiek
De in vivo efficiëntie van natrium-kalium uitwisselende harsen is ongeveer 33 procent; dus ongeveer een derde van het werkelijke natriumgehalte van de hars wordt aan het lichaam afgegeven.
Kionex wordt niet systemisch geabsorbeerd.
Drug Interactions
In vitro bindingsstudies toonden aan dat Kionex significant bindt aan de volgende geteste geneesmiddelen – warfarine, metoprolol, fenytoïne, furosemide, amlodipine en amoxicilline.
Nonklinische toxicologie
Carcinogenese, Mutagenese, Vruchtbaarheidsaantasting
Er zijn geen studies verricht.
Hoe te leveren/Verwerking en opslag
Kionex is verkrijgbaar als roomkleurig tot lichtbruin, fijngemalen poeder in potten van 1 pond (454 g), NDC 0574-2004-16.
bewaren bij 20° tot 25°C (68° tot 77°F) .
Patient Counseling Information
Drug Interactions
Adviseer patiënten die andere orale medicatie gebruiken om de dosering van Kionex te scheiden met ten minste 3 uur (voor of na)
Rx Only
Packaged by
Perrigo
Minneapolis, MN 55427
Revised 08/2017
PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
Rx Only
NDC 0574-2004-16
Kionex®
Sodium Polystyrene Sulfonate for Suspension
AVERAGE ADULT DOSE: 15 g (ongeveer 4 afgestreken theelepels) een- tot viermaal daags in water. Zie de volledige voorschrijfinformatie.
Het effect moet zorgvuldig worden gecontroleerd door frequente serumkaliumbepalingen binnen elke periode van 24 uur. Natriumgehalte ongeveer 60 mEq per 15 g.
Suspensie dient vers te worden bereid en niet langer dan 24 uur te worden bewaard. Doseren in dichte, lichtbestendige containers zoals gedefinieerd in de USP.
OPSLAG: Bewaren bij 20° tot 25°C .
Lees de bijsluiter.
454 gram (1 LB)
| Kionex natrium polystyreen sulfonaat poeder, voor suspensie |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Etiketteerder – Paddock Laboratories, LLC (967694121)
Meer over Kionex (natriumpolystyreensulfonaat)
- Bijwerkingen
- Tijdens zwangerschap of borstvoeding
- Doseringsinformatie
- Gemedicijninteracties
- En Español
- 4 Beoordelingen
- Gedicijnsklasse: kationenwisselaarsharsen
- FDA Alerts (2)
Consumer resources
- Patient Information
- Kionex (Advanced Reading)
Professionele hulpbronnen
- Voorschrijfinformatie
- Natrium Polystyreen Sulfonaat Oraal Poeder (FDA)
Andere merken Kayexalate, Kalexate
Gerelateerde behandelingsgidsen
- Hyperkaliëmie
Medische disclaimer