Inleiding
Pancreaskanker verwijst meestal naar ductaal carcinoom van de pancreas, dat tot 90% van de primaire pancreasmaligniteiten omvat. Het resterende aantal kan worden onderverdeeld in exocriene tumoren (zoals pancreascystisch carcinoom) en endocriene tumoren (afkomstig van eilandjescellen van de alvleesklier).
Pancreaskanker heeft een hoog sterftecijfer, het is de 4e meest voorkomende doodsoorzaak door kanker in het Verenigd Koninkrijk. Het komt zelden voor onder de 40 jaar, met 80% van de gevallen tussen 60-80 jaar. De diagnose wordt zelden vroeg genoeg gesteld voor een curatieve behandeling.
In dit artikel zullen we de risicofactoren, onderzoeken en behandeling van een patiënt met alvleesklierkanker bekijken.
Pathofysiologie
De meest voorkomende vorm van alvleesklierkanker is ductaal carcinoom (90% van de primaire maligniteiten van de alvleesklier). Andere zeldzamere vormen zijn cysteuze tumoren, ampullaire celtumoren en eilandjesceltumoren, die alle vaak een veel betere prognose hebben.
Als de kanker zich uitbreidt, betreft de directe invasie van lokale structuren meestal de milt, het colon transversus en de bijnieren. Lymfatische metastase betreft meestal regionale lymfeklieren, lever, longen en peritoneum. Metastase komt vaak voor op het moment van de diagnose.
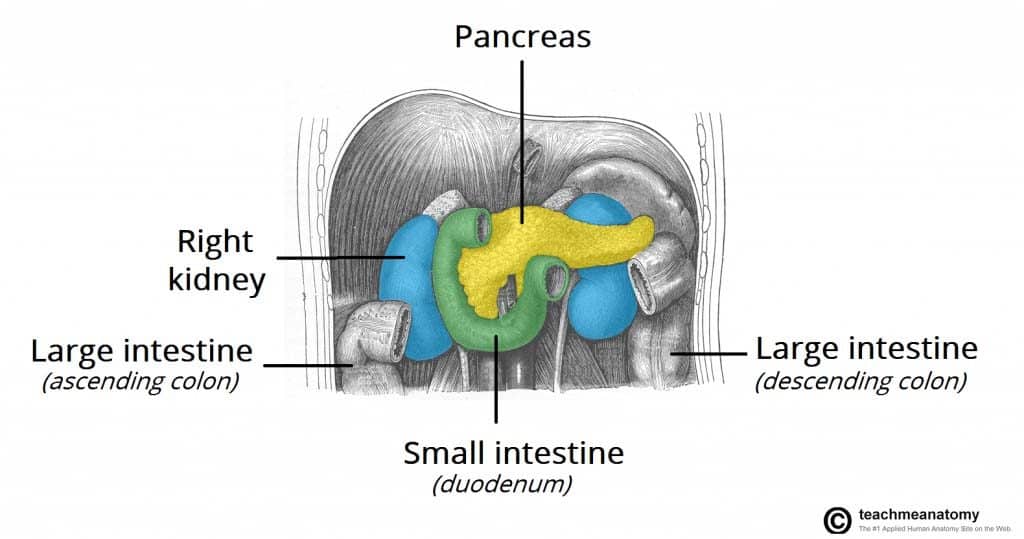 Figuur 1 – Alvleesklierkanker kan direct uitzaaien naar omliggende structuren, zoals de milt, het colon en de bijnieren.
Figuur 1 – Alvleesklierkanker kan direct uitzaaien naar omliggende structuren, zoals de milt, het colon en de bijnieren.Risicofactoren
Er zijn weinig duidelijke risicofactoren voor de ontwikkeling van carcinoom van de alvleesklier. Tot de vastgestelde risicofactoren behoren roken en chronische pancreatitis. Er kan ook een erfelijk element zijn, aangezien 7% van de patiënten een familiegeschiedenis van de ziekte heeft.
Late aanvang van diabetes mellitus is een extra risicofactor. Degenen bij wie diabetes is vastgesteld >50 jaar hebben een 8x groter risico op het ontwikkelen van pancreascarcinoom in de volgende drie jaar dan de algemene bevolking.
Clinische presentatie
In ongeveer 80% van de gevallen van pancreascarcinoom is de diagnose niet te stellen, hetgeen getuigt van de late en vaak vage en niet-specifieke aard van de presentatie ervan.
De specifieke klinische kenmerken* kunnen afhangen van de plaats van de tumor:
- Obstructieve geelzucht – te wijten aan compressie van de gemeenschappelijke galbuis (aanwezig in 90% van de gevallen op het ogenblik van de diagnose), gewoonlijk pijnloos
- Gewichtsverlies – te wijten aan de metabole effecten van de kanker, of secundair aan exocriene dysfunctie
- Buikpijn (aspecifiek) – als gevolg van invasie van de plexus coeliacus of secundair aan pancreatitis
Minder vaak voorkomende presentaties zijn acute pancreatitis of tromboflebitis migrans (een recidiverende migrerende oppervlakkige tromboflebitis, veroorzaakt door een paraneoplastische hypercoagulabele toestand).
*Tumoren van de staart van de pancreas hebben een sluipend beloop en zijn vaak pas in een laat stadium symptomatisch
Bij onderzoek kunnen de patiënten er cachectisch, ondervoed en geelzuchtig uitzien. Bij palpatie kan een abdominale massa in de epigastrische regio worden gevoeld, evenals een vergrote galblaas (volgens de Wet van Courvoisier)
Wet van Courvoisier
De Wet van Courvoisier stelt dat in aanwezigheid van geelzucht en een vergrote/palpabele galblaas, maligniteit van de galwegen of de alvleesklier sterk moet worden verdacht, omdat het onwaarschijnlijk is dat galstenen de oorzaak zijn.
Dit teken kan aanwezig zijn als de verstoppende tumor distaal van het cystic duct is gelegen. In werkelijkheid komt een vergrote galblaas voor bij minder dan 25% van de patiënten met pancreaskanker.
Differentiële diagnose
Pancreaskanker presenteert zich vaak met vage, niet-specifieke kenmerken. De differentiële diagnoses zijn uitgebreid en omvatten:
- Oorzaken van obstructieve geelzucht – galsteenziekte, cholangiocarcinoom, benigne galblaas strictuur
- Oorzaken van epigastrische buikpijn – galstenen, peptische ulcus ziekte, maagcarcinoom, acuut coronair syndroom
Onderzoeken
Laboratoriumonderzoek
Bij verdenking van pancreaskanker moet eerst bloedonderzoek worden verricht, waaronder FBC (anemie of trombocytopenie) en LFT’s (verhoogde bilirubine, alkalische fosfatase en gamma-GT, die een obstructief geelzuchtbeeld laten zien).
CA19-9 is een tumormarker met een hoge sensitiviteit en specificiteit voor pancreaskanker, maar de rol ervan is eerder bij de beoordeling van de respons op behandeling dan voor de initiële diagnose.
Imaging
De initiële beeldvorming voor pancreaskanker is gewoonlijk een abdominale echografie, die een pancreasmassa of een verwijde galboom kan aantonen (evenals mogelijke levermetastasen en ascites indien de ziekte zich in een zeer laat stadium bevindt).
CT beeldvorming (met gebruik van een pancreas protocol, Fig. 2) is zowel het belangrijkste onderzoek in termen van diagnose, maar ook het meest prognostisch informatief omdat het ziekteprogressie kan stadiëren. Een CT-scan van borst-abdomen-pelvis is verder vereist wanneer pancreaskanker is gediagnosticeerd voor stadiëring; een PET-CT-scan kan gerechtvaardigd zijn bij degenen met gelokaliseerde ziekte op CT die een kankerbehandeling zullen ondergaan
Endoscopische echografie (EUS) kan vervolgens worden gebruikt om een fijne naald aspiratie biopsie te leiden om de laesie histologisch te evalueren, als de diagnose nog onduidelijk is. ERCP kan ook worden gebruikt om toegang te krijgen tot de laesie voor biopsie of cytologie, indien op een geschikte plaats*.
*Een galwegborsteling voor cytologie indien ERCP wordt gebruikt om de galwegobstructie te verlichten en er geen weefseldiagnose is.
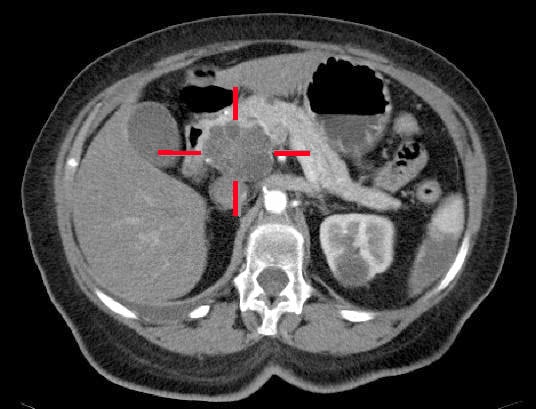 Figuur 2 – Een adenocarcinoom gelokaliseerd in de pancreaskop, geïdentificeerd op CT-scan
Figuur 2 – Een adenocarcinoom gelokaliseerd in de pancreaskop, geïdentificeerd op CT-scanBehandeling
Chirurgie
De enige curatieve behandelingsoptie is momenteel radicale resectie:
- Voor patiënten met tumoren van de kop van de alvleesklier is de meest gebruikelijke operatie met curatieve intentie pancreaticoduodenectomie, ook bekend als Whipple’s procedure
- Pylorussparende resecties kunnen in bepaalde gevallen worden geprobeerd
- Voor patiënten met tumoren van het lichaam of de staart van de alvleesklier, kan vaak een distale pancreatectomie worden uitgevoerd
Absolute contra-indicaties voor chirurgie zijn peritoneale, lever- en verre metastasen. Er is een hoge morbiditeit geassocieerd met deze procedures (tot 40%) en specifieke complicaties omvatten vorming van een pancreasfistel, vertraagde maaglediging en pancreasinsufficiëntie.
Een Cochrane-review vond dat pancreasresectie de overleving verhoogt en de kosten verlaagt in vergelijking met palliatieve behandelingen bij patiënten met lokaal gevorderde pancreaskanker en veneuze betrokkenheid, ervan uitgaande dat er voldoende klinische expertise beschikbaar is.
Whipple’s Procedure
Bij een Whipple’s procedure worden de kop van de pancreas, het antrum van de maag, het 1e en 2e deel van het duodenum, de gemeenschappelijke galbuis en de galblaas verwijderd.
Alle ingewanden die bij de operatie worden verwijderd, worden verwijderd vanwege hun gemeenschappelijke arteriële toevoer (de gastroduodenale slagader), die wordt gedeeld door de kop van de alvleesklier en de twaalfvingerige darm.
Vervolgens worden de staart van de pancreas en de leverbuis aan het jejunum gehecht, waardoor gal en pancreassappen in de darm kunnen wegvloeien, terwijl de maag vervolgens met het jejunum wordt geanastomeerd, zodat voedsel kan worden doorgevoerd.
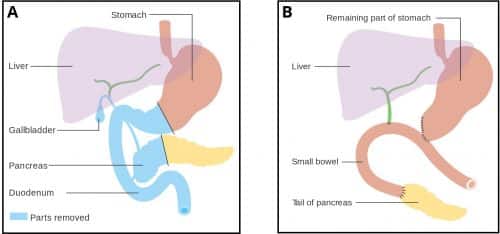 Figuur 3 – Pancreaticoduodenectomie (Whipple’s procedure). A: vóór de procedure, B: na de procedure
Figuur 3 – Pancreaticoduodenectomie (Whipple’s procedure). A: vóór de procedure, B: na de procedure
Chemotherapie
Adjuvante chemotherapie, in het algemeen met 5-flourouracil, wordt na de operatie aanbevolen omdat is aangetoond dat deze de overleving verbetert na de ESPAC-1-studie*.
Bij uitgezaaide ziekte wordt het gebruik van het FOLFIRINOX-regime (folinezuur, 5-fluorouracil, irinotecan en oxaliplatin) aanbevolen bij mensen met een goede prestatiestatus, maar dit heeft slechts een bescheiden verbetering van de overleving opgeleverd; gemcitabinetherapie kan worden overwogen voor mensen met lokaal gevorderde pancreaskanker die niet goed genoeg zijn om FOLFIRINOX te verdragen.
*ESPAC-1 toonde ook aan dat patiënten die werden behandeld met adjuvante chemoradiotherapie over het geheel slechtere uitkomsten hadden dan patiënten die alleen met adjuvante chemotherapie werden behandeld.
Palliatieve zorg
De meerderheid van de patiënten met pancreaskanker komt niet in aanmerking voor een curatieve operatie, maar heeft in plaats daarvan palliatieve zorg nodig.
Obstructieve geelzucht en de daarmee gepaard gaande pruritis kunnen worden verlicht door het inbrengen van een galwegstent, via ERCP of percutaan.
Palliatieve chemotherapie, zoals met een op gemcitabine gebaseerd regime, kan worden uitgeprobeerd bij patiënten met een redelijke prestatiestatus.
Exocriene insufficiëntie komt vaak voor bij gevorderde ziekte of bij patiënten die een aanzienlijke excisie van de alvleesklier hebben ondergaan, wat leidt tot malabsorptie en steatorroe; dit kan in eerste instantie worden behandeld met enzymvervangers (inclusief lipasen), zoals Creon®.
Prognose
Pancreaskanker heeft een hoog metastatisch vermogen, zelfs bij kleine tumoren. De prognose bij pancreaskanker blijft zeer slecht, met een totale 5-jaarsoverleving van <5%.
Key Points
- Pancreaskanker zal zich vaak presenteren met een combinatie van obstructieve geelzucht, buikpijn of gewichtsverlies
- De meeste gevallen worden in eerste instantie op CT-scan ontdekt, maar vereisen een weefseldiagnose door middel van biopsie; CA19-9 is een tumormarker die wordt gebruikt voor het monitoren van ziekteprogressie
- Definitieve behandeling is chirurgische resectie, vaak met adjuvante chemotherapie
- Pancreaskanker heeft een 5-jaarsoverleving van minder dan 5%
Endocriene tumoren van de pancreas
Endocriene tumoren van de pancreas kunnen functioneel of niet-functioneel zijn. Functionele tumoren scheiden actief hormonen af en hun tekenen en symptomen houden hiermee verband, terwijl niet-functionele tumoren geen actieve hormonen afscheiden en de klinische kenmerken louter verband houden met hun kwaadaardige verspreiding.
Endocriene tumoren van de alvleesklier worden vaak geassocieerd met het multipele endocriene neoplasie 1-syndroom (MEN1); MEN1 bestaat meestal uit hyperparathyreoïdie, endocriene pancreastumoren en hypofysetumoren (meestal prolactinomen).
Klinische kenmerken
| Celtype | Afgescheiden hormoon (naam van tumor) | Normale fysiologische functie | Kenmerken van functionele tumor |
| G-cellen | Gastrine (gastrinoma) | Stimuleert afgifte maagzuur | Zollinger-Ellison syndroom, resulterend in ernstige peptische zweren, refractair voor medische behandeling, met diarree en steatorroe |
| α Cellen | Glucagon (Glucagonoma) | Verhoogt bloedglucoseconcentratie | Hyperglykemie, diabetes mellitus, en necrolytisch migratief erytheem |
| β Cellen | Insuline (insulinoom) | Verlaging bloedglucoseconcentratie | Symptomatische hypoglykemie, zoals zweten of veranderde mentale toestand, verbetering bij consumptie van koolhydraten |
| δ Cellen | Somatostatine (Somatostatinoom) | Remmt de afgifte van GH, TSH en prolactine uit de voorste hypofyse, en van gastrine | Diabetes mellitus, steatorroe, galstenen (door remming van cholecystokinine), gewichtsverlies, en achlorhydria (door remming van gastrine) |
| Non-isletcellen | Vasoactief intestinaal peptide (VIPoma) | Secretie van water en elektrolyten in de darm. Ontspanning van de darmgladde spier. | Lange overvloedige waterige diarree, ernstige hypokaliëmie en uitdroging (ook bekend als het syndroom van Verner-Morrison) |
Tabel 1 – Endocriene tumoren van de alvleesklier
Onderzoek
Alle gevallen moeten worden besproken tijdens een multidisciplinaire teamvergadering waar het beheer kan worden gestuurd. Bepaalde bloedonderzoeken kunnen worden gestuurd, afhankelijk van het vermoedelijke subtype (tabel 1)
Pancreatische NET’s worden het best onderzocht met een combinatie van CT-beeldvorming, MRI-beeldvorming, en/of endoscopische echografie. Intra-arteriële calcium met digitale subtractie-angiografie kan ook worden gebruikt bij de lokalisatie en beoordeling van insulinomen en gastrinomen.
Behandeling
Kleine niet-functionele goed gedifferentieerde pancreas-NET’s (<1 cm) kunnen gewoon worden geobserveerd. Grotere of functionerende tumoren worden gereseceerd, waarbij eventuele verre metastatische ziekte ook wordt gereseceerd indien de tumor van lage graad is en de metastasen een gering volume hebben.
Somatostatineanalogen kunnen worden gebruikt om de effecten van hormonale hypersecretie te controleren en te verbeteren (zelfs in het geval van somatostatinomen).