Reações Químicas de Gorduras e Óleos
Gorduras e óleos podem participar de uma variedade de reações químicas – por exemplo, porque triglicerídeos são ésteres, eles podem ser hidrolisados na presença de um ácido, uma base, ou enzimas específicas conhecidas como lipases. A hidrólise de gorduras e óleos na presença de uma base é usada para fazer sabão e é chamada saponificação. Hoje em dia a maioria dos sabões são preparados através da hidrólise dos triglicéridos (muitas vezes do sebo, óleo de coco ou ambos) usando água sob alta pressão e temperatura. Carbonato de sódio ou hidróxido de sódio é então utilizado para converter os ácidos gordos em seus sais de sódio (moléculas de sabão):
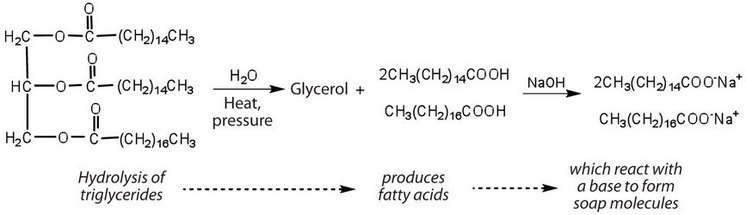
Looking Closer: Sabões
Sabão ordinário é uma mistura dos sais de sódio de vários ácidos gordos, produzidos numa das mais antigas sínteses orgânicas praticadas pelo homem (segundo apenas a fermentação dos açúcares para produzir álcool etílico). Tanto os fenícios (600 a.C.) como os romanos fabricavam sabão a partir de gordura animal e cinzas de madeira. Mesmo assim, a produção generalizada de sabão só começou a partir do século XVII. O sabão era tradicionalmente feito com banha ou sebo derretido com um ligeiro excesso de álcali em grandes cubas abertas. A mistura era aquecida, e o vapor era borbulhado através dela. Após a saponificação, o sabão era precipitado da mistura pela adição de cloreto de sódio (NaCl), removido por filtração, e lavado várias vezes com água. Foi então dissolvido em água e reprecipitado com a adição de mais NaCl. A glicerina produzida na reação também foi recuperada das soluções aquosas de lavagem.
Pumice ou areia é adicionada para produzir sabão para lavagem, enquanto ingredientes como perfumes ou corantes são adicionados para produzir sabonetes perfumados e coloridos. O sopro do ar através do sabão derretido produz um sabão flutuante. Sabonetes macios, feitos com sais de potássio, são mais caros mas produzem uma espuma mais fina e são mais solúveis. Eles são usados em sabonetes líquidos, xampus e cremes de barbear.
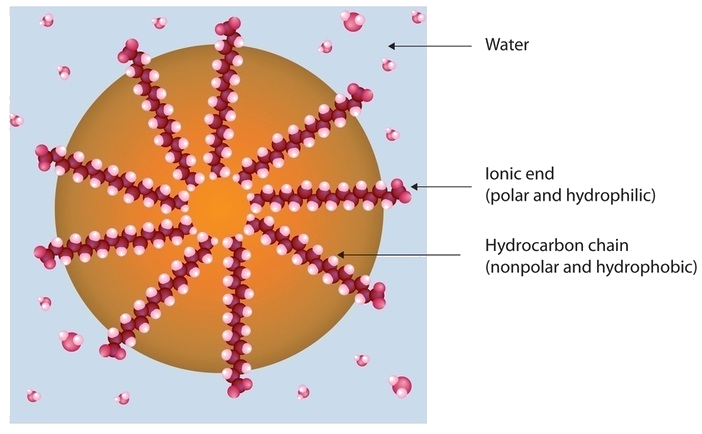
Sujeira e sujeira geralmente aderem à pele, roupas e outras superfícies, combinando com óleos corporais, gorduras de cozinha, graxas lubrificantes e substâncias similares que agem como colas. Como estas substâncias não são miscíveis na água, lavar apenas com água pouco faz para removê-las. No entanto, o sabão remove-as, porque as moléculas de sabão têm uma natureza dupla. Uma ponta, chamada cabeça, carrega uma carga iônica (um ânion carboxilato) e por isso se dissolve na água; a outra ponta, a cauda, tem uma estrutura de hidrocarbonetos e se dissolve em óleos. As caudas de hidrocarbonetos dissolvem-se no solo; as cabeças iônicas permanecem na fase aquosa, e o sabão quebra o óleo em gotículas minúsculas de sabão, chamadas micelas, que se dispersam por toda a solução. As gotículas se repelem entre si por causa de suas superfícies carregadas e não se coalescem. Com o óleo não mais “colando” a sujeira à superfície suja (pele, pano, prato), a sujeira fechada pelo sabão pode ser facilmente lavada.
As duplas ligações em gorduras e óleos podem sofrer hidrogenação e também oxidação. A hidrogenação de óleos vegetais para produzir gorduras semi-sólidas é um processo importante na indústria alimentar. Quimicamente, é essencialmente idêntica à reacção de hidrogenação catalítica descrita para os alcenos.

Em processos comerciais, o número de ligações duplas hidrogenadas é cuidadosamente controlado para produzir gorduras com a consistência desejada (macias e maleáveis). Óleos vegetais (canola, milho, soja) baratos e abundantes são assim transformados em margarinas e gorduras de cozinha. Na preparação da margarina, por exemplo, óleos parcialmente hidrogenados são misturados com água, sal e leite seco sem gordura, juntamente com agentes aromatizantes, corantes e vitaminas A e D, que são adicionados para aproximar o aspecto, sabor e nutrição da manteiga. (Também são adicionados conservantes e antioxidantes.) Na maioria da manteiga de amendoim comercial, o óleo de amendoim tem sido parcialmente hidrogenado para evitar que se separe. Os consumidores poderiam diminuir a quantidade de gordura saturada em sua dieta usando os óleos originais não processados em seus alimentos, mas a maioria das pessoas preferiria espalhar margarina em suas torradas do que jogar óleo sobre ela.
Muitas pessoas mudaram de manteiga para margarina ou encurtamento vegetal devido à preocupação de que gorduras animais saturadas possam elevar os níveis de colesterol no sangue e resultar em artérias entupidas. Entretanto, durante a hidrogenação dos óleos vegetais, ocorre uma reação de isomerização que produz os ácidos graxos trans mencionados no ensaio de abertura. No entanto, estudos demonstraram que os ácidos gordos trans também aumentam os níveis de colesterol e aumentam a incidência de doenças cardíacas. Os ácidos gordos trans não têm a curva nas suas estruturas, o que ocorre nos ácidos gordos cis e, por conseguinte, embalam-se de forma muito semelhante à dos ácidos gordos saturados. Os consumidores são agora aconselhados a utilizar óleos polinsaturados e margarinas macias ou líquidas e reduzir o seu consumo total de gordura para menos de 30% do seu consumo total de calorias por dia.
Gorduras e óleos que estão em contacto com o ar húmido à temperatura ambiente acabam por sofrer reacções de oxidação e hidrólise que os fazem ficar rançosos, adquirindo um odor característico desagradável. Uma das causas do odor é a liberação de ácidos graxos voláteis pela hidrólise das ligações ésteres. A manteiga, por exemplo, liberta ácidos butíricos, caprílicos e caprílicos com cheiro desagradável. Os microorganismos presentes no ar fornecem lipases que catalisam este processo. O ranço hidrolítico pode ser facilmente evitado cobrindo a gordura ou óleo e mantendo-o em um refrigerador.
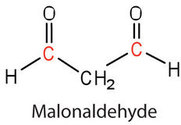
Outra causa de compostos voláteis e odoríferos é a oxidação dos componentes dos ácidos graxos insaturados, particularmente a unidade estrutural facilmente oxidada

em ácidos graxos polinsaturados, como os ácidos linoleico e linolênico. Um produto particularmente ofensivo, formado pela clivagem oxidativa de ambas as ligações duplas nesta unidade, é um composto chamado malonaldeído.
Rancidez é uma grande preocupação da indústria alimentar, razão pela qual os químicos alimentares estão sempre à procura de novos e melhores antioxidantes, substâncias adicionadas em quantidades muito pequenas (0,001%-0,01%) para prevenir a oxidação e assim suprimir a ranço. Os antioxidantes são compostos cuja afinidade com o oxigénio é maior do que a dos lípidos dos alimentos; assim, funcionam esgotando de preferência o fornecimento de oxigénio absorvido no produto. Como a vitamina E tem propriedades antioxidantes, ela ajuda a reduzir os danos aos lipídios no organismo, particularmente aos ácidos graxos insaturados encontrados nos lipídios da membrana celular.