Anemia hemolítica auto-imune (AIHA) é mediada por anticorpos, e na maioria dos casos a imunoglobulina (Ig) G é o anticorpo mediador. Este tipo de AIHA é referido como AIHA “quente” porque os anticorpos IgG ligam-se melhor à temperatura corporal. A AIHA “fria” é mediada por anticorpos IgM, que se ligam ao máximo a temperaturas inferiores a 37°C. A AIHA causada por uma reação medicamentosa é rara, com uma incidência anual estimada de 1:1.000.000 para a AIHA grave relacionada a medicamentos.1 Este artigo revisa o manejo dos tipos mais comuns de AIHA, com foco na AIHA quente, fria e induzida por medicamentos; a avaliação e diagnóstico da AIHA é revisada em um artigo separado.
Anemia Hemolítica Autoimune Quente
Na AIHA, a hemólise é mediada por anticorpos que se ligam à superfície dos glóbulos vermelhos. A AIHA em que os anticorpos IgG são os anticorpos ofensivos é referida como AIHA morna. “Quente” refere-se ao facto de o anticorpo se ligar melhor à temperatura corporal (37°C). Na AIHA quente, os testes irão mostrar moléculas IgG ligadas à superfície dos glóbulos vermelhos, com 50% dos doentes a mostrarem também C3. Entre 50% e 90% dos casos de AIHA são devidos a anticorpos quentes.2,3 A incidência de AIHA quente varia de acordo com a série, mas é aproximadamente 1 caso por 100.000 pacientes por ano; esta forma de hemólise afeta mais frequentemente as mulheres do que os homens.4,5
Opções terapêuticas
Primeira Linha
Esteroides. O objetivo da terapia em AIHA quente pode ser difícil de definir. Entretanto, a maioria concordaria que um hematócrito acima de 30% (ou superior para prevenir sintomas) com um aumento mínimo na contagem de reticulócitos – reflexo de um processo hemolítico significativamente retardado – é um objetivo razoável. O tratamento inicial da AIHA quente é a prednisona na dose padrão de 1 mg/kg diariamente (Tabela 1).6,7 Os pacientes também devem ser iniciados com inibidores da bomba de protões para prevenir úlceras. Pode levar até 3 semanas para que os pacientes respondam à terapia com prednisona. Assim que o hematócrito do paciente estiver acima de 30%, a prednisona é lentamente afilada. Embora aproximadamente 80% dos pacientes respondam aos esteróides, apenas 30% podem ser totalmente afilados dos esteróides. Para pacientes que podem ser mantidos com uma dose diária de esteróides de 10 mg ou menos, os esteróides podem ser a terapia mais razoável a longo prazo. Além disso, como a hemólise ativa leva a um aumento da demanda por ácido fólico, pacientes com AIHA quente são frequentemente prescritos 1 mg diários de ácido fólico para prevenir anemia megaloblástica devido à deficiência de ácido fólico.
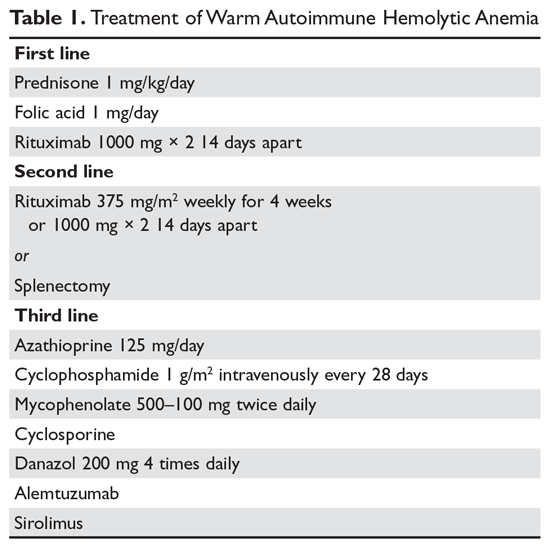
Rituximab. Cada vez mais, a terapia rituximab (anti-CD20) é adicionada aos esteróides iniciais. Dois ensaios clínicos mostraram tanto respostas de longo e curto prazo aumentadas com o uso de rituximab.8,9 Uma consideração importante é que a maioria dos pacientes respondem gradualmente ao rituximab durante semanas, então uma resposta rápida não deve ser esperada. A maioria dos estudos tem usado a dosagem tradicional de 375 mg/m2 semanalmente por 4 semanas. Estas respostas parecem ser duráveis, mas como em trombocitopenia imune (ITP), repetir o tratamento com rituximab é eficaz.
Os principais efeitos colaterais de rituximab são reações de infusão, que são frequentemente piores com a primeira dose. Estas reacções podem ser controladas com anti-histamínicos, esteróides, e, para rigores severos, meperidina. Raramente, os pacientes podem desenvolver neutropenia (aproximadamente 1:500) que parece ser auto-imune na natureza. As infecções parecem estar apenas minimamente aumentadas com o uso de rituximab.10 Um grupo de risco é o de portadores crônicos do vírus da hepatite B, que pode experimentar uma reativação do vírus que pode ser fatal. Assim, os pacientes que estão a ser considerados para rituximab têm de ser examinados para o estado de portadores do vírus da hepatite B.11 Os pacientes que recebem rituximab correm um risco muito reduzido de leucoencefalopatia multifocal progressiva, o que é mais comum em pacientes com cancro e em pacientes fortemente imunodeprimidos. O risco global é desconhecido, mas é inferior a 1:50.000,