Autoregulação do fluxo sanguíneo cerebral
Autoregulação do fluxo sanguíneo cerebral é a capacidade do cérebro de manter um fluxo sanguíneo relativamente constante, apesar das alterações na pressão de perfusão . A auto-regulação está presente em muitos leitos vasculares, mas está particularmente bem desenvolvida no cérebro, provavelmente devido à necessidade de um abastecimento constante de sangue e homeostase de água. Em adultos normotensos, o fluxo sanguíneo cerebral é mantido em ~50 mL por 100 g de tecido cerebral por minuto, desde que o CPP esteja na faixa de ~60 a 160 mmHg . Acima e abaixo deste limite, a auto-regulação é perdida e o fluxo sanguíneo cerebral torna-se dependente da pressão arterial média de uma forma linear. Quando a PPC cai abaixo do limite inferior da auto-regulação, ocorre isquemia cerebral . A redução no fluxo sanguíneo cerebral é compensada por um aumento na extração de oxigênio do sangue . Os sinais ou sintomas clínicos de isquemia não são observados até que a diminuição da perfusão exceda a capacidade de aumento da extração de oxigênio para atender às necessidades metabólicas. Neste ponto, sinais clínicos de hipoperfusão ocorrem, incluindo tonturas, alteração do estado mental e eventualmente danos irreversíveis nos tecidos (infarto) .
Os mecanismos de auto-regulação no cérebro não são completamente compreendidos e provavelmente diferem com aumentos vs. diminuições na pressão. Embora o papel do envolvimento neuronal na autorregulação seja atraente, estudos têm mostrado que a autorregulação do fluxo sanguíneo cerebral é preservada em animais simpaticamente e parassimpateticamente desnervados, indicando que uma contribuição importante de fatores neurogênicos extrínsecos para a autorregulação do fluxo sanguíneo cerebral é improvável (ver Inervação Perivascular). Recentemente, foi demonstrado um papel do óxido nítrico neuronal na auto-regulação da modulação do fluxo sanguíneo cerebral, sugerindo que embora a inervação extrínseca possa não estar envolvida, a inervação intrínseca pode ter um papel. Biprodutos do metabolismo também têm sido propostos para ter um papel na autoregulação. Reduções no fluxo sanguíneo cerebral estimulam a libertação de substâncias vasoactivas do cérebro que causam a dilatação arterial. Os candidatos para estas substâncias vasoactivas incluem H+, K+, O2, adenosina, e outros. A autorregulação do fluxo sanguíneo cerebral quando a pressão flutua no extremo alto da curva autorregulatória é mais provável devido ao comportamento miogênico do músculo liso cerebral que se contrai em resposta à pressão elevada e se dilata em resposta à diminuição da pressão . A importante contribuição da atividade miogênica para a autorregulação é demonstrada in vitro em artérias cerebrais isoladas e pressurizadas que se contraem em resposta ao aumento da pressão e se dilatam em resposta à diminuição da pressão (ver Resposta Miogênica). A autorregulação em pressões abaixo da faixa de pressão miogênica provavelmente envolve hipoxia e liberação de fatores metabólicos .
A importância da autorregulação na função cerebral normal é realçada pelo fato de que um dano cerebral significativo ocorre quando os mecanismos autorregulatórios são perdidos. Por exemplo, durante a hipertensão aguda a pressões acima do limite autorregulatório, a constrição miogênica do músculo liso vascular é superada pela pressão intravascular excessiva e ocorre a dilatação forçada dos vasos cerebrais. A perda do tônus miogênico durante a dilatação forçada diminui a resistência cerebrovascular, um resultado que pode produzir um grande aumento no fluxo sanguíneo cerebral (300-400%), conhecido como auto-regulatório (Figura 16). Além disso, a diminuição da resistência cerebrovascular aumenta a pressão hidrostática no endotélio cerebral, causando a formação de edema, causa subjacente de condições como encefalopatia hipertensiva, síndrome da encefalopatia reversível posterior (PRES) e eclâmpsia (ver Formação de Edema Vasogênico).
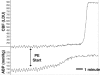
FIGURA 16
Traçado de CBF (em unidades Doppler a laser) e ABP (em mmHg) em resposta a doses crescentes de EP. Neste experimento, o CBF aumentou quatro vezes maior que a linha de base, pois o ABP aumentou de 140 para 210 mmHg, demonstrando um avanço autorregulatório. Utilizado (mais…)
Embora incomum desde o advento da terapia anti-hipertensiva eficaz, a encefalopatia hipertensiva ocorre como resultado de um aumento súbito e sustentado da pressão arterial suficiente para exceder o limite superior da autorregulação do fluxo sanguíneo cerebral (>160 mmHg) . Estudos iniciais sobre a reação dos vasos cerebrais à pressão arterial elevada produziram o conceito de vasoespasmo hipertensivo. Pensou-se que a encefalopatia hipertensiva aguda era o resultado de espasmo – definido como uma vasoconstrição descontrolada – das artérias cerebrais, causando isquemia do tecido cerebral. Este conceito teve origem nas observações de Byrom que produziu hipertensão renal experimental e encontrou ~90% dos ratos hipertensos com manifestações neurológicas apresentaram múltiplas manchas corticais de extravasamento do azul tripano, enquanto que os ratos sem sintomas cerebrais pareciam ter permeabilidade cerebrovascular normal. Ele também observou o que chamou de vasoconstrição/vasodilatação alternada nos vasos piais, um fenômeno conhecido como “sausage-string”. Esta observação levou-o a concluir que o vasoespasmo cerebral causou isquemia e formação de edema em resposta à hipertensão aguda. Byrom mais tarde modificou sua visão e se referiu a um achado na circulação mesentérica que vasos com essa aparência de “sausage-string” tinham vazamento de proteína apenas nas partes dilatadas dos vasos . Desde então, foi estabelecido que a pressão alta resulta em aumento do fluxo sanguíneo cerebral e “ruptura da auto-regulação” . Outras experiências confirmaram que a perda de vasoconstrição miogênica durante a dilatação forçada em vez de espasmo é o evento crítico na encefalopatia hipertensiva .