Nome genérico: poliestireno sulfonato de sódio
Forma de dosagem: suspensão oral / retal
Revisado medicamente por Drugs.com. Última atualização em 22 de julho de 2020.
- Visão geral
- Efeitos secundários
- Dosagem
- Profissional
- Interacções
- Mais
- Indicações e Uso do Kionex
- Dose e administração do Kionex
- Informações gerais
- Dose recomendada
- Preparação e Administração
- Dosagem Formas e Forças
- Contraindicações
- Avisos e Precauções
- Necrose intestinal
- Perturbações eletrolíticas
- Sobrecarga de fluidos em pacientes sensíveis a alta ingestão de sódio
- Risco de aspiração
- Aglutinação a outros medicamentos administrados oralmente
- Reações adversas
- Interações com drogas
- Interações gerais
- Antacidas donativos de catiões
- Sorbitol
- UTILIZAÇÃO EM POPULAÇÕES ESPECÍFICAS
- Pregnância
- Lactação
- Uso pediátrico
- Overdosagem
- Kionex Descrição
- Kionex – Farmacologia Clínica
- Mecanismo de Ação
- Farmacodinâmica
- Farmacocinética
- Nonclinical Toxicology
- Carcinogenesis, Mutagenesis, Impairment of Fertility
- Como Fornecido/Armazenamento e Manuseio
- Informação de Aconselhamento Paciente
- PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
- Mais sobre Kionex (poliestireno sulfonato de sódio)
- Recursos do consumidor
- Recursos profissionais
- Guias de tratamento relacionadas
Indicações e Uso do Kionex
Kionexis indicado para o tratamento da hipercalemia.
Limitação de uso:
Kionex não deve ser usado como tratamento de emergência para hipercalemia com risco de vida devido ao seu início retardado de ação .
Dose e administração do Kionex
Informações gerais
Administer Kionex pelo menos 3 horas antes ou 3 horas depois de outros medicamentos orais. Pacientes com gastroparese podem requerer uma separação de 6 horas
Dose recomendada
A intensidade e a duração da terapia dependem da severidade e resistência da hipercalemia.
Oral
A dose média diária total de Kionex para adultos é de 15 g a 60 g, administrada em doses de 15 g (quatro colheres de chá), uma a quatro vezes ao dia.
Rectal
A dose média para adultos é de 30 g a 50 g a cada seis horas.
Preparação e Administração
Preparar a suspensão fresca e usar em 24 horas.
Não aquecer o Kionex, pois poderia alterar as propriedades de troca da resina.
Uma colher de chá de nível contém aproximadamente 3,5 g de Kionex e 15 mEq de sódio.
Suspensão oral
Suspender cada dose numa pequena quantidade de água ou xarope, aproximadamente 3 a 4 mL de líquido por grama de resina. Administrar com paciente em uma posição ereta .
Enema
Após um clister inicial de limpeza, inserir um tubo de borracha macio, grande tamanho (francês 28) no reto por uma distância de cerca de 20 cm, com a ponta bem no cólon sigmóide, e fita adesiva no lugar.
Administer como uma emulsão quente (temperatura corporal) em 100 mL de veículo aquoso e enxaguar com 50 a 100 ml de líquido. Uma suspensão um pouco mais espessa pode ser usada, mas não forma uma pasta.
Agitar a emulsão suavemente durante a administração. A resina deve ser retida o máximo de tempo possível e seguida por um clister de limpeza com uma solução não-sódica. Certifique-se de que é utilizado um volume adequado de solução de limpeza (até 2 litros).
Dosagem Formas e Forças
Kionex é um creme a castanho claro, pó finamente moído e está disponível em frascos de 454 g.
Contraindicações
Kionex está contra-indicado em pacientes com as seguintes condições:
– Hipersensibilidade a resinas de poliestireno sulfonato – Doença obstrutiva intestinal – Neonatos com mobilidade intestinal reduzida
Avisos e Precauções
Necrose intestinal
Casos de necrose intestinal, alguns fatais, e outros eventos adversos gastrointestinais graves (sangramento, colite isquémica, perfuração) foram relatados em associação com o uso de Kionex. A maioria destes casos relatou o uso concomitante de sorbitol. Fatores de risco para eventos adversos gastrointestinais estavam presentes em muitos dos casos, incluindo prematuridade, história de doença ou cirurgia intestinal, hipovolemia e insuficiência e falência renal. A administração concomitante de sorbitol não é recomendada.
– Usar somente em pacientes que tenham função intestinal normal. Evitar o uso em pacientes que não tiveram uma evacuação intestinal após a cirurgia. – Evite o uso em pacientes com risco de desenvolver constipação ou impacção (incluindo aqueles com história de impacção, constipação crónica, doença inflamatória intestinal, colite isquémica, aterosclerose intestinal vascular, ressecção intestinal prévia ou obstrução intestinal). Interromper o uso em pacientes que desenvolvem constipação intestinal.
Perturbações eletrolíticas
Monitoramento sérico de potássio durante a terapia, pois pode ocorrer hipocalemia grave.
Kionex não é totalmente seletivo para potássio, e pequenas quantidades de outros cátions, como magnésio e cálcio, também podem ser perdidas durante o tratamento. Monitorar cálcio e magnésio em pacientes que recebem Kionex.
Sobrecarga de fluidos em pacientes sensíveis a alta ingestão de sódio
A cada 15 g de Kionex contém 1500 mg (60 mEq) de sódio. Monitore pacientes sensíveis à ingestão de sódio (insuficiência cardíaca, hipertensão, edema) para sinais de sobrecarga de líquidos. O ajuste de outras fontes de sódio pode ser necessário.
Risco de aspiração
Caso de bronquite aguda ou broncopneumonia causada pela inalação de partículas de poliestireno sulfonato de sódio foram relatados. Pacientes com reflexo de mordaça prejudicado, nível de consciência alterado ou pacientes propensos a regurgitação podem estar em risco aumentado. Administre Kionex com o paciente em posição vertical.
Aglutinação a outros medicamentos administrados oralmente
Kionex pode aglutinar medicamentos administrados oralmente, o que poderia diminuir sua absorção gastrointestinal e levar a uma eficácia reduzida. Administre outros medicamentos orais pelo menos 3 horas antes ou 3 horas depois do Kionex. Pacientes com gastroparese podem necessitar de uma separação de 6 horas. .
Reações adversas
As seguintes reações adversas são discutidas em outra parte da rotulagem:
– Necrose intestinal – Perturbações eletrolíticas – Aspiração
As seguintes reações adversas foram identificadas durante o uso pós-aprovação do Kionex. Como essas reações são relatadas voluntariamente de uma população de tamanho incerto, nem sempre é possível estimar sua freqüência de forma confiável ou estabelecer uma relação causal com a exposição a drogas.
Gastrointestinal: anorexia, constipação intestinal, diarréia, impacção fecal, concreções gastrointestinais (bezoares), colite isquémica, náuseas, ulcerações, vómitos, irritação gástrica, obstrução intestinal (devido à concentração de hidróxido de alumínio)
Metabolic: alcalose sistêmica
Interações com drogas
Interações gerais
Não foram realizados estudos formais de interação medicamentosa em humanos.
Kionex tem o potencial de ligar outras drogas. Em estudos de ligação in vitro, foi demonstrado que o Kionex liga significativamente os medicamentos orais (n=6) que foram testados. Diminuição da absorção de lítio e tiroxina também tem sido relatada com a co-administração do Kionex. A ligação do Kionex a outros medicamentos orais poderia causar diminuição da absorção gastrointestinal e perda de eficácia quando tomado próximo ao momento em que o Kionex é administrado. Administrar Kionex pelo menos 3 horas antes ou 3 horas após a administração de outros medicamentos orais. Pacientes com gastroparese podem necessitar de uma separação de 6 horas. Monitor para resposta clínica e/ou níveis sanguíneos onde possível.
Antacidas donativos de catiões
A administração oral simultânea de Kionex com antiácidos e laxantes não absorvíveis de catiões pode reduzir a capacidade de troca de potássio da resina e aumentar o risco de alcalose sistémica.
Sorbitol
Sorbitol pode contribuir para o risco de necrose intestinal e o uso concomitante não é recomendado.
UTILIZAÇÃO EM POPULAÇÕES ESPECÍFICAS
Pregnância
Resumo do risco
Kionex não é absorvido sistemicamente após administração oral ou retal e não é esperado que o uso materno resulte em risco fetal.
Lactação
Resumo do risco
Kionex não é absorvido sistemicamente pela mãe, portanto não se espera que a amamentação resulte em risco para o bebê.
Uso pediátrico
Estudos de segurança e eficácia não foram realizados em pacientes pediátricos.
Em pacientes pediátricos, como em adultos, espera-se que o Kionex ligue o potássio na proporção prática de troca de 1mEq de potássio por 1 grama de resina.
Em recém-nascidos, o Kionex não deve ser administrado por via oral. Tanto em crianças como em recém-nascidos, uma dosagem excessiva ou uma diluição inadequada pode resultar em impacção da resina. Bebês prematuros ou bebês de baixo peso ao nascer podem ter um risco aumentado de efeitos adversos gastrointestinais com Kionex. uso .
Overdosagem
Overdosagem pode resultar em distúrbios eletrolíticos incluindo hipocalemia, hipocalcemia e hipomagnesemia. Devem ser tomadas medidas apropriadas para corrigir os eletrólitos séricos (potássio, cálcio, magnésio), e a resina deve ser removida do trato alimentar pelo uso apropriado de laxantes ou enemas.
Kionex Descrição
Kionex é um benzeno, dietenil-polímero, com etenil-benzeno, sulfonado, sal sódico e tem a seguinte fórmula estrutural:
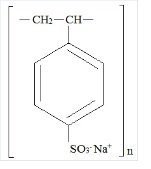
O medicamento é um creme de poliestireno sulfonato de sódio finamente moído a castanho claro, uma resina de permuta catiónica preparada na fase sódica com uma capacidade de permuta in vitro de aproximadamente 3.1 mEq (in vivo aproximadamente 1 mEq) de potássio por grama. O conteúdo de sódio é de aproximadamente 100 mg (4,1 mEq) por grama do fármaco. Pode ser administrado oralmente ou retalmente como um enema.
Um grama de Kionex contém 4,1 mEq de sódio.
Kionex – Farmacologia Clínica
Mecanismo de Ação
Kionex é um polímero de troca catiônica não-absorvível que contém um counterion de sódio.
Kionex aumenta a excreção fecal de potássio através da ligação do potássio no lúmen do trato gastrointestinal. A ligação do potássio reduz a concentração de potássio livre na luz do trato gastrointestinal, resultando numa redução dos níveis séricos de potássio. A relação de troca prática é de 1 mEq K por 1 grama de resina.
Como a resina passa ao longo do intestino ou é retida no cólon após a administração por enema, os íons sódio são parcialmente liberados e são substituídos por íons potássio. Esta ação ocorre principalmente no intestino grosso, que excreta íons de potássio em maior grau do que o intestino delgado. A eficiência deste processo é limitada e imprevisivelmente variável.
Farmacodinâmica
A redução efetiva do potássio sérico com Kionex pode levar horas a dias.
Farmacocinética
A eficiência in vivo das resinas de troca sódio-potássio é de aproximadamente 33%; portanto, cerca de um terço do conteúdo real de sódio da resina é entregue ao organismo.
Kionex não é absorvido sistemicamente.
Interacções de Drogas
Estudos de ligação in vitro mostraram que o Kionex ligado significativamente às seguintes drogas testadas – warfarina, metoprolol, fenitoína, furosemida, amlodipina e amoxicilina.
Nonclinical Toxicology
Carcinogenesis, Mutagenesis, Impairment of Fertility
Estudos não foram realizados.
Como Fornecido/Armazenamento e Manuseio
Kionex está disponível como um creme para castanho claro, pó finamente moído em frascos de 1 libra (454 g), NDC 0574-2004-16.
Store at 20° to 25°C (68° to 77°F) .
Informação de Aconselhamento Paciente
Interacções com Drogas
Aconselhar pacientes que estejam a tomar outros medicamentos orais para separar a dosagem de Kionex por pelo menos 3 horas (antes ou depois)
Apenas Rx
Empacotado por
Perrigo
Minneapolis, MN 55427
Revisado 08/2017
PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
Rx Apenas
NDC 0574-2004-16
Kionex®
Sulfonato de Poliestireno de Sódio para Suspensão
DOSE ADULTADORA AVERADA: 15 g (aproximadamente 4 colheres de chá de nível) uma a quatro vezes por dia em água. Ver informação completa da prescrição.
O efeito deve ser cuidadosamente controlado através de determinações frequentes de soro de potássio dentro de cada período de 24 horas. O teor de sódio deve ser aproximadamente 60 mEq por 15 g.
Suspensão deve ser preparada de fresco e não deve ser armazenada para além de 24 horas. Dispensar em recipientes herméticos e resistentes à luz, conforme definido na USP.
Suspensão: Armazenar a 20° a 25°C (68° a 77°F) .
Ler o folheto informativo.
454 gramas (1 LB)
| Kionex sulfonato de poliestireno de sódio em pó, para suspensão |
||||||||||||||||||
|
||||||||||||||||||
| >
>
|
||||||||||||||||||
> |
||||||||||||||||||
>
|
||||||||||||||||||
> |
||||||||||||||||||
>
>
Etiquetador – Laboratórios Paddock, LLC (967694121)
Mais sobre Kionex (poliestireno sulfonato de sódio)
- Efeitos secundários
- Durante a gravidez ou amamentação
- Informações sobre a dosagem
- Interacções com o Dragão
- En Español
- 4 Revisões
- Classe do Dragão: resinas de troca catiónica
- Alertas FDA (2)
Recursos do consumidor
- Informação do paciente
- Kionex (Leitura avançada)
Recursos profissionais
- Informações sobre a impressão
- Solfonato de poliestireno de sódio em pó oral (FDA)
Outras marcas Kayexalate, Kalexate
Guias de tratamento relacionadas
- Hipercalemia
Relatação de responsabilidade médica