Generický název: polystyren sulfonát sodný
Dávkovací forma: perorální / rektální suspenze
Medicínská recenze: Drugs.com. Naposledy aktualizováno 22. července 2020.
- Přehled
- Nežádoucí účinky
- Dávkování
- Odborné
- Interakce
- Další
- Indikace a použití přípravku Kionex
- Dávkování a způsob podání přípravku Kionex
- Všeobecné informace
- Doporučené dávkování
- Příprava a podání
- Dávkovací formy a síly
- Kontraindikace
- Upozornění a opatření
- Střevní nekróza
- Elektrolytové poruchy
- Přetížení tekutinami u pacientů citlivých na vysoký příjem sodíku
- Riziko aspirace
- Vazba na jiné perorálně podávané léky
- Nežádoucí účinky
- Lékové interakce
- Všeobecné interakce
- Kationt-donující antacida
- Sorbitol
- POUŽITÍ U ZVLÁŠTNÍCH POPULACÍ
- Těhotenství
- Kojení
- Pediatrické použití
- Předávkování
- Kionex Popis přípravku
- Kionex – klinická farmakologie
- Mechanismus účinku
- Farmakodynamika
- Farmakokinetika
- Neklinická toxikologie
- Karcinogeneze, mutageneze, poškození fertility
- Jak se přípravek dodává/Skladování a zacházení s ním
- Informace pro pacienty
- OBAL/ŠTÍTEK PRVNÍHO OBALU
- Více o přípravku Kionex (polystyren-sulfonát sodný)
- Zdroje pro spotřebitele
- Zdroje pro odborníky
- Související léčebné příručky
Indikace a použití přípravku Kionex
Kionexis indikován k léčbě hyperkalémie.
Omezení použití:
Kionex by neměl být používán jako nouzová léčba život ohrožující hyperkalémie, protože má opožděný nástup účinku .
Dávkování a způsob podání přípravku Kionex
Všeobecné informace
Přípravek Kionex podávejte nejméně 3 hodiny před nebo 3 hodiny po podání jiných perorálních léků. Pacienti s gastroparézou mohou vyžadovat odstup 6 hodin
Doporučené dávkování
Intenzita a délka léčby závisí na závažnosti a rezistenci hyperkalémie.
Orální
Průměrná celková denní dávka přípravku Kionex pro dospělé je 15 g až 60 g, podávaná jako 15g dávka (čtyři rovné čajové lžičky), jedenkrát až čtyřikrát denně.
Rektální
Průměrná dávka pro dospělé je 30 g až 50 g každých šest hodin.
Příprava a podání
Suspenzi připravujte čerstvou a spotřebujte ji do 24 hodin.
Přípravek Kionex nezahřívejte, protože by to mohlo změnit výměnné vlastnosti pryskyřice.
Jedna zarovnaná čajová lžička obsahuje přibližně 3,5 g přípravku Kionex a 15 mEq sodíku.
Orální suspenze
Každou dávku rozpusťte v malém množství vody nebo sirupu, přibližně 3 až 4 ml tekutiny na gram pryskyřice. Podávejte pacientovi ve vzpřímené poloze .
Klyzma
Po úvodním očistném klyzmatu zaveďte měkkou gumovou hadičku velkého rozměru (French 28) do konečníku na vzdálenost asi 20 cm, špičkou dobře do esovitého tračníku, a zalepte páskou.
Podávejte jako teplou (tělesná teplota) emulzi ve 100 ml vodného nosiče a propláchněte 50 až 100 ml tekutiny. Lze použít poněkud hustší suspenzi, ale nevytvářejte pastu.
Emulzi během podávání jemně roztírejte. Pryskyřici je třeba ponechat co nejdéle a následně provést očistné klyzma roztokem neobsahujícím sodík. Zajistěte, aby byl využit dostatečný objem očistného roztoku (až 2 litry).
Dávkovací formy a síly
Kionex je krémový až světle hnědý, jemně mletý prášek a je k dispozici ve 454 g nádobkách.
Kontraindikace
Kionex je kontraindikován u pacientů s následujícími stavy:
– Přecitlivělost na polystyren-sulfonátové pryskyřice – Obstrukční střevní onemocnění – Novorozenci se sníženou motilitou střev
Upozornění a opatření
Střevní nekróza
V souvislosti s užíváním přípravku Kionex byly hlášeny případy střevní nekrózy, některé fatální, a další závažné gastrointestinální nežádoucí účinky (krvácení, ischemická kolitida, perforace). Ve většině těchto případů bylo hlášeno současné užívání sorbitolu. V mnoha případech byly přítomny rizikové faktory gastrointestinálních nežádoucích účinků, včetně nedonošenosti, střevního onemocnění nebo operace v anamnéze, hypovolemie a renální insuficience a selhání. Současné podávání sorbitolu se nedoporučuje.
– Používejte pouze u pacientů, kteří mají normální funkci střev. Vyhněte se použití u pacientů, kteří neměli stolici po operaci. – Vyhněte se použití u pacientů s rizikem vzniku zácpy nebo impakce (včetně pacientů s anamnézou impakce, chronické zácpy, zánětlivého onemocnění střev, ischemické kolitidy, vaskulární střevní aterosklerózy, předchozí resekce střev nebo střevní obstrukce). U pacientů, u kterých se objeví zácpa, přestaňte přípravek užívat.
Elektrolytové poruchy
Během léčby sledujte sérový draslík, protože může dojít k těžké hypokalémii.
Kionex není zcela selektivní pro draslík a během léčby může dojít i ke ztrátě malého množství jiných kationtů, jako je hořčík a vápník. U pacientů užívajících přípravek Kionex je třeba sledovat obsah vápníku a hořčíku.
Přetížení tekutinami u pacientů citlivých na vysoký příjem sodíku
Každá 15 g dávka přípravku Kionex obsahuje 1500 mg (60 mEq) sodíku. U pacientů citlivých na příjem sodíku (srdeční selhání, hypertenze, otoky) sledujte příznaky přetížení tekutinami. Může být nutná úprava jiných zdrojů sodíku.
Riziko aspirace
Byly hlášeny případy akutní bronchitidy nebo bronchopneumonie způsobené vdechnutím částic polystyren-sulfonátu sodného. Zvýšené riziko mohou mít pacienti s poruchou dávivého reflexu, změněnou úrovní vědomí nebo pacienti se sklonem k regurgitaci. Přípravek Kionex podávejte pacientovi ve vzpřímené poloze.
Vazba na jiné perorálně podávané léky
Kionex může vázat perorálně podávané léky, což může snížit jejich gastrointestinální absorpci a vést ke snížení účinnosti. Ostatní perorální léky podávejte nejméně 3 hodiny před nebo 3 hodiny po podání přípravku Kionex. Pacienti s gastroparézou mohou vyžadovat odstup 6 hodin. .
Nežádoucí účinky
Následující nežádoucí účinky jsou popsány na jiném místě v označení:
– Střevní nekróza – Poruchy elektrolytů – Aspirace
Při poregistračním užívání přípravku Kionex byly zjištěny následující nežádoucí účinky. Vzhledem k tomu, že tyto reakce jsou hlášeny dobrovolně z populace nejisté velikosti, není vždy možné spolehlivě odhadnout jejich četnost nebo stanovit příčinnou souvislost s expozicí léčivu.
Gastrointestinální: anorexie, zácpa, průjem, impakce stolice, gastrointestinální konkrementy (bezoáry), ischemická kolitida, nevolnost, ulcerace, zvracení, podráždění žaludku, střevní obstrukce (v důsledku koncentrace hydroxidu hlinitého)
Metabolické: systémová alkalóza
Lékové interakce
Všeobecné interakce
U lidí nebyly provedeny žádné formální studie lékových interakcí.
Kionex má potenciál vázat jiné léky. Ve vazebných studiích in vitro bylo prokázáno, že přípravek Kionex významně váže perorální léky (n=6), které byly testovány. Při současném podávání přípravku Kionex byla rovněž hlášena snížená absorpce lithia a tyroxinu. Vazba přípravku Kionex na jiné perorální léky by mohla způsobit sníženou gastrointestinální absorpci a ztrátu účinnosti při užívání v blízkosti doby, kdy je podáván přípravek Kionex. Podávejte přípravek Kionex nejméně 3 hodiny před nebo 3 hodiny po podání jiných perorálních léků. Pacienti s gastroparézou mohou vyžadovat odstup 6 hodin. Pokud je to možné, sledujte klinickou odpověď a/nebo hladinu v krvi.
Kationt-donující antacida
Současné perorální podávání přípravku Kionex s nevstřebatelnými kationt-donujícími antacidy a laxativy může snížit schopnost výměny draslíku v pryskyřici a zvýšit riziko systémové alkalózy.
Sorbitol
Sorbitol může přispívat k riziku střevní nekrózy a jeho současné užívání se nedoporučuje.
POUŽITÍ U ZVLÁŠTNÍCH POPULACÍ
Těhotenství
Shrnutí rizik
Kionex se po perorálním nebo rektálním podání systémově neabsorbuje a neočekává se, že by užívání u matky vedlo k ohrožení plodu.
Kojení
Souhrn rizik
Kionex není matkou systémově absorbován, takže se neočekává, že by kojení vedlo k riziku pro kojence.
Pediatrické použití
Studie bezpečnosti a účinnosti nebyly u pediatrických pacientů provedeny.
U pediatrických pacientů se stejně jako u dospělých očekává, že Kionex bude vázat draslík v praktickém výměnném poměru 1mEq draslíku na 1 g pryskyřice.
U novorozenců by Kionex neměl být podáván perorální cestou. U dětí i novorozenců by nadměrné dávkování nebo nedostatečné ředění mohlo vést k impakci pryskyřice. U předčasně narozených dětí nebo dětí s nízkou porodní hmotností může být zvýšené riziko gastrointestinálních nežádoucích účinků přípravku Kionex. použití .
Předávkování
Předávkování může vést k poruchám elektrolytů včetně hypokalémie, hypokalcémie a hypomagnezémie. Měla by být přijata vhodná opatření ke korekci sérových elektrolytů (draslík, vápník, hořčík) a pryskyřice by měla být odstraněna ze zažívacího traktu vhodným použitím laxativ nebo klystýru.
Kionex Popis přípravku
Kionex je benzen, diethenyl-polymer, s etenylbenzenem, sulfonovaná, sodná sůl a má následující strukturní vzorec:
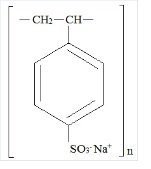
Přípravek je krémová až světle hnědá jemně mletá, prášková forma polystyren-sulfonátu sodného, kationtové výměnné pryskyřice připravené v sodné fázi s výměnnou kapacitou in vitro přibližně 3. Výměnná kapacita kationtové pryskyřice je 1,5 %.1 mEq (in vivo přibližně 1 mEq) draslíku na gram. Obsah sodíku je přibližně 100 mg (4,1 mEq) na gram léčiva. Lze jej podávat perorálně nebo rektálně jako klyzma.
Jeden gram přípravku Kionex obsahuje 4,1 mEq sodíku.
Kionex – klinická farmakologie
Mechanismus účinku
Kionex je neabsorbovaný kationtový výměnný polymer, který obsahuje sodíkový protiiont.
Kionex zvyšuje vylučování draslíku stolicí prostřednictvím vazby draslíku v lumen gastrointestinálního traktu. Vazba draslíku snižuje koncentraci volného draslíku v lumen gastrointestinálního traktu, což vede ke snížení sérové hladiny draslíku. Praktický výměnný poměr je 1 mEq K na 1 gram pryskyřice.
Při průchodu pryskyřice střevem nebo při jejím zadržování v tlustém střevě po podání klyzmatem se ionty sodíku částečně uvolňují a jsou nahrazovány ionty draslíku. K tomuto působení dochází především v tlustém střevě, které vylučuje draselné ionty ve větší míře než tenké střevo. Účinnost tohoto procesu je omezená a nepředvídatelně proměnlivá.
Farmakodynamika
Účinné snížení sérového draslíku přípravkem Kionex může trvat hodiny až dny.
Farmakokinetika
Účinnost in vivo výměnných pryskyřic pro sodík a draslík je přibližně 33 %; do těla se tedy dostane přibližně jedna třetina skutečného obsahu sodíku v pryskyřici.
Kionex se systémově nevstřebává.
Lékové interakce
Vazbové studie in vitro ukázaly, že se Kionex významně váže na následující testovaná léčiva – warfarin, metoprolol, fenytoin, furosemid, amlodipin a amoxicilin.
Neklinická toxikologie
Karcinogeneze, mutageneze, poškození fertility
Studie nebyly provedeny.
Jak se přípravek dodává/Skladování a zacházení s ním
Kionex je dostupný jako krémový až světle hnědý, jemně mletý prášek ve sklenicích po 1 libře (454 g), NDC 0574-2004-16.
Skladujte při teplotě 20° až 25°C .
Informace pro pacienty
Lékové interakce
Poradit pacientům, kteří užívají jiné perorální léky, aby oddělili dávkování přípravku Kionex nejméně o 3 hodiny (před nebo po)
Pouze na lékařský předpis
Balí
Perrigo
Minneapolis, MN 55427
Revidováno 08/2017
OBAL/ŠTÍTEK PRVNÍHO OBALU
Pouze na lékařský předpis
NDC 0574-2004-16
Kionex®
Polystyren-sulfonát sodný pro suspenzi
Dávkování pro dospělé: 15 g (přibližně 4 vrchovaté čajové lžičky) jedenkrát až čtyřikrát denně ve vodě. Viz úplná preskripční informace.
Účinek musí být pečlivě kontrolován častým stanovením draslíku v séru během každých 24 hodin. Obsah sodíku přibližně 60 mEq na 15 g.
Suspenze by měla být čerstvě připravená a neměla by být skladována déle než 24 hodin. Dávkujte v těsných, světlu odolných obalech, jak je definováno v USP.
SKLADOVÁNÍ:
Přečtěte si příbalovou informaci.
454 g (1 LB)
| Kionex sodium polystyren sulfonate powder, pro suspenzi |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Označovač – Padesát laboratoří, LLC (967694121)
Více o přípravku Kionex (polystyren-sulfonát sodný)
- Nežádoucí účinky
- Při těhotenství nebo kojení
- Informace o dávkování
- Lékové interakce
- En Español
- 4 recenze
- Třída léčivých přípravků:
- Upozornění FDA (2)
Zdroje pro spotřebitele
- Informace pro pacienty
- Kionex (Pokročilé čtení)
.
Zdroje pro odborníky
- Informace o předepisování
- Polystyren sulfát sodný v perorálním prášku (FDA)
Další značky Kayexalate, Kalexate
Související léčebné příručky
- Hyperkalémie
Vyjádření lékařské odpovědnosti