Níže uvedené tabulky a obrázky ukazují, jak se mění teplota tání s rostoucím počtem uhlíků až do C33 pro různé druhy uhlovodíků, alkoholů a karboxylových kyselin. Podrobnější definice a příklady molekulových struktur různých tříd organických sloučenin jsou uvedeny pod obrázky.
- Teplota tání – teplota, při které se pevná látka mění v kapalinu
- Teplota varu – teplota, při které se kapalina mění v plyn
Pro uhlovodíky se stejným počtem uhlíku se teplota varu zvyšuje v následujícím pořadí:
multisubstituovaný alkan <jednosubstituovaný alkan <jednosubstituovaný alken < normální alken < normální alkan < alkylcyklohexan < alkylbenzen < cykloalken < cykloalkan < 2-, 4- a 3-alkanol / 1-alkylnaftalen < 1-alkanol < normální alkanová kyselina
U teplot tání se trendy s rostoucím počtem uhlíků u různých typů uhlovodíků více mění.
Podívejte se také na body varu uhlovodíků, alkoholů a kyselin, hustoty pro různé druhy organických sloučenin a hustoty, body varu a tání sloučenin dusíku a síry.
Viz také hodnoty pKa pro fenoly, alkoholy a karboxylové kyseliny.
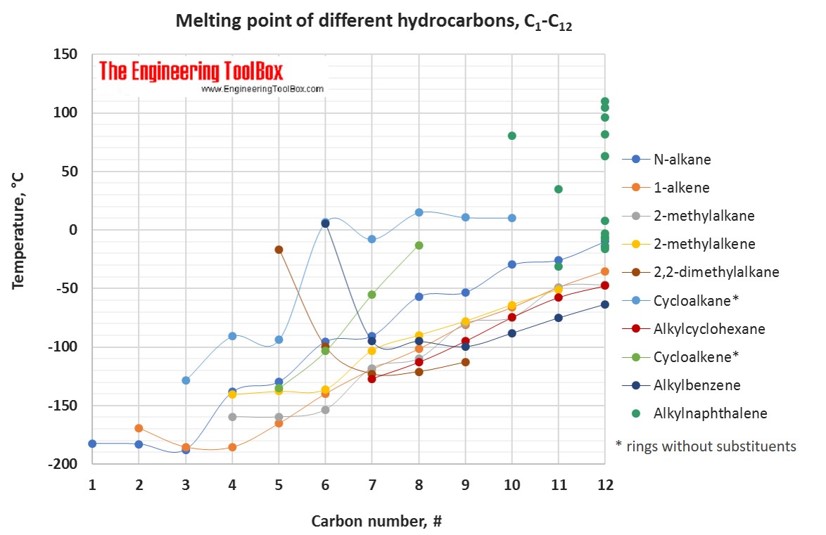
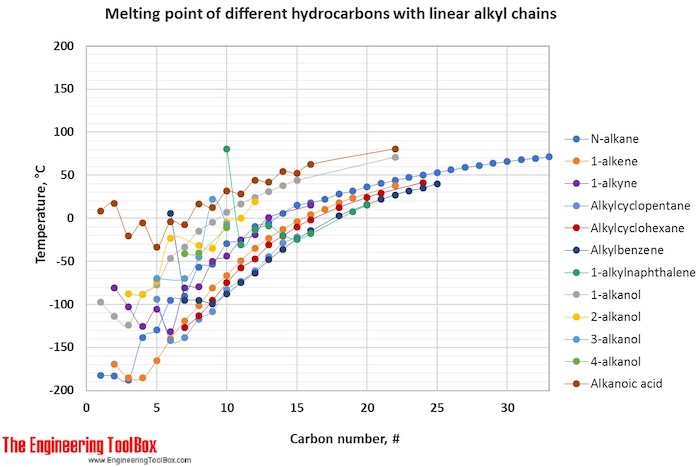
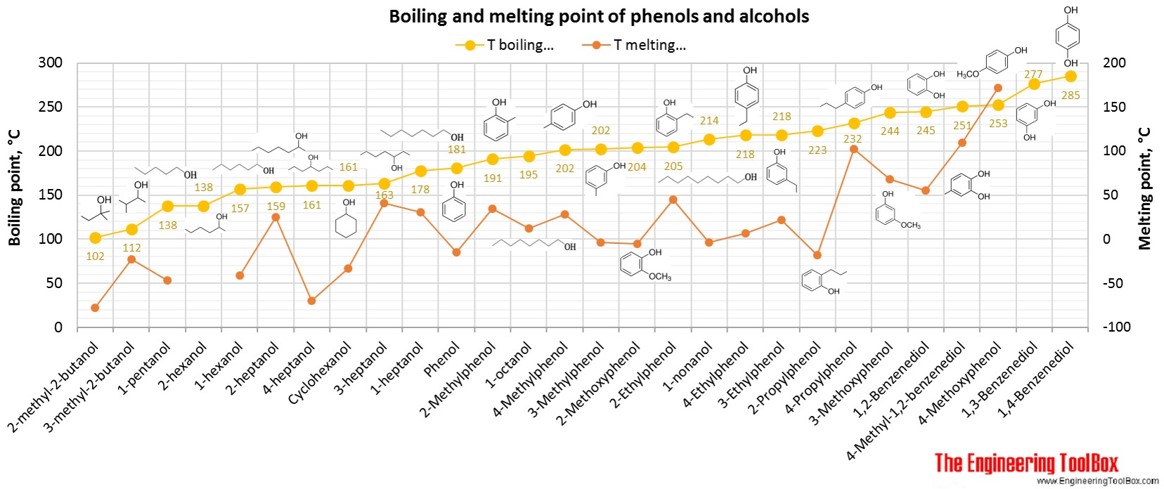
Pro celou tabulku – otočte obrazovku!
| Teplota tání uhlovodíků, alkoholů a kyselin, C1-C16, udávaný ve °C | |||||||||||||||||
| Číslo uhlíku | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | |
| Alkylcyklohexan* | -127 | -113 | -95 | -78 | -58 | -48 | -31 | -20 | -10 | -2 | |||||||
| 2,2-dimetylalkan | -17 | -100 | -123 | -121 | -113 | ||||||||||||
| 3-methylalkan | -118 | -119 | -121 | -108 | -85 | -80 | -58 | ||||||||||
| Alkylbenzen* | 6 | -95 | -95 | -100 | -88 | -75 | -63 | -48 | -36 | -24 | -14 | ||||||
| Alkylcyklopentan | -142 | -138 | -117 | -108 | -83 | -73 | -61 | -45 | -29 | -22 | |||||||
| 2-methylalkan | -160 | -160 | -154 | -118 | -110 | -80 | -75 | -49 | -47 | ||||||||
| 1-alken | -169 | -185 | -185 | -165 | -140 | -119 | -102 | -81 | -66 | -49 | -35 | -23 | -13 | -4 | |||
| 2-methylalken | -140 | -138 | -136 | -103 | -90 | -78 | -64 | -51 | |||||||||
| N-alkan | -183 | -183 | -188 | -138 | -130 | -95 | -91 | -57 | -53 | -30 | -26 | -10 | |||||
| 1-alkyn | -81 | -103 | -126 | -106 | -132 | -81 | -79 | -50 | -44 | -25 | -19 | 1 | 15 | ||||
| 3-alkanol | -70 | -70 | -45 | 22 | -8 | ||||||||||||
| Cykloalken** | -135 | -104 | -55 | ||||||||||||||
| 4-alkanol | -41 | -41 | -11 | ||||||||||||||
| 2-alkanol | -88 | -88 | -73 | -23 | -32 | -35 | -5 | 0 | 19 | ||||||||
| 1-alkanol | -98 | -114 | -124 | -89 | -78 | -46 | -33 | -15 | -5 | 7 | 17 | 24 | 31 | 38 | 44 | ||
| Cykloalkan** | -129 | -91 | -94 | 7 | -8 | 15 | 11 | 10 | |||||||||
| Kyselina alkanová | 8 | 17 | -21 | -5 | -34 | -4 | -7 | 17 | 12 | 31 | 29 | 44 | 42 | 63 | |||
| 1-alkylnaftalen | 80 | -31 | -14 | -9 | -20 | -25 | -18 | ||||||||||
| Teplota tání uhlovodíků, alkoholů a kyselin C1-C16, udávaný v °F | |||||||||||||||||
| Číslo uhlíku | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | |
| Alkylcyklohexan* | -197 | -171 | -139 | -108 | -72 | -54 | -24 | -5 | 14 | 29 | |||||||
| 2,2-dimetylalkan | 2 | -148 | -189 | -186 | -171 | ||||||||||||
| 3-methylalkan | -180 | -182 | -186 | -162 | -121 | -112 | -72 | ||||||||||
| Alkylbenzen* | 42 | -139 | -139 | -147 | -126 | -103 | -82 | -54 | -33 | -11 | 6 | ||||||
| Alkylcyklopentan | -224 | -217 | -179 | -162 | -117 | -99 | -78 | -48 | -20 | -8 | |||||||
| 2-methylalkan | -255 | -256 | -245 | -180 | -166 | -112 | -103 | -56 | -53 | ||||||||
| 1-alken | -273 | -302 | -302 | -265 | -220 | -182 | -151 | -114 | -87 | -56 | -31 | -10 | 9 | 25 | 40 | ||
| 2-methylalken | -221 | -216 | -213 | -153 | -130 | -108 | -83 | -60 | |||||||||
| N-alkan | -297 | -297 | -306 | -217 | -201 | -140 | -131 | -70 | -64 | -21 | -14 | 15 | |||||
| 1-alkyn | -113 | -153 | -194 | -158 | -205 | -114 | -111 | -58 | -47 | -13 | -2 | 34 | 59 | ||||
| 3-alkanol | -94 | -94 | -49 | 72 | 19 | ||||||||||||
| Cykloalken** | -211 | -154 | -67 | ||||||||||||||
| 4-alkanol | -42 | -41 | 12 | ||||||||||||||
| 2-alkanol | -126 | -127 | -99 | -9 | -25 | -31 | 23 | 32 | 66 | ||||||||
| 1-alkanol | -144 | -173 | -192 | -127 | -108 | -52 | -28 | 6 | 23 | 45 | 62 | 76 | 88 | 100 | 111 | ||
| Cykloalkan** | -199 | -131 | -137 | 44 | 18 | 59 | 51 | 51 | |||||||||
| Kyselina alkanová | 47 | 63 | -5 | 23 | -28 | 25 | 19 | 62 | 54 | 89 | 83 | 111 | 107 | 145 | |||
| 1-alkylnaftalen | 177 | -24 | 7 | 17 | -3 | -12 | 0 | ||||||||||
| * C#(N-alkyl)=0-10 | |||||||||||||||||
| ** kruhy bez substituentů | |||||||||||||||||
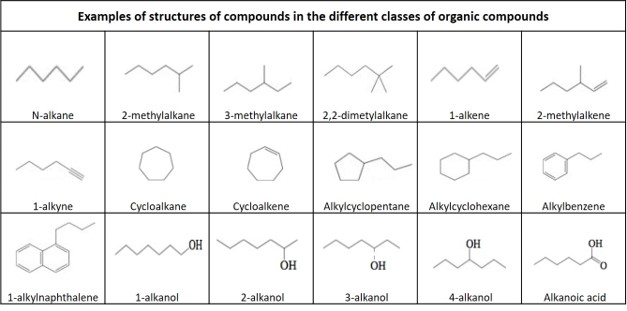
Definice organických sloučenin
Vodík:
Hlavní skupiny uhlovodíků:
Alkan: Acyklický nasycený uhlovodík s obecným vzorcem CnH2n+2. Nazývá se také parafín.
Alken: Je to nenasycený uhlovodík, který obsahuje alespoň jednu dvojnou vazbu uhlík-uhlík, s obecným vzorcem CnH2n. Nazývá se také olefin.
Alkyn: Nenasycený uhlovodík obsahující alespoň jednu trojnou vazbu uhlík-uhlík, s obecným vzorcem CnH2n-2. Nazývá se také acetylen.
Cykloalkan: Jednokruhový (monocyklický) nasycený uhlovodík s obecným vzorcem CnH2n. Nazývá se také naften.
Cykloalken: Uhlovodík alken, který obsahuje uzavřený kruh atomů uhlíku, ale nemá aromatický charakter, s obecným vzorcem CnH2n-2. Nazývá se také cykloolefin.
Aromatický uhlovodík: Cyklická (prstencová), planární (plochá) molekula s prstencem rezonančních vazeb, která vykazuje větší stabilitu než jiná geometrická nebo vazbová uspořádání se stejným souborem atomů. Nejjednodušší z aromatických sloučenin mají 6 atomů uhlíku a obsahují 3 dvojné vazby. Jednookruhový aromat se bez substituentů nazývá benzen se vzorcem C6H6.
Polycyklické aromatické uhlovodíky: uhlovodíky, které jsou složeny z více aromatických kruhů. Dvoukroužkový aromatický uhlovodík bez jakýchkoli substituentů se nazývá naftalen, se vzorcem C10H8.
Některé podskupiny uhlovodíků uvedené v tomto dokumentu:
Alkyl:
2-Methylalkan: Rozvětvený alkan s methylovou skupinou připojenou k druhému atomu uhlíku v hlavním uhlíkovém řetězci.
3-Methylalkan: Rozvětvený alkan s methylovou skupinou připojenou k třetímu atomu uhlíku v hlavním uhlíkovém řetězci.
2-Methylalken:
Alkylcyklohexan:
Alkylcyklopentan: Monosubstituovaný cyklohexan s jedním větvením připojením jedné alkylové skupiny na jeden uhlík cyklohexanového kruhu, s obecným vzorcem CnH(2n+1)C6H11.
Alkylcyklopentan: A monosubstitued cyclopentane with one branching via attachment of one alkyl group on one carbon of the cyclohexane ring, with a general formula CnH2n+1C5H9.
Alkylbenzen:
Alkylnaftalen: Monosubstituovaný benzen s jednou větví připojením jedné alkylové skupiny na jeden uhlík benzenového kruhu, s obecným vzorcem CnH(2n+1)C6H5:
Některé další skupiny organických sloučenin:
Alkohol: organická sloučenina, ve které je hydroxylová funkční skupina (-OH) vázána na nasycený atom uhlíku
Alkanol: Alkohol, ve kterém je hydroxylová skupina vázána na alkan
Karboxylová kyselina: organická sloučenina, která obsahuje karboxylovou skupinu (C(=O)OH). Obecný vzorec karboxylové kyseliny je R-COOH, přičemž R se vztahuje ke zbytku molekuly
Kyselina alkanová:
Karboxylová kyselina, kde R je alkan.