Farbstoffe werden in vielen Industriezweigen verwendet – zum Einfärben von Kleidung, Farben, Kunststoffen, Fotografien, Drucken und Keramiken. Farbstoffe werden jetzt auch in neuartigen Anwendungen eingesetzt und als funktionell (Hochtechnologie) bezeichnet, da sie nicht nur aus ästhetischen Gründen, sondern für bestimmte Zwecke, z. B. in der Chirurgie, im Produkt enthalten sind.
Farbstoffe können entweder Farbstoffe oder Pigmente sein. Farbstoffe sind lösliche farbige organische Verbindungen, die in der Regel aus einer Lösung in Wasser auf Textilien aufgebracht werden. Sie sind so konzipiert, dass sie sich fest an die Polymermoleküle binden, aus denen die Textilfaser besteht.
Pigmente sind unlösliche Verbindungen, die in Farben, Druckfarben, Keramiken und Kunststoffen verwendet werden. Sie werden mit Hilfe einer Dispersion in einem geeigneten Medium aufgetragen. Bei den meisten Pigmenten handelt es sich ebenfalls um organische Verbindungen.
- Manipulation der Farbe und Anwendung von Farbstoffen
- Die Färbung von Textilien
- Klassifizierung von Farbstoffen
- Klassifizierung von Farbstoffen nach ihrer chemischen Struktur
- (a) Azofarbstoffe
- (b) Anthrachinonfarbstoffe
- (c) Phthalocyanine
- Klassifizierung der Farbstoffe nach Anwendungsmethoden
- Farbstoffe der Gruppe 1
- (i) Säurefarbstoffe
- (ii) Metallkomplexfarbstoffe
- (iii) Direktfarbstoffe
- (iv) Basische Farbstoffe
- (v) Dispersionsfarbstoffe
- Farbstoffe der Gruppe 2
- i) Reaktivfarbstoffe
- (ii) Küpenfarbstoffe
- (iii) Schwefelfarbstoffe
- Pigmente
- Funktionelle (hochtechnologische) Farbstoffe und Pigmente
- (a) Flüssigkristallanzeigen
- (b) Laserfarbstoffe
- (c) Tintenstrahldruck
- (d) Photodynamische Therapie
Manipulation der Farbe und Anwendung von Farbstoffen
Dieser Abschnitt befasst sich mit der Chemie, die hinter der Farbe von Farbstoffen steht, und damit, wie das Zielmaterial, z. B. eine Faser, die Färbemethode und den verwendeten Farbstoff beeinflusst.
Ein Farbstoff in Lösung wird durch die selektive Absorption bestimmter Wellenlängen des Lichts durch bestimmte Bindungen im Molekül gefärbt. Das durchgelassene Licht wird vom Betrachter gesehen und erscheint farbig, weil nun einige Wellenlängen des sichtbaren Spektrums fehlen.

Abbildung 1 Mauveine war der erste synthetische Farbstoff überhaupt. Er wurde 1856 zufällig von William Perkin hergestellt, der versuchte, Chinin zu synthetisieren. Besonders populär wurde es, als Königin Victoria auf der Royal Exhibition 1862 in London ein mit Mauvein gefärbtes Seidenkleid trug.
Mit freundlicher Genehmigung der Society of Dyers and Colourists.
Durch die Absorption sichtbarer Lichtenergie durch die Verbindung werden Elektronen im Molekül von einem Zustand niedriger Energie, dem Grundzustand, in einen Zustand höherer Energie, den angeregten Zustand, versetzt. Man spricht davon, dass das Molekül während dieses Anregungsprozesses einen elektronischen Übergang durchlaufen hat. Bestimmte Anregungsenergien entsprechen bestimmten Wellenlängen des sichtbaren Lichts.
Es ist ein n-Elektron (ein Elektron in einer Doppel- oder Dreifachbindung), das in den angeregten Zustand versetzt wird. Noch weniger Energie wird für diesen Übergang benötigt, wenn abwechselnd Einfach- und Doppelbindungen (d.h. konjugierte Doppelbindungen) in demselben Molekül vorhanden sind. Die Anregung des Elektrons wird durch das Vorhandensein aromatischer Ringe aufgrund der verstärkten Delokalisierung der n-Elektronen noch erleichtert.
Durch Veränderung der Struktur der Verbindung können Farbchemiker die Wellenlänge des absorbierten sichtbaren Lichts und damit die Farbe der Verbindung verändern.
Die Moleküle der meisten farbigen organischen Verbindungen enthalten zwei Teile:
(i) einen einzelnen Arylring (aromatisch) wie Benzol oder einen Benzolring mit einem Substituenten. Alternativ kann es sich um ein kondensiertes Ringsystem wie Naphthalin (zwei miteinander verschmolzene Ringe) oder Anthracen (drei miteinander verschmolzene Ringe) handeln.
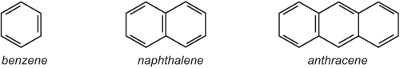
An der Stelle, an der die Ringe zusammenkommen, teilen sie sich zwei Kohlenstoffatome, so dass Naphthalin mit zwei Ringen 10 Kohlenstoffatome hat, nicht 12. In ähnlicher Weise hat Anthracen 14 Kohlenstoffatome und nicht 18. Da Naphthalin und Anthracen über alle Ringe hinweg delokalisierte Elektronen enthalten, ist es unangebracht, das Symbol für delokalisierte Elektronen zu verwenden, das in den anderen Einheiten für Benzol verwendet wird, da dies auf zwei oder drei getrennte delokalisierte Systeme hinweisen würde. Daher werden in dieser Einheit Kekule-Strukturen verwendet.
(ii) ein ausgedehntes konjugiertes Doppelbindungssystem, das ungesättigte Gruppen enthält, die als Chromophore bekannt sind, wie:
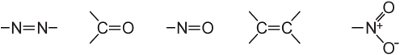
Die Intensität der Farbe kann in einem Farbstoffmolekül durch Hinzufügen von Substituenten, die einsame Elektronenpaare enthalten, zum Arylring erhöht werden, wie:
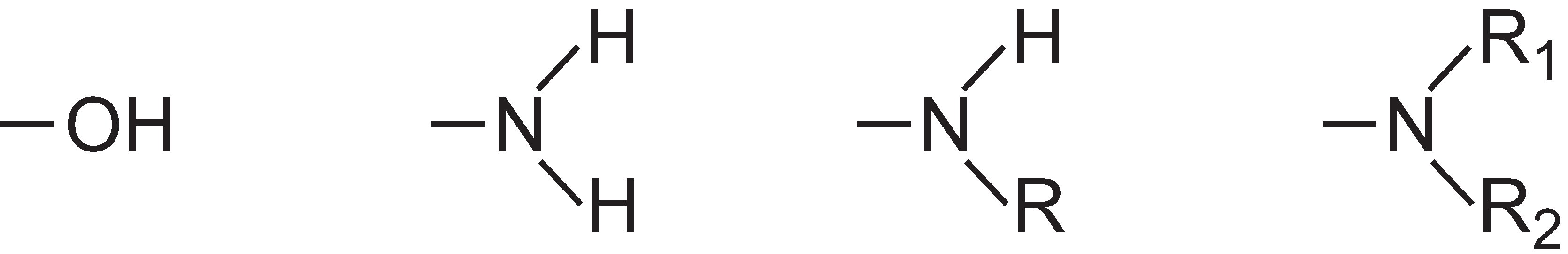
Diese Gruppen sind als Auxochrome bekannt.
Manchmal wird die gesamte Struktur des Farbstoffs als Chromogen bezeichnet.
Um den Farbstoff industriell nutzbar zu machen, müssen die Farbchemiker auch in der Lage sein, die Löslichkeit der Verbindung zu verändern, und es können Gruppen hinzugefügt werden, um den Farbstoff wasserlöslich zu machen. Beispiele hierfür sind die Sulfonsäuregruppe, -SO3H, oder die Carbonsäuregruppe, -COOH, oder üblicherweise das Natriumsalz dieser Säuren, -SO3-Na+ bzw. -COO-Na+.
Ein weiteres wichtiges Anliegen der Chemiker, die Farbstoffe entwickeln, ist die Verbesserung der Reaktivität mit dem zu färbenden Objekt, z. B. den Molekülen der Faser. Dies wird im Folgenden erörtert und mit Beispielen belegt.
Die Färbung von Textilien
Die chemische Beschaffenheit eines Farbstoffs wird durch die chemischen und physikalischen Eigenschaften der Fasern des zu färbenden Textils bestimmt. Die vier wichtigsten Fasertypen (Tabelle 1) sind Eiweißfasern, Zellulosefasern, Regeneratfasern (auf der Basis von Zellulose oder Derivaten) und synthetische Fasern.
| Naturfasern | Menschliche Fasern | ||
|---|---|---|---|
| Protein | Zellulose | Regenerat | Synthetisch |
| Wolle | Baumwolle | Viskose Viskose | Polyamide |
| Seide | Leinen | Celulose Ethanoate | Polyester |
| Mohair | Ramie | Acrylate | |
| Kaschmir | |||
| Der Begriff regeneriert wird verwendet, wenn ein natürliches Polymer chemisch behandelt wurde, um ein anderes Polymer zu bilden. Natürliche pflanzliche Zellulose zum Beispiel ergibt bei der Behandlung mit Ethansäureanhydrid (Essigsäureanhydrid) ein Polymer, Celluloseethanoat, das Zellwolle ist. |
|||
Tabelle 1 Klassifizierung von Textilfasern.
Während des Färbevorgangs eines Textils verteilt sich der Farbstoff zwischen den beiden Phasen, der festen Faserphase und der wässrigen Phase, und am Ende des Färbevorgangs ist die Lösung erschöpft und der größte Teil des Farbstoffs ist mit der Faser verbunden. Sobald die Farbstoffmoleküle in die Faser eindringen, kommt es zu einer unmittelbaren Wechselwirkung zwischen den beiden Komponenten, die eine Desorption der Farbstoffmoleküle zurück in die Lösung verhindert. Die Art der Wechselwirkung, ob physikalisch oder chemisch, hängt von den Gruppen auf den Farbstoffmolekülen und in den Faserketten ab (Tabelle 2).
| Bindungstyp | ungefähre relative Stärke |
|---|---|
| kovalent | 30,0 |
| ionisch | 7.0 |
| Wasserstoff | 3.0 |
| andere intermolekulare | 1.0 |
Tabelle 2 Ungefähre relative Bindungsstärken zwischen einem Farbstoff und einem Stoff.

Abbildung 2 Bevor ein Farbstoff verwendet wird, muss seine Lichtechtheit bestimmt werden. Diese
Gestelle an der Nordostküste Australiens werden für viele
Witterungstests verwendet, darunter auch für die Farbechtheit. Die Position der Gestelle kann
verändert werden, aber auf dem Foto stehen sie in einem Winkel von 45° zur Horizontalen.
Mit freundlicher Genehmigung des Allunga Exposure Laboratory.
Die Farbechtheit eines gefärbten Textils ist definiert als seine Widerstandsfähigkeit gegenüber Veränderungen, wenn es einer bestimmten Reihe von Bedingungen ausgesetzt wird. Der Farbstoff sollte durch Sonnenlicht (Lichtechtheit), Hitze beim Bügeln (Hitzeechtheit), Schweiß (Schweißechtheit) und beim Waschen (Waschechtheit) nicht stark beeinträchtigt werden.
Klassifizierung von Farbstoffen
Der Colour Index International, der von der Society of Dyers and Colourists in Bradford erstellt wird, ist eine umfassende Liste bekannter kommerzieller Farbstoffe und Pigmente und wird regelmäßig aktualisiert. Jeder Farbstoff ist mit einem Colour Index (C.I.) Namen und einer Nummer versehen. Zum Beispiel:
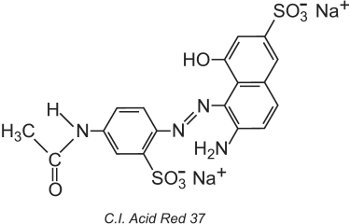
Alle Farbstoffe in der Liste wurden nach ihrer chemischen Struktur und nach ihrer Anwendungsmethode klassifiziert.
Klassifizierung von Farbstoffen nach ihrer chemischen Struktur
Der Colour Index ordnet Farbstoffe bekannter Struktur nach ihrem chemischen Typ einer von 25 Strukturklassen zu. Zu den wichtigsten gehören:
a) Azofarbstoffe
b) Anthrachinonfarbstoffe
c) Phthalocyanine
(a) Azofarbstoffe
Die Azofarbstoffe bilden die größte chemische Klasse, die mindestens 66% aller Farbstoffe enthält. Das charakteristische Merkmal ist das Vorhandensein einer oder mehrerer Azogruppen in den Strukturen,

zusammen mit Hydroxylgruppen, Amin- und substituierten Amingruppen als Hilfsstoffe.
Aromatische Azoverbindungen werden aus aromatischen Aminen über das entsprechende Diazoniumsalz hergestellt.
Ein Diazoniumsalz entsteht, wenn ein aromatisches Amin mit salpetriger (Salpetersäure(III)) Säure behandelt wird. Die salpetrige Säure wird in situ durch Zugabe von verdünnter Salzsäure zu einer kühlen Lösung von Natriumnitrit bei ca. 278 K gebildet. Im folgenden Beispiel wurde aus Phenylamin (Anilin), dem einfachsten aromatischen Amin, eine Lösung von Benzoldiazoniumchlorid gebildet:

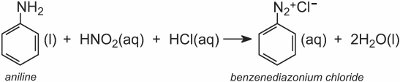
Eine Lösung einer anderen Verbindung, wie z. B. eines anderen aromatischen Amins oder eines Phenols, wird dann zu der gekühlten Lösung gegeben und ergibt eine Azoverbindung, die gefärbt ist. Ein Beispiel ist die Bildung eines roten Farbstoffs, wenn eine wässrige Lösung von 4-Aminonaphthalinsulfonsäure (Naphthionsäure) zu einer Lösung von 4-Nitrobenzoldiazoniumchlorid gegeben wird, um C.I. zu bilden. Acid Red 74:
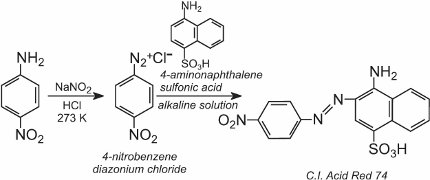
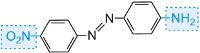
Azobenzol ist das Chromophor dieser Azofarbstoffe,
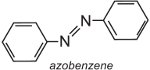
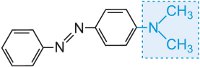
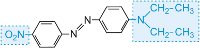
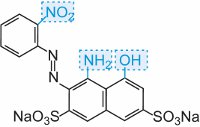
und die Farbe des Moleküls kann durch Variation der Auxochrome verändert und die Farbintensität erhöht werden (Tabelle 3).
| Struktur | Farbe beobachtet |
|---|---|
 |
gelb-grün |
 |
gelb |
 |
rot |
 |
blau |
 |
Tabelle 3 Die Molekularstrukturen einiger Azofarbstoffe mit den Auxochromen.
Einige Azofarbstoffe, die eine Hydroxygruppe ortho (oder para) zur Azogruppe enthalten, wie z.B. C.I. Acid Orange 7, weisen Tautomerie auf, ein Prozess, bei dem das Molekül in zwei oder mehr verschiedenen Strukturen im Gleichgewicht existiert. Das Wasserstoffatom der Hydroxylgruppe kann zum Stickstoffatom der Azogruppe wandern und umgekehrt:
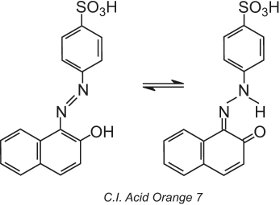
Bei dieser Art von Tautomerie besteht ein Gleichgewicht zwischen einem Hydroxyazotautomer und einem Ketohydrazontautomer, wobei das Ketohydrazontautomer im Allgemeinen dominiert und die beobachtete Farbe eine längere Wellenlänge aufweist (bathochrome Verschiebung).
(b) Anthrachinonfarbstoffe
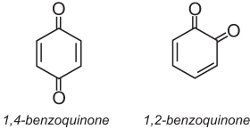
Anthrachinonfarbstoffe machen etwa 15 % der Farbstoffe aus und haben Strukturen, die auf Chinonen basieren. Das einfachste Chinon ist Benzochinon, das zwei Isomere aufweist:
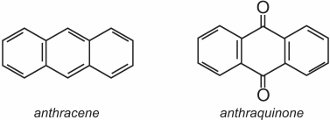
Anthrachinon, das einfachste der Anthrachinone, basiert auf Anthracen:
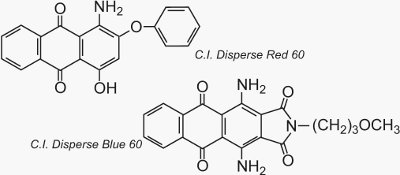
Zwei bekannte Beispiele für Anthrachinone, die als Farbstoffe verwendet werden, sind C.I. Disperse Red 60 und C.I. Disperse Blue 60:
(c) Phthalocyanine
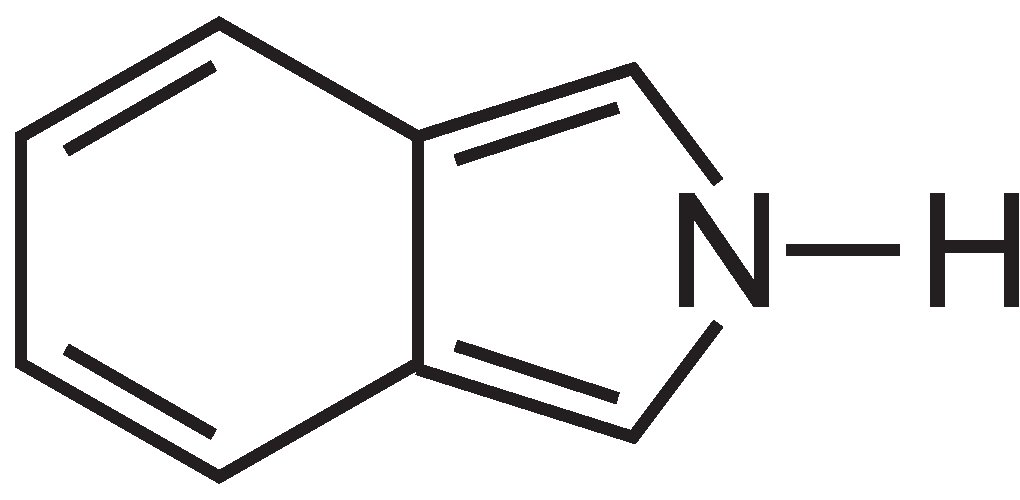
Phthalocyanine bestehen im Wesentlichen aus vier Molekülen Isoindol:
Diese Moleküle sind in einem Phthalocyanin durch Stickstoffatome miteinander verbunden. Die Struktur von Phthalocyanin ist:
Diese Moleküle sind in einem Phthalocyanin durch Stickstoffatome miteinander verbunden. Die Struktur von Phthalocyanin ist:
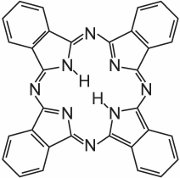
Phthalocyanine koordinieren sich mit Metallatomen. Die wichtigsten, die etwa 2 % aller Farbstoffe ausmachen, sind die Kupferphthalocyanine, die für ihre brillanten blauen und grünen Farben verwendet werden. Ein Beispiel ist C.I. Direct Blue 86:
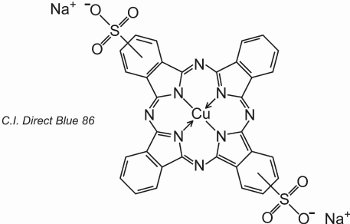
Die Sulfonsäuregruppen unterstützen die Löslichkeit des Farbstoffs in Wasser.
Die Formel zeigt, dass die Sulfonsäuregruppen an verschiedenen Stellen der aromatischen Ringe sitzen können.
Klassifizierung der Farbstoffe nach Anwendungsmethoden
Die Klassifizierung nach der Anwendungsmethode ist wichtig für den Textilfärber, der den Farbstoff anwendet, um die gewünschte Farbe zu erhalten. Um den gewünschten Farbton zu erhalten, muss der Färber in der Regel Mischungen von Farbstoffen herstellen und sicherstellen, dass diese miteinander verträglich sind.
Die grundlegenden Merkmale, die die Farbstoffübertragung von der Lösung auf die Faser steuern, sind:
- der pH-Wert der Lösung im Färbebad (für saure und basische Farbstoffe)
- ein Elektrolyt (eine Lösung von Natriumsulfat oder -chlorid)
- die Temperatur (im Bereich von Raumtemperatur bis 400 K)
- chemische Stoffe, die als Dispergiermittel bezeichneten Chemikalien, die eine stabile wässrige Dispersion von Farbstoffen mit sehr geringer Löslichkeit erzeugen
In Tabelle 4 sind die Farbstoffe unter ihren technologischen Bezeichnungen aufgeführt, die angeben, wie sie angewendet werden, sowie die Fasern, auf die sie angewendet werden.
| Farbstoff | Faser |
|---|---|
| Gruppe 1 | |
| Säure | Wolle und andere Proteinfasern, Polyamide |
| Metallkomplex | Wolle und andere Eiweißfasern, Polyamide |
| Direkt | Baumwolle, Leinen, Viskose |
| Basisch | Acryl |
| Dispers | Polyester, Polyamide, Ethanoate |
| Gruppe 2 | |
| Reaktiv | Baumwolle, Leinen, Viskose, Wolle, Seide |
| Mehrwertsteuer | Baumwolle, Leinen, Viskose |
| Schwefel | Baumwolle, Leinen |
Tabelle 4 Technologische Klassifizierung von Farbstoffen.
Farbstoffe der Gruppe 1
Farbstoffe dieser Gruppe zeichnen sich durch ihre Löslichkeit in Wasser aus. Sie sind daher nicht besonders waschecht. Die Anwendung erfolgt in einem einstufigen Verfahren.
(i) Säurefarbstoffe
Die wichtigsten chemischen Typen sind Azo-, Anthrachinon- und Phthalocyaninfarbstoffe, die das gesamte sichtbare Spektrum abdecken und somit eine vollständige Farbpalette ergeben. Diese Farbstoffe sind in Wasser löslich und bilden anionische Spezies. Sie werden in der Regel bei ca. 373 K angewendet. Während Wolle und andere Proteinfasern oberhalb dieser Temperatur leicht abgebaut werden, können Polyamidfasern (z. B. Nylons) bei 393 K behandelt werden, ohne dass sie Schaden nehmen (Tabelle 4).
Der pH-Wert der Lösung im Färbebad hängt von den individuellen Eigenschaften der Farbstoffe ab. Niedrigere Werte werden durch Zugabe von Schwefelsäure und höhere Werte durch Zugabe von Lösungen von Ethansäure und Ammoniumsulfat oder Ammoniumethanoat erreicht. Natriumsulfat kann zugesetzt werden, um die Diffusion der Farbstoffanionen in der Faserstruktur zu steuern.
Aufgrund der Struktur des Farbstoffs bilden sich Ionenbindungen, Wasserstoffbrücken und andere intermolekulare Wechselwirkungen (Tabelle 2) zwischen dem Farbstoff und der Faser, wodurch die Farbstoffe schnell werden. Ein Beispiel für einen typischen Säurefarbstoff ist C.I. Acid Red 73:
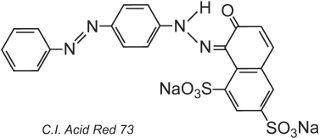
Eine der Azogruppen in diesem Tautomer liegt als Ketohydrazonform vor.
(ii) Metallkomplexfarbstoffe
Die chemischen Typen sind Azo und Anthrachinon, die eine vollständige Farbpalette ergeben. Sie sind jedoch stumpfer als die Säurefarbstoffe, weil in der Farbstoffstruktur ein Metallatom enthalten ist. Häufig werden Chromsalze verwendet, aber auch Kobalt- und Nickelsalze werden bevorzugt.
Das Metallatom bildet einen Koordinationskomplex mit zwei Molekülen einer Monoazoverbindung, die Hydroxyl-, Carboxyl- oder Aminogruppen in 2,2′-Position zur Azogruppe enthält. Diese Verbindungen werden als „1:2-Metallkomplex“-Farbstoffe bezeichnet. Ein Beispiel ist C.I. Acid Violet 78:
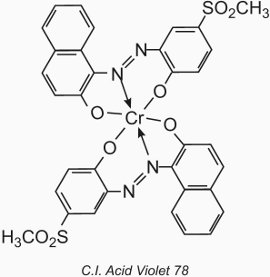
Ihre Anwendung auf Wolle ist ähnlich wie bei den Säurefarbstoffen, aber der pH-Wert ist auf den Bereich von 4,5 bis 6,0 beschränkt (Tabelle 4).
(iii) Direktfarbstoffe
Direktfarbstoffe eignen sich besonders zum Färben von Fasern aus Zellulose (Tabellen 1 und 4).
Sie werden mit Sulfonsäuregruppen synthetisiert, um sie in Wasser löslich zu machen, wobei sie in Natriumkationen und die anionische Farbstoffspezies dissoziieren. Sie sind außerdem so konzipiert, dass sie eine möglichst lineare und planare Struktur aufweisen. Dadurch kann sich der Farbstoff an die Zelluloseketten in der Faser anlagern, oft über intermolekulare Bindungen (einschließlich Wasserstoff).
Sie werden im Färbebad in wässriger Lösung aufgetragen, die Natriumchlorid enthält. Das Salz verringert die elektrischen Abstoßungskräfte zwischen der negativen Ladung auf der Faseroberfläche und der anionischen Farbstoffspezies.
Die meisten Direktfarbstoffe sind Azoverbindungen, die oft zwei oder drei Azogruppen enthalten. Beispiele hierfür sind C.I. Direct Orange 25, das -OH-, -NHCO- und -N=N-Gruppen aufweist, die alle das Potenzial haben, Wasserstoffbrückenbindungen mit den Hydroxylgruppen in Cellulose zu bilden:
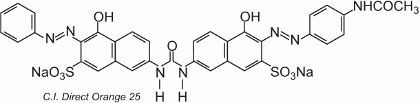
Der Farbstoff weist Tautomerie auf, da zwei Hydroxylgruppen in ortho-Stellung zu den Azogruppen vorhanden sind. Eines der Tautomere im Gleichgewicht mit dieser Form ist
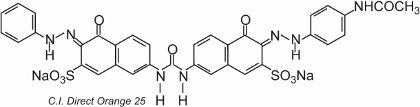
, bei dem zwei Ketohydrazongruppen vorhanden sind.
Ein weiteres Beispiel, C.I. Direct Blue 71, hat drei Azogruppen, von denen eine als Ketohydrazontautomer vorliegt:
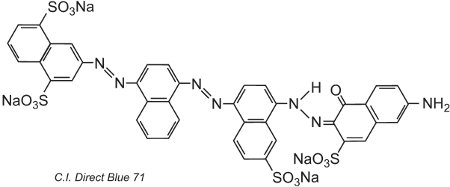
(iv) Basische Farbstoffe
Basische Farbstoffe gehörten zu den frühesten synthetischen Farbstoffen. Mauveine ist in der Tat ein basischer Farbstoff. Das Chromophor liegt als Kation vor und wird heute zum Färben von Acrylfasern verwendet (in der Regel ein Copolymer mit Propenonitril (Acrylnitril) und einer kleinen Menge eines Co-Monomers, das Sulfonat-, -SO3-, und Carboxylat-, -CO2-, Gruppen enthält). Dabei handelt es sich um Ionen-Ionen-Wechselwirkungen (Tabellen 2 und 4).
Es gibt etwa 100 basische (kationische) Farbstoffe, deren Farben Rot-, Gelb- und Blautöne mit leuchtenden kräftigen Nuancen umfassen. Einige basieren auf den Chromophorsystemen Azo und Anthrachinon. Viele basieren auch auf Arylcarbonium-Ionen. Beispiele sind C.I. Basic Green 4 (bekannt als Malachitgrün) und C.I. Basic Red 9.
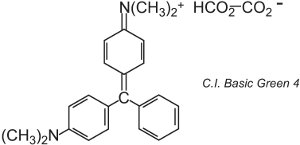 |
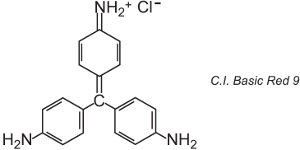 |
Beides sind Triarylmethane, eine Gruppe von Farbstoffen, die mit relativ kleinen Strukturveränderungen eine Reihe von roten, grünen und violetten Farbtönen erzeugen.
Andere, so genannte Polymethinfarbstoffe (sie enthalten eine oder mehrere -CH=-Gruppen) werden ebenfalls verwendet. Sie verdanken ihre Farbe dem Vorhandensein eines konjugierten Systems. Ein Beispiel für einen solchen Farbstoff ist C.I. Basic Yellow 28, ein Diazacyanin:
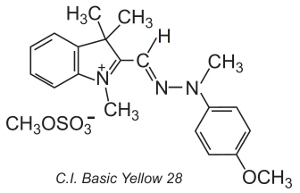
Die Farbstoffe werden oft in einer Lösung eines Elektrolyten, der die Diffusionsgeschwindigkeit in der Faserstruktur steuert, bei Temperaturen von etwa 370 K eingesetzt.
(v) Dispersionsfarbstoffe
Diese Farbstoffe sind im Wesentlichen hydrophob und in Wasser fast unlöslich. Sie haben jedoch eine Affinität für hydrophobe Fasern, z. B. Polyester, und werden als sehr feine Dispersionen in Wasser verwendet (Tabelle 4).
Die meisten Dispersionsfarbstoffe sind Azoverbindungen und können Farben im gesamten Spektrum erzeugen. Einige sind Farbstoffe auf Anthrachinonbasis für Rot-, Violett-, Blau- und Grüntöne.
Polyesterfasern können bei 400 K unter Druck gefärbt werden, was die Verwendung von Farbstoffstrukturen mit größerer Molekülgröße ermöglicht, die bessere Echtheiten erzielen, zum Beispiel:
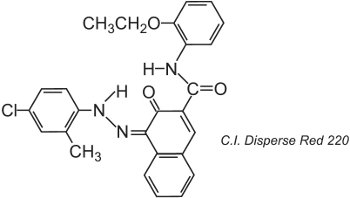
Die gezeigte Struktur ist das Ketohydrazontautomer.
Farbstoffe der Gruppe 2
Obwohl die Farbstoffe dieser Gruppe in einem zweistufigen Verfahren aufgetragen werden (im Gegensatz zum einstufigen Verfahren bei den Farbstoffen der Gruppe 1), haben die Farbstoffe Vorteile, insbesondere bei den Echtheiten.
i) Reaktivfarbstoffe
Reaktivfarbstoffe sind für das Färben von Baumwolle von herausragender Bedeutung, da sie leuchtende, intensive Färbungen mit hohen Echtheiten ermöglichen. Ungefähr 95 % der Reaktivfarbstoffe sind Azofarbstoffe, die die gesamte Farbpalette abdecken. Blau- und Grüntöne werden auch durch Anthrachinon- und Phthalocyanin-Strukturen erzeugt.
Wie der Name dieser Farbstoffe schon sagt, reagieren sie mit der Faser, sei es auf Zellulosebasis (Baumwolle) oder auf Proteinbasis (Wolle), und bilden kovalente Bindungen (Tabelle 4). Die beiden Phasen, zuerst die Färbung und dann die Reaktion, können getrennt oder gleichzeitig stattfinden. Das charakteristische Strukturmerkmal ist das Vorhandensein von einer oder mehreren reaktiven Gruppen. Typischerweise werden die Farbstoffe als
D-B-RG
dargestellt, wobei D das Chromogen, B eine verbrückende Gruppe und RG die reaktive Gruppe ist.
Die wichtigsten reaktiven Gruppen sind die chlorierten Triazine und Vinylsulfone.
Eines der drei Isomere des einfachsten Triazins ist:
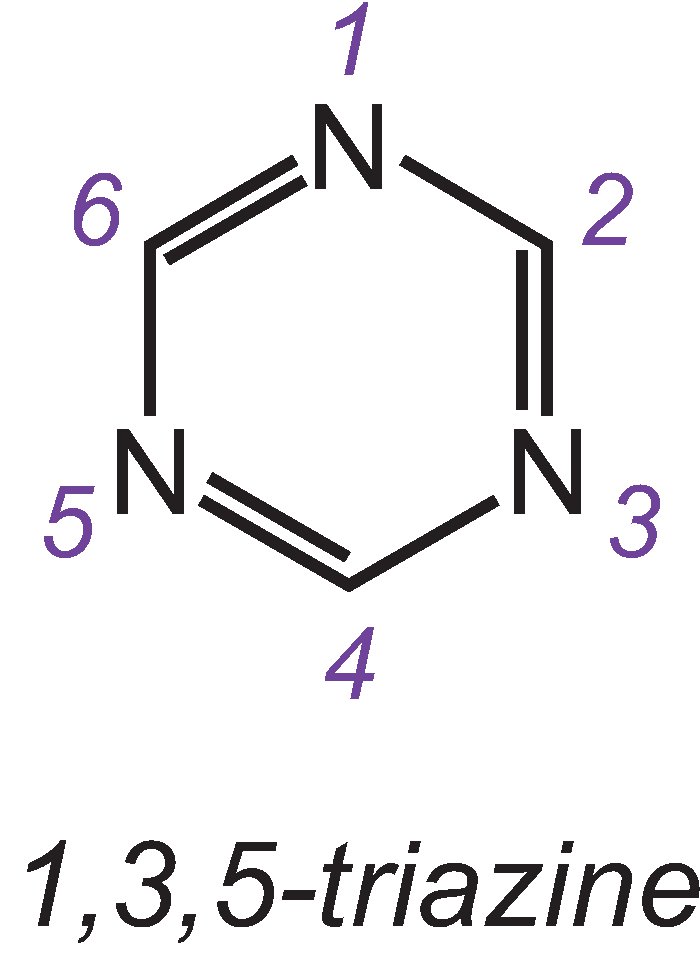
Ein Beispiel für einen Farbstoff mit einer Dichlortriazingruppe ist C.I. Reactive Blue 109:
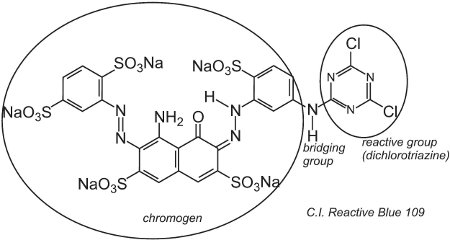
Die Reaktion zwischen den -OH-Gruppen der Zellulose in der Faser und den -C-Cl-Gruppen im Chlortriazin erfolgt durch eine (nukleophile) Substitutionsreaktion zur Bildung kovalenter Bindungen.
Ethenyl-(Vinyl-)sulfon enthält die CH2=CHSO2-Gruppe und das einfachste ist Diethenylsulfon (Divinylsulfon). Die Sulfongruppe ist in C.I. Reactive Blue 19 zu sehen:
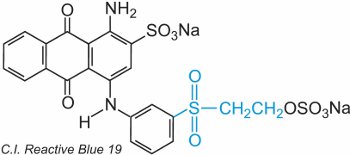
In diesem Beispiel gibt es keine verbrückende Gruppe.
Der Farbstoff reagiert mit Cellulose durch Addition an die Schwefel-Sauerstoff-Doppelbindung.
Reaktivfarbstoffe können in wässriger Lösung eine Hydrolyse des Sulfons erfahren, wodurch es gegenüber der Cellulose unreaktiv wird. Das bedeutet, dass der nicht umgesetzte Farbstoff, wenn er nicht ordnungsgemäß abgewaschen wird, auf der Oberfläche des Stoffes verbleibt und eine scheinbare Farbe ergibt, die sich mit der Zeit auswäscht. Um dieses Problem zu verringern, wurden Farbstoffe mit zwei verschiedenen reaktiven Gruppen mit unterschiedlicher Reaktivität entwickelt. Diese Farbstoffe bieten eine verbesserte Echtheit, denn wenn eine der Gruppen in Lösung hydrolysiert wird, reagiert die andere mit den Hydroxylgruppen im Stoff. Die erste dieser Gruppen enthält sowohl eine Chlortriazin- als auch eine Vinylsulfon-Gruppe; ein Beispiel dafür ist C.I. Reactive Red 194:
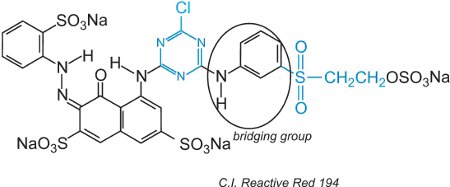
Neben den beiden unterschiedlichen Reaktivgruppen gibt es ein Chromogen und eine Brückengruppe.
Alle Reaktivfarbstoffe haben eine relativ kleine Molekülgröße, und sie haben auch zwei oder mehr Sulfonsäuregruppen im Chromogen, was zu einer hohen Wasserlöslichkeit führt. Ein Teil der Farbstoffspezies (anionisch) reagiert nicht mit der Faser, sondern wird hydrolysiert, und das Produkt muss durch Waschen entfernt werden.

Abbildung 3 Jeans werden mit Indigo und einer Vielzahl von Schwefelfarbstoffen gefärbt, wobei die Wahl von der gewünschten Farbe abhängt.
Mit freundlicher Genehmigung von Lizzie Hubbard.
(ii) Küpenfarbstoffe
Ungefähr 80 % der Küpenfarbstoffe gehören zur chemischen Klasse der Anthrachinone und decken die gesamte Farbpalette ab. Eine Art, die Indigo-Farbstoffe, umfasst Indigo:
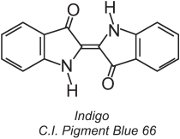
Alle Küpenfarbstoffe sind wasserunlöslich. Um sie auf eine Faser, zum Beispiel Baumwolle, aufzubringen, werden sie in eine alkalische Lösung gegeben (Tabelle 4). Der unlösliche Farbstoff wird zu einem farblosen (Leuko-)Anion reduziert, das löslich ist und eine Affinität zur Faser besitzt. Dieses wird dann von der Faser adsorbiert, manchmal in Gegenwart von Natriumchlorid, also unter ähnlichen Bedingungen wie bei den Direktfarbstoffen. Nach dem Färbevorgang wird der ursprüngliche unlösliche Stammfarbstoff in der Faser durch Oxidation regeneriert, in der Regel unter Verwendung einer Wasserstoffperoxidlösung oder einfach an der Luft:
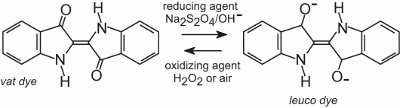
Die Farbstoffe sind in der Faserstruktur unlöslich und weisen daher eine gute Waschechtheit auf, und sie besitzen auch eine hohe Lichtechtheit.
(iii) Schwefelfarbstoffe
Schwefelfarbstoffe werden wie Küpenfarbstoffe in löslicher anionischer Form auf Textilien (Cellulose, Tabelle 4) aufgebracht und dann in die unlösliche Form oxidiert.
C.I. Sulphur Black 1 und C.I. Sulphur Blue 7 gehören zu den am meisten verwendeten Schwefelfarbstoffen. Wie andere Schwefelfarbstoffe auch, sind ihre Strukturen variabel und weitgehend unbekannt. Sie liefern eine Reihe von Schwarz-, Braun- und stumpfen Blautönen. Ihre Herstellung ist jedoch viel billiger als die von Küpenfarbstoffen, da ihre Zubereitung durch Erhitzen verschiedener organischer Verbindungen mit Schwefel einfach ist.
Pigmente
Pigmente werden zur Färbung von Farben, Druckfarben, Keramik und Kunststoffen verwendet. Sie können für eine viel größere Vielfalt von Stoffen verwendet werden als Farbstoffe, da sie für ihre Anwendung nicht auf die Wasserlöslichkeit angewiesen sind. Ein Pigment ist ein fein verteilter Feststoff, der in seinem Anwendungsmedium im Wesentlichen unlöslich ist. In den meisten Fällen wird das Pigment einem flüssigen Medium zugesetzt, z. B. einer nassen Farbe oder einem geschmolzenen Thermoplast. Dann lässt man das Medium durch Verdampfen des Lösungsmittels oder durch Abkühlen erstarren, wodurch die Pigmentmoleküle im festen Zustand mechanisch fixiert werden.
Die in Pigmenten verwendeten Chromophore sind in der Regel die gleichen wie die in Farbstoffen verwendeten, aber die Pigmente sind große Moleküle und haben keine löslich machenden Gruppen. Sie enthalten Gruppen, die intermolekulare Bindungen bilden, die zur Verringerung der Löslichkeit beitragen. Je größer das Molekül, desto undurchsichtiger ist das Pigment.

| Abbildungen 4 und 5 Die roten und gelben Farbstoffe sind Azopigmente (C.I. Pigment Red 57 und C.I. Pigment Yellow 13). Das Blau ist das Pigment Kupferphthalocyanin. Mit freundlicher Genehmigung der BASF. |
 |
Organische Pigmente erzeugen im Allgemeinen eine höhere Farbintensität und -helligkeit als anorganische Pigmente wie Chromgelb (Blei(II)-chromat(VI)).
Organische Pigmente weisen eine Reihe von Echtheitseigenschaften auf, die von der Molekularstruktur und der Art der intramolekularen Verbindung im festen Zustand abhängen. Eine Vergrößerung der Molekülgröße eines Pigments führt im Allgemeinen zu einer Verringerung der Löslichkeit des Pigments. Außerdem enthalten viele Pigmente eine Amidgruppe (-NHCO-), die ihre Löslichkeit weiter verringert, da die Moleküle in großen Strukturen durch Wasserstoffbrückenbindungen (zwischen der N-H-Gruppe in einem Molekül und einer C=O-Gruppe in einem anderen) zusammengehalten werden.
Viele organische Pigmente basieren auf der Azochemie und dominieren die gelben, orangen und roten Farbbereiche. Ein Beispiel für ein einfaches Monoazopigment ist C.I. Pigment Yellow 1:
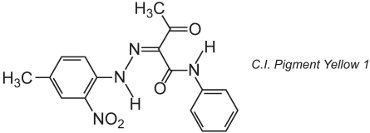
Diese Form ist das Ketohydrazontautomer.
Kupferphthalocyanine stellen den Großteil der blauen und grünen Pigmente. Sie sind strukturell komplex, aber relativ kostengünstig in der Herstellung. Sie bieten eine ausgezeichnete Beständigkeit gegen Licht, Hitze, Säuren und Laugen.
Ein Beispiel ist C.I. Pigment Blue 15:
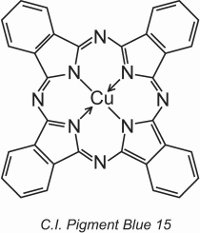
Zuvor wurde die Struktur eines Farbstoffs, C.I. Direct Blue 86, dargestellt, und es ist zu sehen, wie die Sulfonsäuregruppen in dieser Struktur ein Pigment in einen Farbstoff verwandeln.
Funktionelle (hochtechnologische) Farbstoffe und Pigmente
Funktionelle Farbstoffe und Pigmente werden im Vergleich zu Verbindungen, die zum Färben von Textilien verwendet werden, in kleinen Mengen hergestellt. Sie sind jedoch Gegenstand von Forschung und Interesse und werden für eine Vielzahl von Zwecken entwickelt. Einige davon sind im Folgenden dargestellt.
(a) Flüssigkristallanzeigen
Flüssigkristalle spielen seit vielen Jahren eine wichtige Rolle in unserem Leben in verschiedenen Formen von Informationsanzeigen, z. B. in Taschenrechnern. Ursprünglich konnten sie nur Unterschiede zwischen hell und dunkel anzeigen. Man fand heraus, dass dieser Kontrast durch die Verwendung von Farbstoffen erhöht und farbige Bildschirme hergestellt werden konnten. Inzwischen haben sie die traditionellen Anzeigetechnologien der Leuchtdioden und Kathodenstrahlröhren weitgehend ersetzt. Die verwendeten Farbstoffe wurden speziell entwickelt, um die Ausrichtung der Flüssigkristallmoleküle zu ändern und so eine höhere Farbintensität zu erzielen. Man sagt, dass diese Farbstoffe Dichroismus aufweisen.
(b) Laserfarbstoffe
Der Begriff Laser ist ein Akronym, das sich auf die Lichtverstärkung durch stimulierte Emission von Strahlung bezieht.
Gemeinsam wurden anorganische Laser verwendet, die jedoch nur in der Lage waren, Strahlung bei einigen ausgewählten Wellenlängen und in sehr schmalen Banden zu erzeugen. Die Verwendung von Farbstoffen hat die Erzeugung von Licht im gesamten Spektrum von 320 bis 1200 nm Wellenlänge ermöglicht. Farbstofflaser werden u. a. in der Kommunikationstechnologie und der Mikrochirurgie eingesetzt.
(c) Tintenstrahldruck
Der Tintenstrahldruck ist eine berührungslose Technik zur Erzeugung von Bildern, bei der kleine Tintentröpfchen, idealerweise computergesteuert, in schneller Folge auf ein Substrat gerichtet werden. Dieses Verfahren hat zahlreiche Anwendungen gefunden. Da die Tröpfchen so groß sein müssen, dass eine gute Schärfe erreicht wird, wurden Farbstoffe gegenüber Pigmenten bevorzugt. Die Tröpfchen sind kleiner (Pigmente neigen dazu, die Düsen zu verstopfen), und die wässrige Löslichkeit verringert die Umweltbelastung und hält den Preis niedrig. Die ersten Farbstoffe wurden bereits in anderen Industriezweigen verwendet, zeichneten sich jedoch durch schlechte Wasserechtheit aus. Dies hat zur Entwicklung spezifischer Farbstoffe und einzigartiger Flüssigkeitssysteme geführt. Diese Farbstoffe sind so konzipiert, dass sie in leicht alkalischen Systemen (pH 7,5 bis 10) löslich sind und durch die leicht sauren Bedingungen (pH 4,5 bis 6,5) auf dem Papier oder einem anderen Substrat unlöslich werden. Diese Technologie hat einen großen Einfluss auf den industriellen Großdruck von Verpackungen, Textilien, Wandbekleidungen und Werbedisplays.
(d) Photodynamische Therapie
Hierbei handelt es sich um eine Behandlung von Krebs, bei der eine Kombination aus Laserlicht, einer photosensibilisierenden Verbindung (dem Farbstoff) und molekularem Sauerstoff verwendet wird. Der Farbstoff wird dem Patienten intravenös verabreicht und dringt mit der Zeit in die Krebszellen ein. Die Bestrahlung der Zellen mit Laserlicht kann deren Zerstörung einleiten.
Der Laser interagiert mit dem Farbstoff und versetzt ihn in einen angeregten Zustand. Durch einen komplexen Prozess werden angeregte (reaktivere) Sauerstoffmoleküle erzeugt, die mit ungesättigten Zentren in den Proteinen und Lipiden der Zellmembran reagieren. Bei dieser Behandlungsmethode wird ein invasiver chirurgischer Eingriff vermieden.