Termit; luminesenssi, fotoluminesenssi, fluoresenssi ja fosforesenssi ovat rutiininomaisesti käytettyjä tutkimuspapereissa kuvaamaan valon emittoimista näytteestä. Tämä moninkertainen nimeäminen voi olla hämmentävää, sillä useita termejä käytetään vaihtelevasti ja eri tieteellisistä taustoista tulevat tutkijat käyttävät mieluummin yhtä nimitystä kuin toista. Tässä artikkelissa vastaamme kysymykseen: ”Mitä eroa on luminesenssilla, fotoluminesenssilla, fluoresenssilla ja fosforesenssilla”.
Mitä on luminesenssi?
Luminesenssi on mikä tahansa valon (sähkömagneettisten aaltojen) emissio aineesta, joka ei synny kuumentamalla. Tämä määritelmä erottaa luminesenssin hehkutuksesta, joka on aineen kohonneesta lämpötilasta johtuvaa valonsäteilyä, kuten hehkuvan kuuman hehkun. Sana luminesenssi on johdettu latinankielisestä valoa tarkoittavasta sanasta lumen ja latinankielisestä sanasta escentia, joka tarkoittaa ’prosessia’, ja on siis prosessi, jossa valoa syntyy.

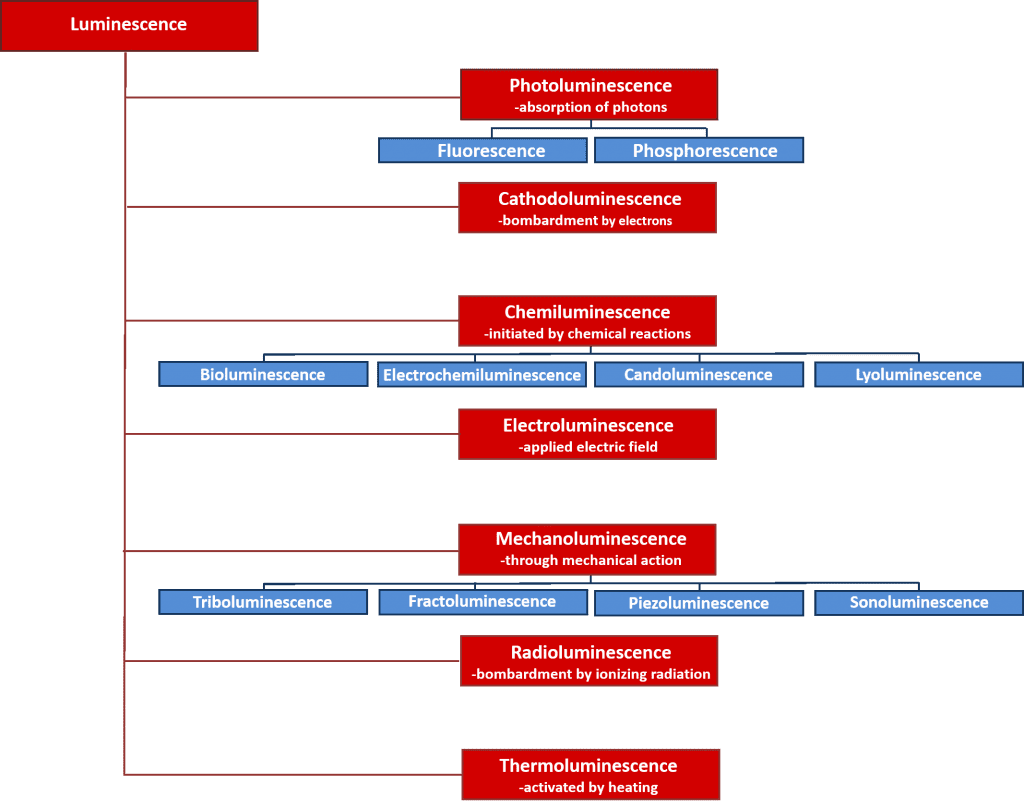
Luminesenssia on monenlaista, ja se voidaan luokitella luminesenssiprosessin käynnistävän energialähteen mukaan. Kuvassa 2 esitetään yleiskatsaus luminanssin eri tyypeistä ja niiden energialähteistä. Monilla näistä luminesenssiprosesseista on tärkeitä tieteellisiä ja teollisia sovelluksia, kuten elektroluminesenssi, jossa valo emittoituu elektronien ja aukkojen rekombinaatiosta sen jälkeen, kun materiaaliin on kohdistettu sähkökenttä, ja se on valoa emittoivien diodien toimintaperiaate, ja kemiluminesenssi, jossa valon emittoituminen käynnistyy kemiallisesta reaktiosta ja jota käytetään biologisissa testeissä ja joka on vastuussa hehkutikkujen hehkumisesta. Tässä artikkelissa keskitytään kuitenkin fotoluminesenssiin, joka muodostaa perustan tehokkaalle rikkomattomalle spektroskopiatekniikalle, fotoluminesenssispektroskopialle, jota käytetään laajalti sekä yliopistoissa että teollisuudessa.
Mitä on fotoluminesenssi?
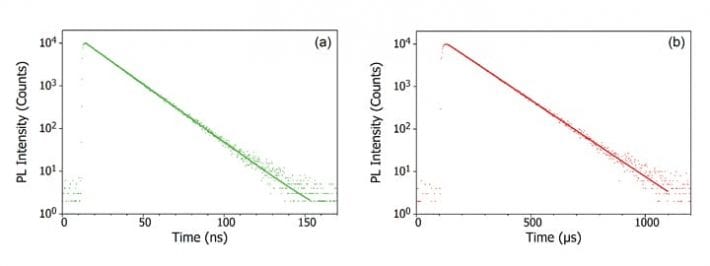
Fotoluminesenssi on valon emittoitumista materiaalista valon absorption jälkeen. Sana itsessään on sikäli mielenkiintoinen, että se on yhdistelmä latinankielisestä johdetusta sanasta luminesenssi ja kreikankielisestä valoa tarkoittavasta etuliitteestä foto-. Fotonien absorption aiheuttamaa luminesenssiä kutsutaan fotoluminesenssiksi. Kyse voi yhtä hyvin olla orgaanisen väriainemolekyylin valonemissiosta liuoksessa (kuva 3a) tai elektronien ja aukkojen rekombinaatiosta kaistasta toiseen puolijohteen valoherkistyksen seurauksena (kuva 3b).

Minkä tahansa fotoniabsorption indusoiman valon emissioinnin kuvaaminen fotoluminesenssiksi on täsmällistä; on kuitenkin yleinen käytäntö, erityisesti kemisteillä, jakaa fotoluminesenssi edelleen fluoresenssiin ja fosforesenssiin.
Mitä eroa on fluoresenssilla ja fosforesenssilla?
Fluoresenssille ja fosforesenssille on erilaisia määritelmiä, joista yksinkertaisin on, että fluoresenssi on välitöntä fotoluminesenssia, joka tapahtuu hyvin pian aineen valoherkistyksen jälkeen, kun taas fosforesenssi on pitkäikäistä fotoluminesenssia, joka jatkuu vielä pitkään sen jälkeen, kun valoherkistys on loppunut. Vaikka tämä on yksinkertainen määritelmä, se ei selitä, miksi fotoluminesenssin aikaskaaloissa on tällaisia eroja, ja jotkin materiaalit voivat jäädä harmaalle alueelle klassisen fluoresenssin ja fosforesenssin aikaskaalojen välille. Perusteellisemman määritelmän on perustuttava emissioprosessiin osallistuvien herätteiden ja perustilojen kvanttimekaniikkaan. Tätä lähestymistapaa käyttäen fluoresenssi ja fosforesenssi voidaan määritellä vastaavasti fotoluminesenssiksi, kun säteilevä siirtymä ei edellytä muutosta spinin moninaisuudessa, ja fotoluminesenssiksi, kun säteilevä siirtymä edellyttää muutosta spinin moninaisuudessa.
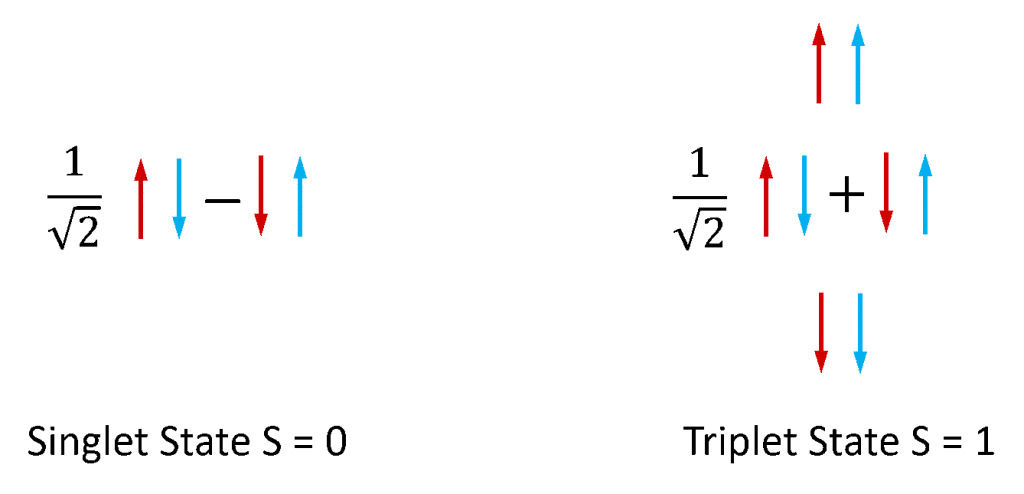
Fluoresenssia ja fosforesenssia käytetään tavallisimmin viittaamaan molekyylisysteemien fotoluminesenssiin. Vakaiden molekyylien elektronit ovat aina pareittain, sillä molekyylit, joissa on parittomia elektroneja, ovat erittäin reaktiivisia ja epävakaita. Elektroneilla on oma kulmamomentti, joka tunnetaan nimellä ”spin”, ja elektronipari voi olla jommassakummassa kahdesta spin-tilasta riippuen kahden elektronin spinien suhteellisesta symmetriasta. Jos elektroniparin spinit ovat antisymmetrisessä konfiguraatiossa, elektroniparin kokonaisspin on nolla (S = 0), kun taas jos ne ovat symmetrisessä konfiguraatiossa, elektroniparin kokonaisspin on yksi (S = 1). Kuten kuvassa 4 on havainnollistettu, on olemassa yksi elektronin spiniparin tilojen yhdistelmä, joka on antisymmetrinen, ja kolme spiniparin tilojen yhdistelmää, jotka ovat symmetrisiä, ja S = 0- ja S = 1-tiloja kutsutaan näin ollen vastaavasti singletti- ja triplettitiloiksi.
Kun fotoni absorboituu molekyylissä, toinen elektroneista kohoaa korkeammalle energiatasolle, ja molekyylissä ollaan nyt kiihottuneessa tilassa. Molekyylin perustila on (lähes) aina singlettitila (S0), ja kulmamomentin säilymisen vuoksi myös valoherkistyneen tilan on oltava singlettitila (S1), kuten alla olevasta Jablonski-diagrammista näkyy. S1-tilan hajoaminen takaisin S0-tilaan on sallittu siirtymä (koska molemmilla tiloilla on sama spin-kertaisuus), mikä johtaa nopeaan fotoluminesenssiin, joka tapahtuu pikosekunnista nanosekunneista nanosekunteihin ja jota kutsutaan fluoresenssiksi.
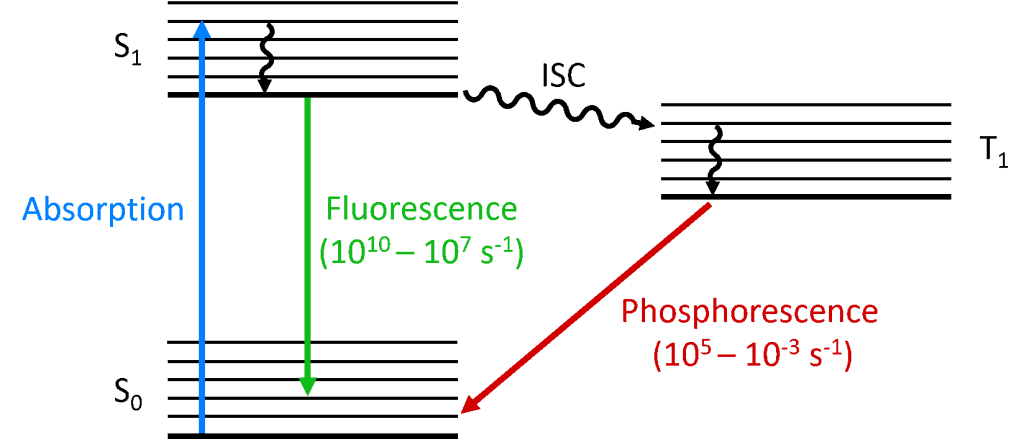
Vaihtoehtoisesti molekyyli voi käydä läpi systeemienvälisen siirtymän (ISC) kiihottuneeseen tripletti-tilaan (T1). ISC tapahtuu tyypillisesti molekyyleissä, joissa on suuri spin-orbit-kytkentä, eli elektronin orbitaalikulmamomentin ja spin-kulmamomentin kytkentä, joka mahdollistaa konversion singletti ja tripletti -tilojen välillä. Spin-orbit-kytkennän voimakkuus kasvaa atomin massan kasvaessa, ja siksi fosforisoivien molekyylien on sisällettävä raskasmetalleja, kuten europiumia ja iridiumia. T1-tilan hajoaminen takaisin S0-tilaan on kielletty siirtymä, koska tiloilla on erilainen spin-kertaisuus, mikä johtuu kulmamomentin säilymisestä. Spin-orbit-kytkentä kuitenkin lieventää tätä rajoitusta, ja säteilevä siirtyminen T1-tilasta S1-tilaan on mahdollista. Koska se on ”kielletty”, T1-S0-siirtymästä syntyvä fotoluminesenssi tapahtuu paljon hitaammalla aikaskaalalla, mikrosekunnista tuhansiin sekunteihin, ja sitä kutsutaan fosforesenssiksi.
On myös huomattava, että joidenkin materiaalien emissio ei aina siististi kuulu jompaankumpaan luokkaan. Esimerkkinä tästä on termisesti aktivoitu viivästynyt fluoresenssi (TADF). TADF:ssä S1- ja T1-tasot ovat energialtaan lähellä toisiaan ja voimakkaasti kytkeytyneitä, joten käänteinen ISC T1:stä S1:ään on mahdollista. Tämä synnyttää viivästyneen S1-S0-siirtymän, joka johtaa fotoluminesenssiin fluoresenssin ja fosforesenssin välisellä aikaskaalalla, jota kutsutaan viivästyneeksi fluoresenssiksi. Jos haluat lisätietoja TADF:stä ja sen käytöstä korkean hyötysuhteen OLED-ledissä, lue viesti ”Mikä on TADF?”.
Miten emissiota kuvataan fotoluminesenssina ja milloin fluoresenssina/fosforesenssina, riippuu viime kädessä henkilökohtaisista mieltymyksistä. Kemistit ja biologit, jotka tutkivat ensisijaisesti molekyylijärjestelmiä, suosivat fluoresenssin ja fosforesenssin käyttöä, koska näissä hyvin lokalisoiduissa molekyylijärjestelmissä on erilliset singletti ja tripletti tilat. Fyysikot sen sijaan tutkivat pääasiassa puolijohdemateriaaleja, joissa elektronit ovat hyvin delokalisoituneita ja joissa singletti ja tripletti eivät useinkaan ole merkityksellisiä. Tämä on yksi syy siihen, miksi fyysikot käyttävät yleensä laajempaa termiä fotoluminesenssi kuvaamaan valon emissiota.
Kutsuttiinpa sitä miksi tahansa, fotoluminesenssi, fluoresenssi ja fosforesenssi voivat antaa runsaasti tietoa molekyylien ja materiaalien ominaisuuksista, aina varauksenkuljettajien eliniän määrittämisestä aurinkokennoissa elävien solujen mikkelien ympärillä olevan solvaation dynamiikan mittaamiseen.
Luminesenssin, fotoluminesenssin, fluoresenssin ja fosforesenssin tuotteet
Fotoluminesenssin mittaamiseen tarvitaan fotoluminesenssispektrometri, ja Edinburgh Instruments tarjoaa valikoiman yksittäisiä fotonilaskentaan perustuvia fotoluminesenssispektrometrejä, joiden avulla voit mitata näytteidesi fotoluminesenssispektrejä, elinikää, anisotrooppisuutta ja kvanttituotosta.
Keep in Touch
Jos nautit tämän artikkelin lukemisesta ja haluat nähdä ensimmäisenä kaikki Edinburgh Instrumentsin viimeisimmät uutiset, sovellukset ja tuotetiedot, tilaa harvoin ilmestyvä uutiskirjeemme alla olevasta punaisesta tilauspainikkeesta ja seuraa meitä sosiaalisessa mediassa.