
Une femme hispanique de 57 ans s’est présentée avec les symptômes de voir des taches violettes occasionnelles dans sa vision depuis trois semaines. Elle n’était pas sûre que cela soit limité à un seul œil. Au-delà de cela, elle a déclaré que sa vision était bonne et qu’elle ne portait que des lunettes de lecture.
Ses antécédents médicaux étaient significatifs pour un diabète de type 2 et un diagnostic récent de VIH. Elle prenait des médicaments mais ne connaissait pas leurs noms, ni son taux de CD4 ou sa charge virale.
Sa meilleure acuité visuelle corrigée était de 20/20 OU. Les champs visuels de confrontation étaient complets jusqu’à un comptage soigneux des doigts. Les pupilles étaient également rondes et réactives ; aucun défaut pupillaire afférent n’a été observé. Le segment antérieur était normal dans les deux yeux. Il y avait des traces de cellules dans le vitré antérieur de l’œil droit. L’œil gauche était clair. Les tensions à l’aplanation mesuraient 11mm Hg OU.
Les nerfs optiques semblaient sains avec de petites cupules et une bonne coloration et perfusion des bords. Nous avons noté des résultats rétiniens évidents dans les deux yeux (figures 1 et 2).
Take the Retina Quiz
1. Que représentent les modifications rétiniennes périphériques de l’œil droit ?
a. Une occlusion de la veine rétinienne.
b. Une choriorétinite active.
c. Une rétinite active.
d. Rétinite inactive.
2. Que représentent les taches blanches du pôle postérieur ?
a. Des taches de coton.
b. Drusen.
c. Exsudat.
d. Des taches de Roth.
3. Quel est le diagnostic ?
a. Toxoplasmose.
b. Nécrose rétinienne aiguë.
c. Rétinite à cytomégalovirus.
d. Rétinopathie diabétique proliférante.
Pour les réponses, voir ci-dessous.
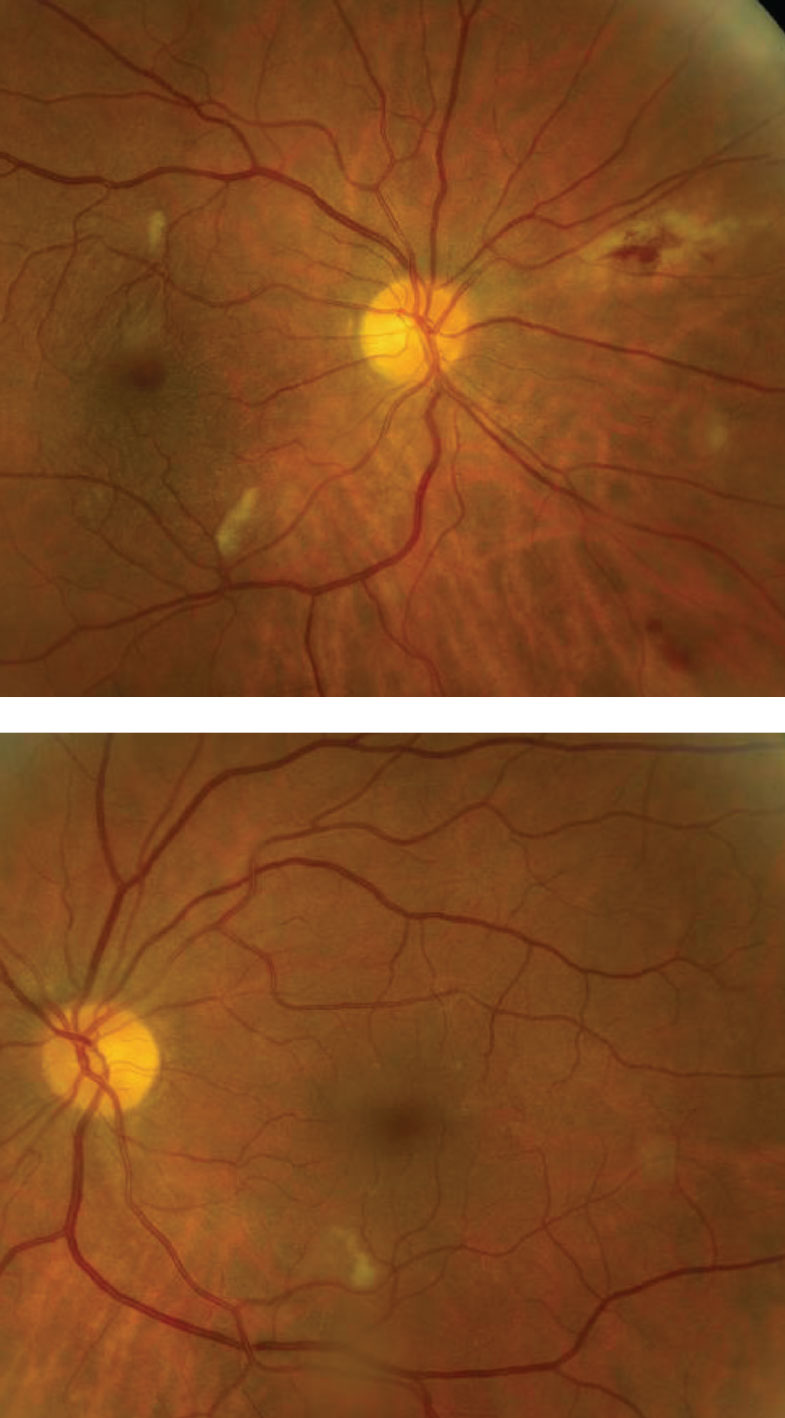
Figures 1 et 2. Notez les modifications rétiniennes périphériques nasales dans l’œil droit (ci-dessus). Pouvez-vous identifier la constatation dans les pôles postérieurs des deux yeux ? Cliquez sur l’image pour l’agrandir.
Diagnostic
Les modifications rétiniennes périphériques nasales de l’œil droit représentent une rétinite active à cytomégalovirus (CMV). Le CMV est l’un des virus de l’herpès qui infecte la plupart des adultes.1 Nous avons presque tous été exposés au CMV au cours de notre vie, mais nous ne présenterons aucun symptôme d’infection car notre système immunitaire est suffisamment fort pour garder le virus sous contrôle1. Mais, chez les personnes dont le système immunitaire est affaibli, comme notre patient séropositif, le virus peut se réactiver et se propager à la rétine, ce qui peut entraîner des complications menaçant la vision.1
La rétinite à CMV est la complication oculaire la plus fréquemment observée chez les patients séropositifs.1 La rétinite à CMV se développe chez les patients dont le nombre de lymphocytes T CD4+ (CD4) est inférieur à 50 et généralement même beaucoup plus bas que cela. Avec l’avènement de la thérapie antirétrovirale hautement active (HAART), le CMV a pratiquement disparu, avec une baisse spectaculaire de 55 % à 95 % du nombre de cas de rétinite à CMV.1
Discussion
La rétinite à CMV peut être présente n’importe où dans la rétine.1 Les lésions du pôle postérieur ont un aspect blanc caractéristique, hémorragique, avec nécrose et œdème rétinien, tandis que les lésions périphériques sont plus indolentes et non hémorragiques.1 La rétinite active suit généralement le trajet de la vascularisation rétinienne de manière centripète.1 Dans de rares cas, le CMV peut également se présenter sous la forme d’une angiite à branches givrées dans laquelle il existe une vascularite rétinienne fulminante et une périphlébite, donnant au fond d’œil une qualité givrée à l’exsudat périvasculaire.1
Les cellules vitréennes seront présentes dans le CMV actif, mais pas dans une mesure aussi importante que celle observée, par exemple, chez les patients atteints de toxoplasmose active, où la vitrite peut être si dense que la lésion rétinienne active peut être difficile à observer, lui donnant un aspect de « phares dans le brouillard ».1,2 En revanche, les patients atteints de CMV n’ont pas un système immunitaire robuste et ne sont donc pas en mesure de mettre en place une réponse immunitaire significative ; par conséquent, l’inflammation du vitré est minime et la rétinite peut être facilement observée.1
Que dire des lésions blanches dans le pôle postérieur de chaque œil ; est-ce aussi une rétinite à CMV ? Heureusement, ce ne sont pas des CMV mais plutôt des taches de ouate (CWS), qui peuvent facilement être confondues avec un CMV précoce. Les SP sont plus petits que les lésions du CMV et il n’y a pas d’inflammation du vitré. Les SP et même les hémorragies rétiniennes sont couramment observés chez les patients séropositifs gravement immunodéprimés.2 En fait, les SP et les hémorragies rétiniennes font partie du spectre de la rétinopathie du VIH.2 Bien que l’étiologie ne soit pas complètement comprise, les chercheurs affirment que les patients immunodéprimés présentent une viscosité plasmatique accrue qui entraîne un dépôt de complexes immuns.2 On pense que ce phénomène est dû à un effet cytopathique direct du virus sur l’endothélium vasculaire.2
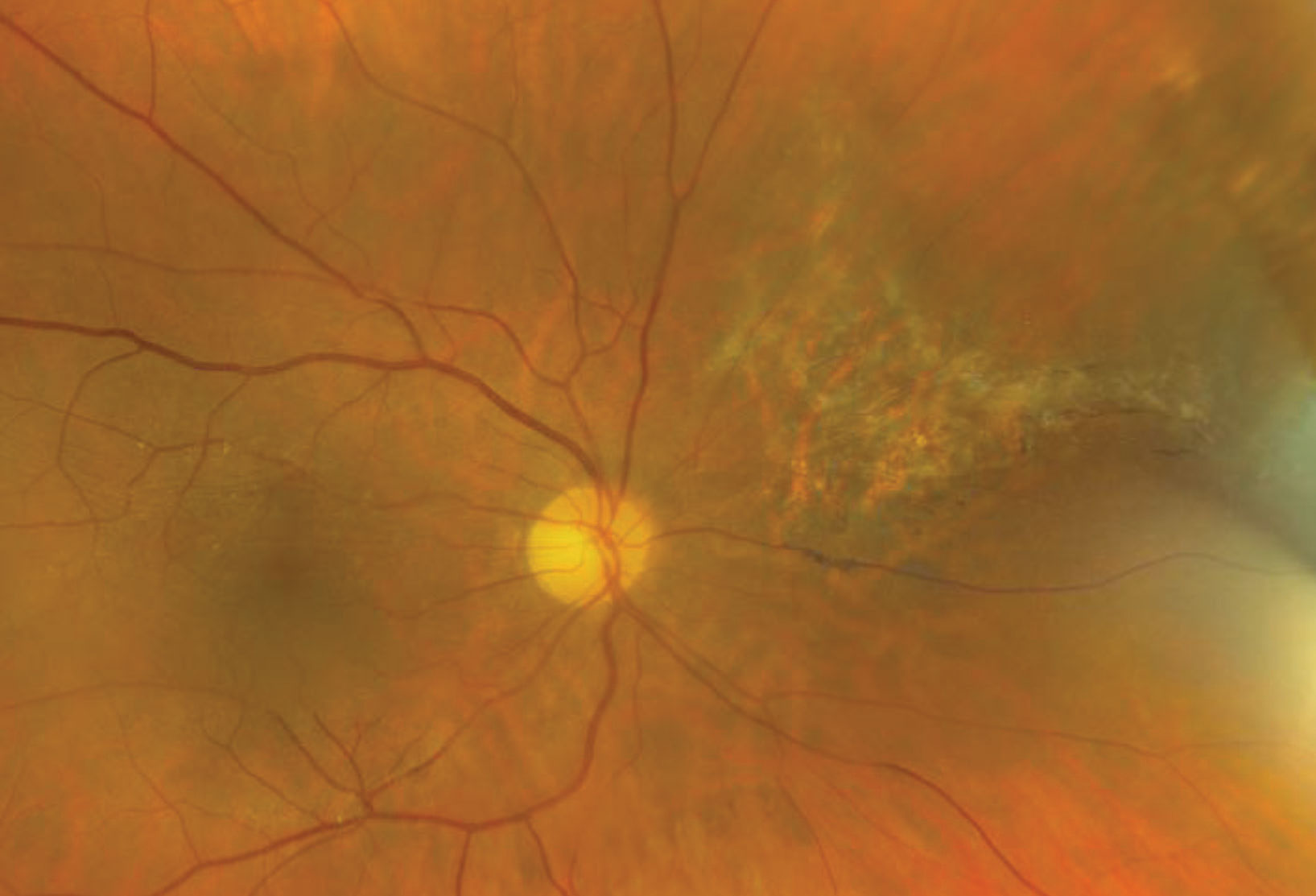
Fig. 3. Voici la rétine de notre patient cinq ans après le diagnostic initial. Cliquez sur l’image pour l’agrandir.
Options thérapeutiques
Le traitement de la rétinite à CMV est devenu assez standardisé avec l’arrivée des médicaments antiviraux, notamment le ganciclovir, le foscarnet, le valganciclovir et le cidofovir. Les méthodes d’administration du traitement comprennent la perfusion intraveineuse, la thérapie orale, l’injection intravitréenne et l’implant intraoculaire de ganciclovir.3 Le traitement anti-CMV spécifique est individualisé pour chaque patient en fonction de la localisation et de la gravité de la rétinite, du niveau de suppression immunitaire sous-jacente, des médicaments concomitants et de la capacité à se conformer au traitement.3 Le traitement est induit à fortes doses pendant deux à trois semaines ou jusqu’à ce que la rétinite se stabilise, suivi d’une dose d’entretien.3 L’amélioration de la survie des patients grâce à la multithérapie a entraîné un changement de paradigme, passant de la suppression de la maladie à court terme dans les premiers jours du traitement à l’arrêt actuel de la thérapie antivirale une fois la récupération immunitaire atteinte.3
Il est clair que notre patiente est gravement immunodéprimée. Elle ne connaissait pas ses CD4 et n’avait été diagnostiquée que récemment après un épisode de pneumonie. Elle a subi une injection intravitréenne immédiate de ganciclovir et a ensuite eu plusieurs implants de ganciclovir sur plusieurs années. Finalement, son système immunitaire s’est suffisamment rétabli pour qu’elle puisse interrompre la thérapie antivirale contre le CMV. Elle a pu maintenir une excellente acuité visuelle dans les deux yeux et nous continuons à la suivre sur une base annuelle (figure 3).
1. Jabs DA, Van Natta ML, Kempen J, et al. Caractéristiques des patients atteints de rétinite à cytomégalovirus à l’ère de la thérapie antirétrovirale hautement active. Am J Ophthalmol. 2002;133:48-61.
2. Freeman WR, Chen A, Henderly DE, et al. Prévalence et importance de la microvasculopathie rétinienne liée au syndrome d’immunodéficience acquise. Am J Ophthalmol. 1989;107(3):229-35.
3. Stewart MW. Gestion optimale de la rétinite à cytomégalovirus chez les patients atteints du sida. Clin Ophthalmol. 2010:4;285-99.
Retina Quiz Answers:
1) c ; 2) a ; 3) c ; 4) c.