A lumineszcencia, fotolumineszcencia, fluoreszcencia és foszforeszcencia kifejezéseket rutinszerűen használják a kutatási cikkekben a minta fénykibocsátásának leírására. Ez a többszörös elnevezés zavaró lehet, mivel több kifejezést felváltva használnak, és a különböző tudományos háttérrel rendelkező kutatók az egyik elnevezést előnyben részesítik a másikkal szemben. Ebben a cikkben arra a kérdésre válaszolunk, hogy “Mi a különbség a lumineszcencia, a fotolumineszcencia, a fluoreszcencia és a foszforeszcencia között”.
Mi a lumineszcencia?
A lumineszcencia egy anyagból származó bármilyen fénykibocsátás (elektromágneses hullámok), amely nem melegítéssel jön létre. Ez a meghatározás megkülönbözteti a lumineszcenciát az izzástól, amely egy anyag megemelkedett hőmérsékletének, például egy izzó parázsnak köszönhető fénykibocsátás. A lumineszcencia szó a fényt jelentő latin lumen szóból és a latin escentia szóból származik, amelynek jelentése ‘a folyamat’, tehát a fénykibocsátás folyamata.

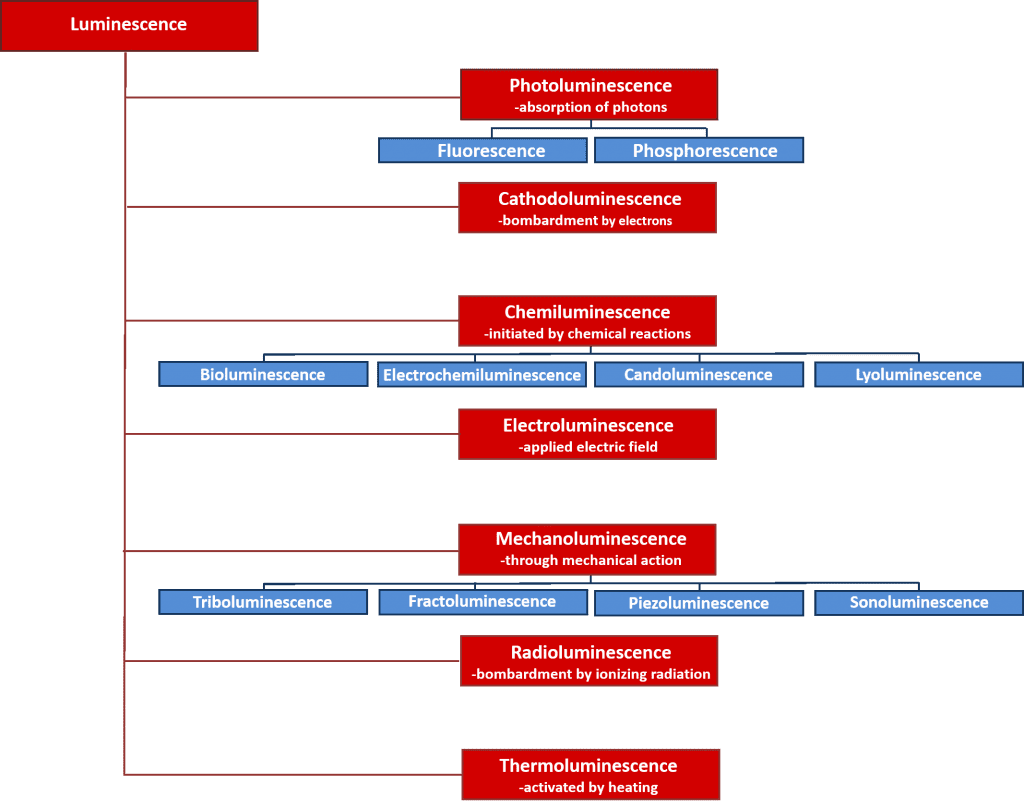
A lumineszcenciának számos típusa létezik, amelyeket a lumineszcencia folyamatát elindító energiaforrás alapján lehet osztályozni. A lumineszcencia különböző típusainak és energiaforrásaiknak áttekintése a 2. ábrán látható. E lumineszcenciafolyamatok közül soknak fontos tudományos és ipari alkalmazása van, mint például az elektrolumineszcencia, ahol a fény az elektronok és lyukak rekombinációja során jön létre, miután egy anyagon elektromos mezőt alkalmaznak, és ez a fénykibocsátó diódák működési elve; és a kemilumineszcencia, ahol a fénykibocsátást kémiai reakció indítja el, és biológiai vizsgálatokban használják, és ez a felelős a világító pálcikák világításáért. E cikk középpontjában azonban a fotolumineszcencia áll, amely az alapja a nagy teljesítményű, roncsolásmentes spektroszkópiai technikának, a fotolumineszcencia-spektroszkópiának, amelyet széles körben alkalmaznak mind a tudományos életben, mind az iparban.
Mi a fotolumineszcencia?
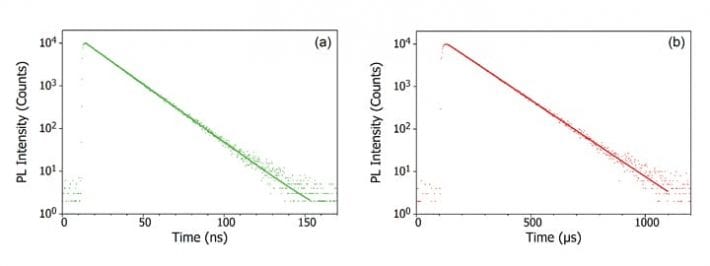
A fotolumineszcencia az anyag fénykibocsátása a fény elnyelését követően. A szó önmagában is érdekes, mivel a latin eredetű luminescence szó és a fényt jelentő görög foto- előtag kombinációja. Minden olyan lumineszcenciát, amelyet fotonok elnyelése indukál, fotolumineszcenciának nevezünk. Ez lehet ugyanúgy egy oldatban lévő szerves festékmolekula fénykibocsátása (3a. ábra), vagy az elektronok és lyukak sávok közötti rekombinációja egy félvezető fotógerjesztését követően (3b. ábra).

Minden fotonelnyelés indukálta fényemissziót fotolumineszcenciaként leírni pontos; azonban általános gyakorlat, különösen a vegyészeknél, hogy a fotolumineszcenciát tovább osztják fluoreszcenciára és foszforeszcenciára.
Mi a különbség a fluoreszcencia és a foszforeszcencia között?
A fluoreszcenciának és a foszforeszcenciának többféle definíciója létezik, a legegyszerűbb szerint a fluoreszcencia azonnali fotolumineszcencia, amely nagyon röviddel az anyag fotógerjesztése után jelentkezik, míg a foszforeszcencia hosszú életű fotolumineszcencia, amely a fotógerjesztés megszűnése után még sokáig tart. Bár ez egy egyszerű meghatározás, nem magyarázza meg, hogy miért van ekkora különbség a fotolumineszcencia időskálái között, és egyes anyagok a klasszikus fluoreszcencia és foszforeszcencia időskálák közötti szürke zónába eshetnek. Az alaposabb meghatározásnak az emissziós folyamatban részt vevő gerjesztett és alapállapotok kvantummechanikáján kell alapulnia. Ezt a megközelítést alkalmazva a fluoreszcencia és a foszforeszcencia definiálható fotolumineszcenciaként, ahol a sugárzási átmenet nem igényel változást a spin multiplicitásában, illetve fotolumineszcenciaként, ahol a sugárzási átmenet a spin multiplicitás változásával jár.
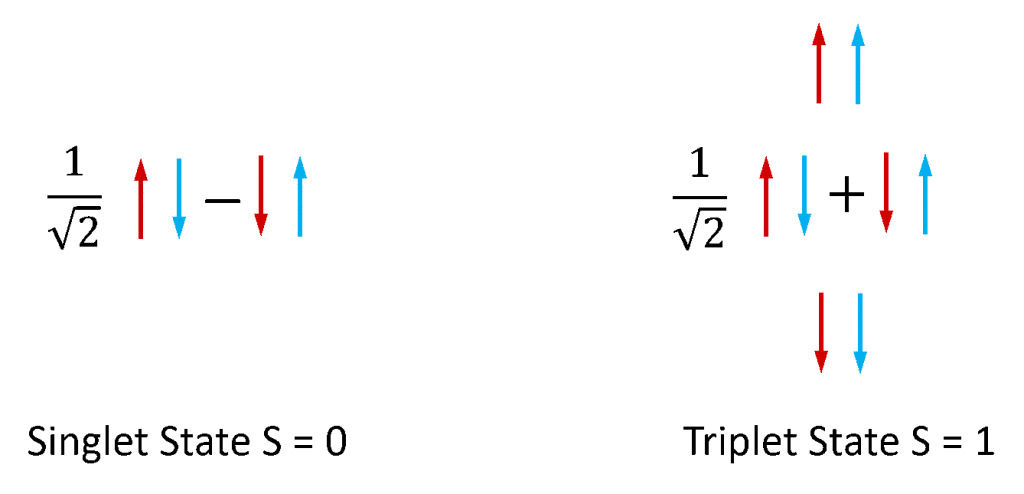
A fluoreszcenciát és a foszforeszcenciát leggyakrabban a molekuláris rendszerek fotolumineszcenciájára használják. A stabil molekulákban az elektronok mindig párban léteznek, mivel a párosítatlan elektronokkal rendelkező molekulák rendkívül reaktívak és instabilak. Az elektronok rendelkeznek egy saját szögimpulzussal, amelyet “spin”-nek nevezünk, és egy elektronpár két teljes spinállapotban létezhet, a két elektron spinjének relatív szimmetriájától függően. Ha a két spin antiszimmetrikus konfigurációban van, akkor az elektronpár teljes spinje nulla (S = 0), míg ha szimmetrikus konfigurációban vannak, akkor a pár teljes spinje egy (S = 1). Amint a 4. ábrán látható, az elektronspin-pár állapotainak egy olyan kombinációja létezik, amely antiszimmetrikus, és három olyan kombinációja, amely szimmetrikus, ezért az S = 0 és S = 1 állapotokat szingulettnek, illetve triplettnek nevezzük.
Amikor egy foton elnyelődik a molekulában, az egyik elektron magasabb energiaszintre emelkedik, és a molekula most gerjesztett állapotba kerül. A molekula alapállapota (majdnem) mindig szingulett állapot (S0), és a szögimpulzus megőrzése miatt a fotoergerjesztett állapotnak is szingulettnek (S1) kell lennie, amint azt az alábbi Jablonski-diagram mutatja. Az S1 állapotnak az S0-ba való visszaalakulása megengedett átmenet (mivel mindkét állapotnak azonos a spin multiplicitása), ami azonnali fotolumineszcenciát eredményez, amely pikoszekundumtól nanoszekundumig terjedő időskálán jelentkezik, és fluoreszcenciának nevezzük.
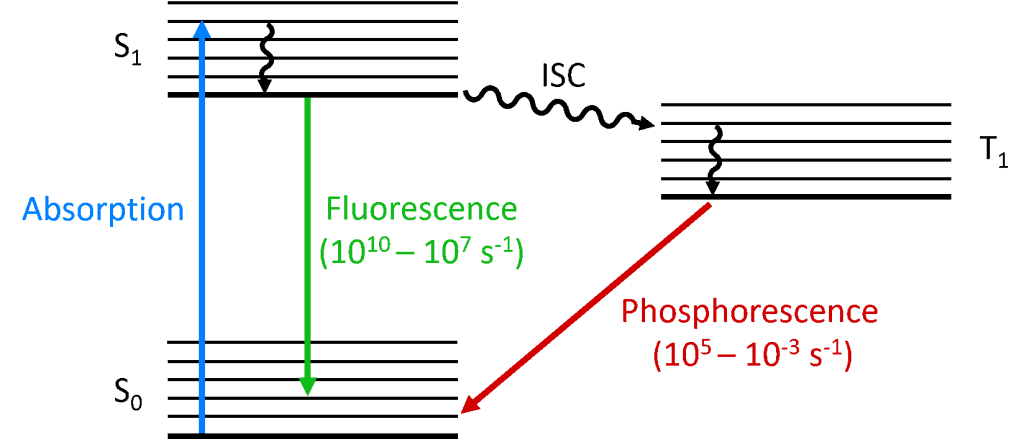
Alternatívaként a molekula átmehet rendszerközi átmenet (ISC) a gerjesztett triplett állapotba (T1). Az ISC jellemzően olyan molekulákban fordul elő, amelyekben nagyfokú a spin-orbit csatolás, azaz az elektron orbitális szögimpulzusának és spin-szögimpulzusának csatolása, ami lehetővé teszi a szingulett és triplett állapotok közötti átalakulást. A spin-orbit csatolás erőssége az atom tömegével nő, ezért a foszforeszkáló molekuláknak olyan nehézfémeket kell tartalmazniuk, mint az európium és az irídium. A T1 állapot visszabomlása az S0-ba tiltott átmenet, mivel az állapotok a szögimpulzus megőrzése miatt különböző spin-szorosságúak. A spin-orbit csatolás azonban feloldja ezt a korlátozást, és lehetővé válik a sugárzásos átmenet a T1 állapotból az S1 állapotba. Mivel ez “tiltott”, a T1-S0 átmenetből eredő fotolumineszcencia sokkal lassabb időskálán, mikroszekundumoktól több ezer másodpercig terjedő időtartományban jelentkezik, és foszforeszcenciának nevezik.
Meg kell jegyezni azt is, hogy egyes anyagok emissziója nem mindig sorolható egyértelműen egyik vagy másik kategóriába. Erre példa a termikusan aktivált késleltetett fluoreszcencia (TADF). A TADF-ben az S1 és a T1 szintek energiája közel van egymáshoz és erősen csatoltak, ezért lehetséges a fordított ISC a T1-ről az S1-re. Ez késleltetett S1-S0 átmenetet eredményez, amely a fluoreszcencia és a foszforeszcencia közötti időskálán, késleltetett fluoreszcenciaként ismert fotolumineszcenciát eredményez. A TADF-ről és a nagy hatékonyságú OLED-ekben való alkalmazásáról bővebben a “Mi a TADF?” című bejegyzésben olvashat.
Az, hogy az emissziót mikor nevezzük fotolumineszcenciának és mikor fluoreszcenciának/foszforeszcenciának, végső soron személyes preferencia kérdése. A kémikusok és biológusok, akik elsősorban molekuláris rendszereket tanulmányoznak, a fluoreszcencia és a foszforeszcencia használatát részesítik előnyben, mivel ezekben az erősen lokalizált molekuláris rendszerekben megkülönböztethető szinglet és triplett állapotok vannak. Ezzel szemben a fizikusok elsősorban félvezető anyagokat tanulmányoznak, ahol az elektronok erősen delokalizáltak, és a szinglet és triplett állapot fogalma gyakran már nem releváns. Ez az egyik oka annak, hogy a fizikusok a fénykibocsátás leírására a tágabb értelemben vett fotolumineszcencia kifejezést használják.
Bárhogy is nevezzük, a fotolumineszcencia, fluoreszcencia és foszforeszcencia rengeteg információt szolgáltathat a molekulák és anyagok tulajdonságairól; a töltéshordozók élettartamának meghatározásától a napelemekben a szolvatációs dinamika méréséig az élő sejtek micellái körül.
Termékek a lumineszcenciához, fotolumineszcenciához, fluoreszcenciához és foszforeszcenciához
A fotolumineszcencia méréséhez fotolumineszcencia-spektrométerre van szükség, és az Edinburgh Instruments egyfotonszámláló fotolumineszcencia-spektrométereket kínál a minták fotolumineszcencia-spektrumának, élettartamának, anizotrópiájának és kvantumhozamának méréséhez.
Keep in touch
Ha élvezte ezt a cikket, és szeretne elsőként értesülni az Edinburgh Instruments legújabb híreiről, alkalmazásairól és termékinformációiról, akkor iratkozzon fel ritkán megjelenő hírlevelünkre az alábbi piros feliratkozási gomb segítségével, és kövessen minket a közösségi médiában.
Egyébként pedig kövessen minket a közösségi médiában.