Nazwa ogólna: sodu polistyrenosulfonian
Postać dawkowania: zawiesina doustna / doodbytnicza
Medically reviewed by Drugs.com. Ostatnio aktualizowany w dniu 22 lipca 2020.
- Overview
- Side Effects
- Dosage
- Professional
- Interactions
- More
- Indications and Usage for Kionex
- Kionex dawkowanie i podawanie
- Informacje ogólne
- Zalecane dawkowanie
- Przygotowanie i podawanie
- Postacie dawkowania i moc
- Przeciwwskazania
- Ostrzeżenia i środki ostrożności
- Nekroza jelit
- Zaburzenia elektrolitowe
- Przeciążenie płynami u pacjentów wrażliwych na wysokie spożycie sodu
- Ryzyko aspiracji
- Wiązanie z innymi lekami podawanymi doustnie
- Działania niepożądane
- Interakcje lekowe
- Interakcje ogólne
- Przeciwskazania do wymiany kationów
- Sorbitol
- STOSOWANIE W SZCZEGÓLNYCH POPULACJACH
- Ciąża
- Laktacja
- Stosowanie u dzieci
- Przedawkowanie
- Kionex Opis
- Kionex – Farmakologia kliniczna
- Mechanizm działania
- Farmakodynamika
- Farmakokinetyka
- Toksykologia niekliniczna
- Karcynogeneza, mutageneza, upośledzenie płodności
- Jak dostarczyć/ Przechowywanie i postępowanie
- Informacje dla pacjenta
- PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
- Więcej o Kionex (sodium polystyrene sulfonate)
- Zasoby dla konsumentów
- Zasoby dla profesjonalistów
- Przewodniki dotyczące leczenia
Indications and Usage for Kionex
Kionexis wskazany w leczeniu hiperkaliemii.
Ograniczenie stosowania:
Kionex nie powinien być stosowany jako leczenie doraźne zagrażającej życiu hiperkaliemii z powodu opóźnionego początku działania.
Kionex dawkowanie i podawanie
Informacje ogólne
Podawać Kionex co najmniej 3 godziny przed lub 3 godziny po innych lekach doustnych. Pacjenci z gastroparezą mogą wymagać 6-godzinnego odstępu
Zalecane dawkowanie
Intensywność i czas trwania terapii zależą od ciężkości i oporności hiperkaliemii.
Doustnie
Średnia całkowita dawka dobowa leku Kionex dla dorosłych wynosi od 15 g do 60 g, podawana w dawce 15 g (cztery płaskie łyżeczki do herbaty), jeden do czterech razy na dobę.
Doustnie
Średnia dawka dla dorosłych wynosi od 30 g do 50 g co sześć godzin.
Przygotowanie i podawanie
Przygotować zawiesinę na świeżo i zużyć w ciągu 24 godzin.
Nie podgrzewać preparatu Kionex, ponieważ może to zmienić właściwości wymienne żywicy.
Jedna płaska łyżeczka zawiera około 3,5 g leku Kionex i 15 mEq sodu.
Zawiesina doustna
Każdą dawkę zawiesić w niewielkiej ilości wody lub syropu, około 3 do 4 mL płynu na gram żywicy. Podawać pacjentowi w pozycji pionowej .
Enema
Po wstępnej lewaty oczyszczającej, wprowadzić miękką, gumową rurkę o dużym rozmiarze (French 28) do odbytnicy na odległość około 20 cm, z końcówką dobrze w esicy, i zakleić taśmą.
Podawać jako ciepłą (temperatura ciała) emulsję w 100 ml roztworu wodnego i spłukać 50 do 100 ml płynu. Można zastosować nieco gęstszą zawiesinę, ale nie należy tworzyć pasty.
Podczas podawania emulsję należy delikatnie wstrząsnąć. Żywica powinna być zatrzymana tak długo, jak to możliwe, a następnie należy wykonać lewatywę oczyszczającą z roztworem niezawierającym sodu. Należy zapewnić odpowiednią objętość roztworu oczyszczającego (do 2 litrów).
Postacie dawkowania i moc
Kionex ma postać kremowego do jasnobrązowego, drobno zmielonego proszku i jest dostępny w słoikach o pojemności 454 g.
Przeciwwskazania
Kionex jest przeciwwskazany u pacjentów z następującymi stanami:
– Nadwrażliwość na żywice sulfonianu polistyrenu – Obstrukcyjna choroba jelit – Noworodki ze zmniejszoną motoryką jelit
Ostrzeżenia i środki ostrożności
Nekroza jelit
Zgłaszano przypadki martwicy jelit, niektóre śmiertelne, oraz inne poważne działania niepożądane dotyczące przewodu pokarmowego (krwawienie, niedokrwienne zapalenie jelita grubego, perforacja) w związku ze stosowaniem produktu leczniczego Kionex. W większości tych przypadków zgłaszano jednoczesne stosowanie sorbitolu. Czynniki ryzyka wystąpienia zdarzeń niepożądanych dotyczących przewodu pokarmowego występowały w wielu przypadkach, w tym wcześniactwo, choroby jelit lub zabiegi chirurgiczne w wywiadzie, hipowolemia oraz niewydolność i niewydolność nerek. Jednoczesne podawanie sorbitolu nie jest zalecane.
– Stosować wyłącznie u pacjentów z prawidłową czynnością jelit. Unikać stosowania u pacjentów, którzy nie mieli wypróżnienia po zabiegu chirurgicznym. – Unikać stosowania u pacjentów, u których istnieje ryzyko wystąpienia zaparć lub ucisku (w tym u pacjentów z zaparciami w wywiadzie, przewlekłymi zaparciami, chorobami zapalnymi jelit, niedokrwiennym zapaleniem jelita grubego, miażdżycą naczyń jelitowych, wcześniejszą resekcją jelita lub niedrożnością jelit). Zaprzestać stosowania u pacjentów, u których wystąpią zaparcia.
Zaburzenia elektrolitowe
Podczas leczenia należy monitorować stężenie potasu w surowicy, ponieważ może wystąpić ciężka hipokaliemia.
Kionex nie jest całkowicie selektywny dla potasu i podczas leczenia może dojść do utraty niewielkich ilości innych kationów, takich jak magnez i wapń. Należy monitorować stężenie wapnia i magnezu u pacjentów otrzymujących lek Kionex.
Przeciążenie płynami u pacjentów wrażliwych na wysokie spożycie sodu
Każda dawka 15 g leku Kionex zawiera 1500 mg (60 mEq) sodu. Należy monitorować pacjentów wrażliwych na spożycie sodu (niewydolność serca, nadciśnienie tętnicze, obrzęki) pod kątem objawów przeciążenia płynami. Może być wymagane dostosowanie innych źródeł sodu.
Ryzyko aspiracji
Zgłaszano przypadki ostrego zapalenia oskrzeli lub zapalenia oskrzelowo-płucnego spowodowane wdychaniem cząstek polistyrenu sulfonianu sodu. Pacjenci z osłabionym odruchem wymiotnym, zmienionym poziomem świadomości lub pacjenci ze skłonnością do regurgitacji mogą być narażeni na zwiększone ryzyko. Kionex należy podawać pacjentowi w pozycji pionowej.
Wiązanie z innymi lekami podawanymi doustnie
Kionex może wiązać się z lekami podawanymi doustnie, co może zmniejszać ich wchłanianie z przewodu pokarmowego i prowadzić do zmniejszenia skuteczności. Inne leki doustne należy podawać co najmniej 3 godziny przed lub 3 godziny po podaniu leku Kionex. Pacjenci z gastroparezą mogą wymagać 6-godzinnego odstępu. .
Działania niepożądane
Następujące działania niepożądane są omówione w innym miejscu etykiety:
– Martwica jelit – Zaburzenia elektrolitowe – Aspiracja
Następujące działania niepożądane zostały zidentyfikowane podczas stosowania produktu Kionex po jego zatwierdzeniu. Ponieważ reakcje te są zgłaszane dobrowolnie przez populację o niepewnej wielkości, nie zawsze jest możliwe wiarygodne oszacowanie ich częstości lub ustalenie związku przyczynowego z ekspozycją na lek.
Przewód pokarmowy: brak łaknienia, zaparcia, biegunka, zaburzenia oddawania stolca, konkrecje żołądkowo-jelitowe (bezoary), niedokrwienne zapalenie jelita grubego, nudności, owrzodzenia, wymioty, podrażnienie żołądka, niedrożność jelit (ze względu na stężenie wodorotlenku glinu)
Metabolizm: alkaloza ogólnoustrojowa
Interakcje lekowe
Interakcje ogólne
Nie przeprowadzono formalnych badań interakcji lekowych u ludzi.
Kionex ma potencjał wiązania się z innymi lekami. W badaniach wiązania in vitro wykazano, że Kionex wiąże w znacznym stopniu leki doustne (n=6), które były badane. Zgłaszano również zmniejszone wchłanianie litu i tyroksyny podczas jednoczesnego stosowania leku Kionex. Wiązanie leku Kionex z innymi lekami doustnymi może powodować zmniejszenie wchłaniania z przewodu pokarmowego i utratę skuteczności, jeśli lek jest przyjmowany blisko terminu podania leku Kionex. Kionex należy podawać co najmniej 3 godziny przed lub 3 godziny po podaniu innych leków doustnych. Pacjenci z gastroparezą mogą wymagać 6-godzinnego odstępu. W miarę możliwości należy monitorować odpowiedź kliniczną i (lub) stężenie leku we krwi.
Przeciwskazania do wymiany kationów
Równoczesne doustne podawanie produktu leczniczego Kionex z niewchłanialnymi przeciwskazaniami do wymiany kationów i środkami przeczyszczającymi może zmniejszyć zdolność żywicy do wymiany potasu i zwiększyć ryzyko zasadowicy ogólnoustrojowej.
Sorbitol
Sorbitol może przyczyniać się do ryzyka martwicy jelit i nie zaleca się jego jednoczesnego stosowania.
STOSOWANIE W SZCZEGÓLNYCH POPULACJACH
Ciąża
Podsumowanie ryzyka
Kionex nie jest wchłaniany ogólnoustrojowo po podaniu doustnym lub doodbytniczym i nie oczekuje się, aby stosowanie u matki powodowało ryzyko dla płodu.
Laktacja
Podsumowanie ryzyka
Kionex nie jest wchłaniany ogólnoustrojowo przez matkę, dlatego nie oczekuje się, że karmienie piersią spowoduje ryzyko dla niemowlęcia.
Stosowanie u dzieci
Badania dotyczące bezpieczeństwa i skuteczności nie zostały przeprowadzone u pacjentów pediatrycznych.
W przypadku pacjentów pediatrycznych, podobnie jak u dorosłych, oczekuje się, że produkt leczniczy Kionex będzie wiązał potas w praktycznym stosunku wymiany 1 mEq potasu na 1 gram żywicy.
W przypadku noworodków produkt leczniczy Kionex nie powinien być podawany drogą doustną. Zarówno u dzieci, jak i u noworodków, nadmierna dawka lub nieodpowiednie rozcieńczenie może spowodować kolizję z żywicą. U wcześniaków lub niemowląt o małej masie urodzeniowej może wystąpić zwiększone ryzyko wystąpienia działań niepożądanych ze strony przewodu pokarmowego podczas stosowania produktu leczniczego Kionex. stosowanie .
Przedawkowanie
Przedawkowanie może spowodować zaburzenia elektrolitowe, w tym hipokaliemię, hipokalcemię i hipomagnezemię. Należy podjąć odpowiednie środki w celu skorygowania stężenia elektrolitów w surowicy (potasu, wapnia, magnezu), a żywica powinna zostać usunięta z przewodu pokarmowego poprzez odpowiednie zastosowanie środków przeczyszczających lub lewatyw.
Kionex Opis
Kionex jest benzenem, diethenyl-polimerem, z etylobenzenem, sulfonowanym, solą sodową i ma następujący wzór strukturalny:
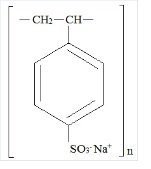
Lek jest kremową do jasnobrązowej, drobno zmieloną, sproszkowaną postacią polistyrenosulfonianu sodu, żywicą kationowymienną przygotowaną w fazie sodowej o zdolności wymiany in vitro około 3.1 mEq (in vivo około 1 mEq) potasu na gram. Zawartość sodu wynosi około 100 mg (4,1 mEq) na gram leku. Może być podawany doustnie lub doodbytniczo w postaci lewatywy.
Jeden gram leku Kionex zawiera 4,1 mEq sodu.
Kionex – Farmakologia kliniczna
Mechanizm działania
Kionex jest niewchłanianym, kationowym polimerem wymiennym, który zawiera przeciwjon sodu.
Kionex zwiększa wydalanie potasu z kałem poprzez wiązanie potasu w świetle przewodu pokarmowego. Wiązanie potasu zmniejsza stężenie wolnego potasu w świetle przewodu pokarmowego, powodując zmniejszenie stężenia potasu w surowicy. Praktyczny współczynnik wymiany wynosi 1 mEq K na 1 gram żywicy.
Jak żywica przechodzi wzdłuż jelita lub jest zatrzymywana w okrężnicy po podaniu w lewatywie, jony sodu są częściowo uwalniane i są zastępowane przez jony potasu. Działanie to zachodzi przede wszystkim w jelicie grubym, które wydala jony potasu w większym stopniu niż jelito cienkie. Skuteczność tego procesu jest ograniczona i nieprzewidywalnie zmienna.
Farmakodynamika
Skuteczne obniżenie stężenia potasu w surowicy za pomocą leku Kionex może trwać od kilku godzin do kilku dni.
Farmakokinetyka
Wydajność in vivo żywic sodowo-potasowych wynosi około 33 procent; w związku z tym do organizmu dostarczana jest około jedna trzecia rzeczywistej zawartości sodu w żywicy.
Kionex nie jest wchłaniany ogólnoustrojowo.
Interakcje z lekami
W badaniach wiązania in vitro wykazano, że Kionex wiązał się znacząco z następującymi badanymi lekami – warfaryną, metoprololem, fenytoiną, furosemidem, amlodypiną i amoksycyliną.
Toksykologia niekliniczna
Karcynogeneza, mutageneza, upośledzenie płodności
Badania nie zostały przeprowadzone.
Jak dostarczyć/ Przechowywanie i postępowanie
Kionex jest dostępny w postaci kremowego do jasnobrązowego, drobno zmielonego proszku w słoikach o masie 1 funta (454 g), NDC 0574-2004-16.
Przechowywać w temperaturze 20° do 25°C (68° do 77°F).
Informacje dla pacjenta
Interakcje lekowe
Należy poinformować pacjentów przyjmujących inne leki doustne, aby oddzielili dawkowanie leku Kionex o co najmniej 3 godziny (przed lub po)
Tylko na receptę
Pakowane przez
Perrigo
Minneapolis, MN 55427
Revised 08/2017
PACKAGE/LABEL PRINCIPAL DISPLAY PANEL
Rx Only
NDC 0574-2004-16
Kionex®
Sodium Polystyrene Sulfonate for Suspension
DAWKA DLA DOROSŁYCH: 15 g (około 4 łyżeczki do herbaty) jeden do czterech razy na dobę w wodzie. Patrz pełna informacja dotycząca stosowania leku
Efekt musi być dokładnie kontrolowany poprzez częste oznaczanie potasu w surowicy krwi w ciągu każdych 24 godzin. Zawartość sodu około 60 mEq na 15 g.
Zawiesina powinna być świeżo przygotowana i nie powinna być przechowywana dłużej niż 24 godziny. Dozować w szczelnych, odpornych na światło pojemnikach, jak określono w USP.
PRZECHOWYWANIE: Przechowywać w temperaturze 20° do 25°C (68° do 77°F) .
Przeczytać ulotkę dołączoną do opakowania.
454 gramy (1 LB)
| Proszek Kionex sodium polystyrene sulfonate, do sporządzania zawiesiny |
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
|
||||||||||||||||||
Labeler -. Paddock Laboratories, LLC (967694121)
Więcej o Kionex (sodium polystyrene sulfonate)
- Sposoby użycia
- W czasie ciąży i karmienia piersią
- Informacje o dawkowaniu
- Interakcje lekowe
- En Español
- 4 Reviews
- Klasa leków: żywice kationowymienne
- Alerty FDA (2)
Zasoby dla konsumentów
- Informacje dla pacjentów
- Kionex (Lektura zaawansowana)
.
Zasoby dla profesjonalistów
- Informacje dla pacjentów
- Sodium Polystyrene Sulfonate Oral Powder (FDA)
Inne marki Kayexalate, Kalexate
Przewodniki dotyczące leczenia
- Hyperkalemia
Zastrzeżenia medyczne
.