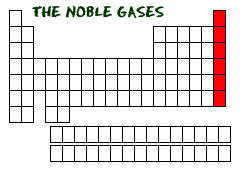
 Vi älskar ädelgaserna. Vissa forskare brukade kalla dem för de inerta gaserna. Det fungerade inte riktigt eftersom det finns några andra gaser som i princip är inerta men inte ädelgaser. Kväve (N2) kan betraktas som en inert gas, men det är ingen ädelgas. Ädelgaserna är en annan familj av grundämnen, och alla ligger i den yttersta högra kolumnen i det periodiska systemet. För alla ni blivande kemister är den längst till höger också känd som grupp noll (grupp 0) eller grupp arton (grupp XVIII). Denna familj har de lyckligaste grundämnena av alla.
Vi älskar ädelgaserna. Vissa forskare brukade kalla dem för de inerta gaserna. Det fungerade inte riktigt eftersom det finns några andra gaser som i princip är inerta men inte ädelgaser. Kväve (N2) kan betraktas som en inert gas, men det är ingen ädelgas. Ädelgaserna är en annan familj av grundämnen, och alla ligger i den yttersta högra kolumnen i det periodiska systemet. För alla ni blivande kemister är den längst till höger också känd som grupp noll (grupp 0) eller grupp arton (grupp XVIII). Denna familj har de lyckligaste grundämnena av alla.
Om man använder Bohrs beskrivning av elektronskal har lyckliga atomer fulla skal. Alla ädelgaser har fulla yttre skal med åtta elektroner. Åh, vänta! Det är inte helt korrekt. I toppen av ädelgaserna finns det lilla helium (He), med ett fullt skal med endast två elektroner. Att deras yttre skal är fullt betyder att de är ganska nöjda och inte behöver reagera med andra grundämnen. Faktum är att de sällan kombineras med andra grundämnen. Denna icke-reaktivitet är anledningen till att de kallas inerta.
Vem tillhör familjen?
 Alla grundämnen i grupp noll är ädelgaser. Listan omfattar helium, neon (Ne), argon (Ar), krypton (Kr), xenon (Xe) och radon (Rn). Tro inte att vi inte använder dessa grundämnen eftersom de inte gillar att reagera. Du hittar ädelgaser över hela vår värld. Neon används i reklamskyltar. Argon används i glödlampor. Helium används i ballonger och för att kyla saker. Xenon används i strålkastare på nya bilar. På grund av sina kemiska egenskaper används dessa gaser också i laboratoriet för att hjälpa till att stabilisera reaktioner som vanligtvis skulle gå för snabbt. När du rör dig nedåt i det periodiska systemet blir grundämnena mer sällsynta i takt med att atomnumren ökar. De är inte bara sällsynta i naturen, utan även sällsynta som användbara grundämnen.
Alla grundämnen i grupp noll är ädelgaser. Listan omfattar helium, neon (Ne), argon (Ar), krypton (Kr), xenon (Xe) och radon (Rn). Tro inte att vi inte använder dessa grundämnen eftersom de inte gillar att reagera. Du hittar ädelgaser över hela vår värld. Neon används i reklamskyltar. Argon används i glödlampor. Helium används i ballonger och för att kyla saker. Xenon används i strålkastare på nya bilar. På grund av sina kemiska egenskaper används dessa gaser också i laboratoriet för att hjälpa till att stabilisera reaktioner som vanligtvis skulle gå för snabbt. När du rör dig nedåt i det periodiska systemet blir grundämnena mer sällsynta i takt med att atomnumren ökar. De är inte bara sällsynta i naturen, utan även sällsynta som användbara grundämnen.
Men vänta, de binder ju varandra!
Vissa gör det. Sedan ungefär 40 år tillbaka har forskare kunnat göra vissa föreningar med ädelgaser. Vissa har använts i föreningar för att göra sprängämnen, och andra bildar bara föreningar i ett labb. Det man ska komma ihåg är att de var tvungna. När de går runt i sitt naturliga liv kommer du aldrig (ja, säg aldrig aldrig, för det kan finnas ett undantag) att hitta ädelgaserna bundna till andra grundämnen.
Relaterad video…
Wikipedia: Ädelgaser
Encyclopedia.com: Ädelgaser: Ädelgaser