Autoreglering av cerebralt blodflöde
Autoreglering av cerebralt blodflöde är hjärnans förmåga att upprätthålla ett relativt konstant blodflöde trots förändringar i perfusionstrycket . Autoreglering finns i många kärlbäddar, men är särskilt välutvecklad i hjärnan, sannolikt på grund av behovet av en konstant blodtillförsel och vattenhomeostas. Hos normotensiva vuxna bibehålls det cerebrala blodflödet på ~50 ml per 100 g hjärnvävnad per minut, förutsatt att CPP ligger i intervallet ~60-160 mmHg . Över och under denna gräns går autoregleringen förlorad och det cerebrala blodflödet blir linjärt beroende av det genomsnittliga arteriella trycket. När CPP sjunker under den nedre gränsen för autoreglering uppstår cerebral ischemi . Minskningen av det cerebrala blodflödet kompenseras av ett ökat syreuttag från blodet . Kliniska tecken eller symtom på ischemi ses inte förrän minskningen av perfusionen överstiger förmågan hos det ökade syreuttaget att tillgodose de metaboliska behoven. Vid denna tidpunkt uppträder kliniska tecken på hypoperfusion, inklusive yrsel, förändrat mentalt tillstånd och slutligen irreversibel vävnadsskada (infarkt) .
Mekanismerna för autoreglering i hjärnan är inte helt förstådda och skiljer sig troligen åt vid ökningar jämfört med minskningar av trycket. Även om en roll för neuronal inblandning i autoregleringen är tilltalande har studier visat att autoregleringen av det cerebrala blodflödet är bevarad hos sympatiskt och parasympatiskt denerverade djur, vilket tyder på att det är osannolikt att extrinsiska neurogena faktorer i hög grad bidrar till autoregleringen av det cerebrala blodflödet (se Perivaskulär Innervation). Nyligen har man visat att neuronal kväveoxid spelar en roll för att modulera autoregleringen av det cerebrala blodflödet, vilket tyder på att även om extrinsisk innervation kanske inte är inblandad, kan intrinsisk innervation ha en roll . Biprodukter från ämnesomsättningen har också föreslagits ha en roll i autoregleringen . Minskat cerebralt blodflöde stimulerar frisättning av vasoaktiva ämnen från hjärnan som orsakar arteriell dilatation. Kandidater för dessa vasoaktiva ämnen är H+, K+, O2, adenosin och andra. Autoreglering av det cerebrala blodflödet när trycket fluktuerar i den övre delen av den autoreglerande kurvan beror sannolikt på det myogena beteendet hos den glatta muskulaturen i hjärnan som drar ihop sig vid förhöjt tryck och utvidgar sig vid sänkt tryck . Den myogena aktivitetens viktiga bidrag till autoregulationen har visats in vitro i isolerade och trycksatta hjärnartärer som drar ihop sig vid ökat tryck och utvidgar sig vid minskat tryck (se Myogena reaktioner). Autoregulering vid tryck under det myogena tryckområdet inbegriper sannolikt hypoxi och frisättning av metaboliska faktorer .
Autoreguleringens betydelse för normal hjärnfunktion framhävs av det faktum att betydande hjärnskador uppstår när de autoregulatoriska mekanismerna går förlorade. Vid akut hypertoni vid tryck över den autoregulatoriska gränsen övervinns till exempel den myogena sammandragningen av den glatta kärlmuskulaturen av det överdrivna intravaskulära trycket och det sker en forcerad utvidgning av hjärnans kärl . Förlusten av myogenisk tonus under den forcerade dilatationen minskar det cerebrovaskulära motståndet, vilket kan ge en stor ökning av det cerebrala blodflödet (300-400 %), som kallas autoregulatoriskt genombrott (figur 16). Dessutom ökar det minskade cerebrovaskulära motståndet det hydrostatiska trycket på det cerebrala endotelet, vilket orsakar ödembildning , den underliggande orsaken till tillstånd som hypertensiv encefalopati, posteriort reversibelt encefalopatisyndrom (PRES) och eklampsi (se Vasogen ödembildning).
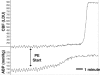
FIGUR 16
Spårning av CBF (i laserdopplerenheter) och ABP (i mmHg) som svar på ökande doser av PE. I detta experiment ökade CBF fyra gånger mer än baslinjen när ABP ökade från 140 till 210 mmHg, vilket visar på ett autoregulatoriskt genombrott. Används (mer…)
Och även om det är ovanligt sedan tillkomsten av effektiv antihypertensiv behandling, inträffar hypertensiv encefalopati som ett resultat av en plötslig, ihållande ökning av blodtrycket som är tillräcklig för att överskrida den övre gränsen för autoregulering av det cerebrala blodflödet (>160 mmHg) . Tidiga studier av hjärnkärlens reaktion på högt blodtryck gav upphov till begreppet hypertensiv vasospasm. Akut hypertensiv encefalopati ansågs vara resultatet av spasm – definierat som en okontrollerad vasokonstriktion – i de cerebrala artärerna, vilket orsakade ischemi i hjärnvävnaden . Detta begrepp har sitt ursprung i observationer av Byrom, som framställde experimentell njurhypertension och fann att ~90 % av hypertensiva råttor med neurologiska manifestationer uppvisade flera kortikala fläckar av trypanblå extravasering, medan råttor utan cerebrala symtom tycktes ha normal cerebrovaskulär permeabilitet. Han noterade också vad han kallade en omväxlande vasokonstriktion/vasodilatation i pialkärlen, ett fenomen som är känt som ett ”korvbandsutseende”. Denna observation ledde honom till slutsatsen att cerebral vasospasm orsakade ischemi och ödembildning som svar på akut hypertoni. Byrom ändrade senare sin uppfattning och hänvisade till ett fynd i mesenterialcirkulationen där kärl med detta ”korvbandsutseende” hade proteinläckage endast i de dilaterade delarna av kärlen . Sedan dess har det fastställts att högt blodtryck resulterar i ökat cerebralt blodflöde och ”genombrott av autoregulationen” . Ytterligare experiment bekräftade att förlust av myogenisk vasokonstriktion under forcerad dilatation snarare än spasm är den kritiska händelsen vid hypertensiv encefalopati.