Lärandemål
I slutet av det här avsnittet kommer du att kunna:
- Ange materiens vanliga faser.
- Förklara de fysiska egenskaperna hos fasta ämnen, vätskor och gaser.
- Beskriv hur atomerna är placerade i fasta ämnen, vätskor och gaser.

Figur 1. (a) Atomer i ett fast ämne har alltid samma grannar, som hålls nära hemmet av krafter som här representeras av fjädrar. Dessa atomer är i huvudsak i kontakt med varandra. En sten är ett exempel på ett fast ämne. Denna sten behåller sin form på grund av de krafter som håller ihop dess atomer. (b) Atomer i en vätska är också i nära kontakt men kan glida över varandra. Krafter mellan dem motstår starkt försök att trycka dem närmare varandra och håller dem också i nära kontakt. Vatten är ett exempel på en vätska. Vatten kan flyta, men det förblir också i en öppen behållare på grund av krafterna mellan dess atomer. (c) Atomer i en gas är åtskilda av avstånd som är betydligt större än atomernas egen storlek, och de rör sig fritt. En gas måste hållas i en sluten behållare för att förhindra att den rör sig fritt ut.
Atomer i fasta ämnen är i nära kontakt med varandra, med krafter mellan dem som gör att atomerna kan vibrera men inte byta position med grannatomer. (Dessa krafter kan ses som fjädrar som kan sträckas eller komprimeras, men som inte lätt kan brytas). På så sätt motstår ett fast ämne alla typer av påfrestningar. Ett fast ämne kan inte lätt deformeras eftersom atomerna som utgör det fasta ämnet inte kan röra sig fritt. Fasta ämnen står också emot kompression, eftersom deras atomer ingår i en gitterstruktur där atomerna befinner sig på ett relativt fast avstånd från varandra. Vid kompression skulle atomerna tvingas in i varandra. De flesta av de exempel vi har studerat hittills har gällt fasta föremål som deformeras mycket lite när de utsätts för påfrestningar.
Samband: Submikroskopisk förklaring av fasta ämnen och vätskor
Vätskor deformeras däremot lätt när de utsätts för påfrestningar och återgår inte till sin ursprungliga form när kraften försvinner, eftersom atomerna är fria att glida runt och byta grannar – det vill säga de flyter (så de är en typ av vätska), med molekylerna som hålls samman av sin ömsesidiga attraktion. När en vätska placeras i en behållare utan lock förblir den i behållaren (förutsatt att behållaren inte har några hål under vätskeytan!). Eftersom atomerna är tätt packade motstår vätskor, liksom fasta ämnen, kompression.
Atomer i gaser är åtskilda med avstånd som är stora jämfört med atomernas storlek. Krafterna mellan gasatomer är därför mycket svaga, utom när atomerna kolliderar med varandra. Gaser flyter alltså inte bara (och anses därför vara vätskor) utan de är också relativt lätta att komprimera eftersom det finns mycket utrymme och få krafter mellan atomerna. När gaser placeras i en öppen behållare kommer de, till skillnad från vätskor, att flyga ut. Den stora skillnaden är att gaser är lätta att komprimera, medan vätskor inte är det. Vi kommer i allmänhet att referera till både gaser och vätskor helt enkelt som vätskor, och göra en åtskillnad mellan dem endast när de beter sig olika.
PhET Explorations:
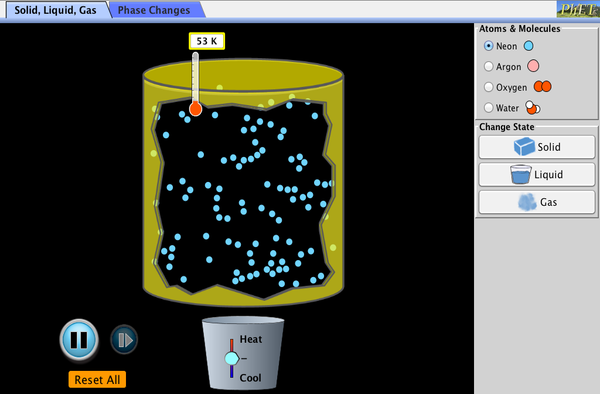
Klicka för att ladda ner simuleringen. Kör med Java.
Avsnittssammanfattning
- En vätska är ett tillstånd av materia som ger efter för sido- eller skjuvkrafter. Både vätskor och gaser är vätskor. Fluidstatik är fysiken för stationära vätskor.
Begreppsfrågor
1. Vilken fysikalisk egenskap skiljer en vätska från ett fast ämne?
2. Vilka av följande ämnen är vätskor vid rumstemperatur: luft, kvicksilver, vatten, glas?
3. Varför är gaser lättare att komprimera än vätskor och fasta ämnen?
4. Hur skiljer sig gaser från vätskor?
Förklaringsordlista
vätskor: vätskor och gaser; en vätska är ett materiatillstånd som ger efter för skjuvkrafter
.