Autoreglarea fluxului sanguin cerebral
Autoreglarea fluxului sanguin cerebral este capacitatea creierului de a menține un flux sanguin relativ constant în ciuda modificărilor presiunii de perfuzie . Autoreglarea este prezentă în multe paturi vasculare, dar este deosebit de bine dezvoltată în creier, probabil din cauza necesității unei aprovizionări constante cu sânge și a homeostaziei apei. La adulții normotensivi, fluxul sanguin cerebral este menținut la ~50 ml per 100 g de țesut cerebral pe minut, cu condiția ca CPP să fie cuprinsă între ~60 și 160 mmHg . Peste și sub această limită, autoreglarea este pierdută și fluxul sanguin cerebral devine dependent de presiunea arterială medie în mod liniar . Atunci când CPP scade sub limita inferioară a autoreglației, are loc ischemia cerebrală . Reducerea fluxului sanguin cerebral este compensată de o creștere a extracției de oxigen din sânge . Semnele sau simptomele clinice ale ischemiei nu sunt observate până când scăderea perfuziei depășește capacitatea extracției crescute de oxigen de a satisface nevoile metabolice. În acest moment, apar semne clinice de hipoperfuzie, inclusiv amețeli, alterarea stării mentale și, în cele din urmă, leziuni tisulare ireversibile (infarct) .
Mecanismele autoreglației în creier nu sunt complet înțelese și probabil diferă în cazul creșterilor față de scăderile de presiune. Deși un rol al implicării neuronale în autoregulație este atrăgător, studiile au arătat că autoregulația fluxului sanguin cerebral este păstrată la animalele denervate simpatic și parasimpatic, ceea ce indică faptul că o contribuție majoră a factorilor neurogeni extrinseci la autoregulația fluxului sanguin cerebral este puțin probabilă (vezi Inervația perivasculară). Recent, a fost demonstrat un rol al oxidului nitric neuronal în modularea autoreglației fluxului sanguin cerebral, sugerând că, deși este posibil ca inervația extrinsecă să nu fie implicată, inervația intrinsecă poate avea un rol . S-a propus, de asemenea, ca biprodusele metabolismului să aibă un rol în autoreglare . Reducerile fluxului sanguin cerebral stimulează eliberarea de substanțe vasoactive din creier care determină dilatarea arterială. Printre candidații pentru aceste substanțe vasoactive se numără H+, K+, O2, adenozina și altele. Autoreglarea fluxului sanguin cerebral atunci când presiunea fluctuează la capătul înalt al curbei autoregulatoare se datorează, cel mai probabil, comportamentului miogen al mușchilor netezi cerebrali care se contractă ca răspuns la presiune ridicată și se dilată ca răspuns la scăderea presiunii . Contribuția importantă a activității miogenice la autoreglare este demonstrată in vitro în arterele cerebrale izolate și presurizate care se contractă ca răspuns la creșterea presiunii și se dilată ca răspuns la scăderea presiunii (a se vedea Răspunsul miogenic). Autoreglarea la presiuni sub intervalul de presiune miogenică implică probabil hipoxia și eliberarea de factori metabolici .
Importanța autoreglementării în funcționarea normală a creierului este evidențiată de faptul că leziuni cerebrale semnificative apar atunci când mecanismele autoregulatoare sunt pierdute. De exemplu, în timpul hipertensiunii acute la presiuni peste limita autoreglării, constricția miogenă a musculaturii netede vasculare este depășită de presiunea intravasculară excesivă și are loc dilatarea forțată a vaselor cerebrale . Pierderea tonusului miogenic în timpul dilatației forțate scade rezistența cerebrovasculară, rezultat care poate produce o creștere mare a fluxului sanguin cerebral (300-400%), cunoscută sub numele de pătrundere autoreglementatoare (figura 16). În plus, scăderea rezistenței cerebrovasculare crește presiunea hidrostatică asupra endoteliului cerebral, provocând formarea edemului , cauza care stă la baza unor afecțiuni precum encefalopatia hipertensivă, sindromul de encefalopatie reversibilă posterioară (PRES) și eclampsia (a se vedea Formarea edemului vasogenic).
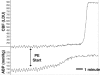
FIGURA 16
Tractarea CBF (în unități Doppler laser) și ABP (în mmHg) ca răspuns la doze crescânde de PE. În acest experiment, CBF a crescut de patru ori mai mult decât valoarea inițială pe măsură ce ABP a crescut de la 140 la 210 mmHg, demonstrând pătrunderea autoreglatoare. Folosit (more…)
Deși mai puțin frecvente de la apariția terapiei antihipertensive eficiente, encefalopatia hipertensivă apare ca urmare a unei creșteri bruște și susținute a tensiunii arteriale suficiente pentru a depăși limita superioară a autoreglației fluxului sanguin cerebral (>160 mmHg) . Studiile timpurii privind reacția vaselor cerebrale la tensiunea arterială ridicată au produs conceptul de vasospasm hipertensiv. Se credea că encefalopatia hipertensivă acută este rezultatul spasmului -;definit ca o vasoconstricție necontrolată-;al arterelor cerebrale, provocând ischemia țesutului cerebral . Acest concept își are originea în observațiile lui Byrom, care a produs hipertensiune renală experimentală și a constatat că ~90% dintre șobolanii hipertensivi cu manifestări neurologice prezentau multiple pete corticale de extravazare a albastru trypan, în timp ce șobolanii fără simptome cerebrale păreau să aibă o permeabilitate cerebrovasculară normală. El a observat, de asemenea, ceea ce a numit o alternanță de vasoconstricție/vasodilatație în vasele piale, un fenomen cunoscut sub numele de aspect de „șir de cârnați”. Această observație l-a condus la concluzia că vasospasmul cerebral a cauzat ischemia și formarea edemului ca răspuns la hipertensiunea acută. Ulterior, Byrom și-a modificat opinia și s-a referit la o constatare făcută în circulația mezenterică, conform căreia vasele cu acest aspect de „sfoară de cârnat” prezentau scurgeri de proteine doar în părțile dilatate ale vaselor . De atunci, s-a stabilit că tensiunea arterială ridicată are ca rezultat creșterea fluxului sanguin cerebral și „spargerea autoreglației” . Alte experimente au confirmat că pierderea vasoconstricției miogenice în timpul dilatației forțate, mai degrabă decât spasmul, este evenimentul critic în encefalopatia hipertensivă .
.