Câțiva atomi sunt mai polari decât alții datorită faptului că sunt mai „lacomi” de electroni.
Aruncă o privire la tabelul periodic, cu cât mergi mai la dreapta și mai sus, cu atât atomii devin mai electronegativi (fără a include gazele nobile, deoarece acestea au învelișurile pline și sunt „fericite” și nu au nevoie de electroni de valență).
Cred că toată lumea a auzit că Floarea (F), de exemplu, este unul dintre cele mai electronegative elemente, va smulge literalmente electroni de la atomii de Hidrogen sau de la atomii de carbon. La fel va face și Clorul (Cl)
Vezi această imagine:
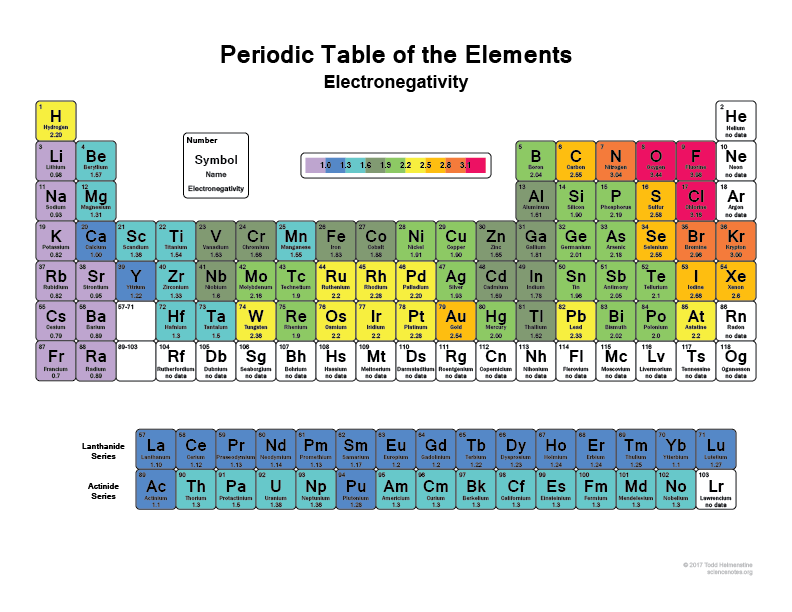
De aceea, atunci când o legătură, unele molecule au regiuni super polare, deoarece au ceva precum Hidrogenul care se leagă cu ceva precum Făina care, practic, are doar electronii cu ea în cea mai mare parte a timpului.
Această întrebare poate fi, de asemenea, explicată prin ideea de nori de electroni și prin faptul că atomii mai electronegativi vor avea, de obicei, mai mulți electroni care rămân cu ei în cea mai mare parte a timpului față de atomii mai puțin electronegativi.

Aceasta se numește moment dipolar și fără a intra prea mult în detalii, vedeți cum majoritatea electronilor sunt mai aproape de oxigen decât de hidrogen (pentru că oxigenul este mai electronegativ decât hidrogenul)
Apropo, cuvântul „electronegativ” sună uneori contraintuitiv, dar este electro-negativ în loc de pozitiv, deoarece în chimie atomii care câștigă electroni au un semn negativ (Ex: #Cl^-# este un clor care a câștigat un electron).