El objetivo principal del trasplante de páncreas es mejorar la diabetes mellitus insulinodependiente (tipo 1 o tipo 2) y producir una independencia total de la insulina inyectada. El trasplante simultáneo de páncreas y riñón (SPK) (véase la imagen de abajo) es la principal opción si el paciente tiene también nefropatía diabética y cumple los requisitos para ser incluido en la lista de trasplantes de riñón. El primer trasplante de páncreas en humanos junto con un trasplante de riñón se realizó con éxito en la Universidad de Minnesota por el Dr. William Kelly y el Dr. Richard Lilleheiat la Universidad de Minnesota. En 2015 se realizaron 947 trasplantes de páncreas en Estados Unidos.
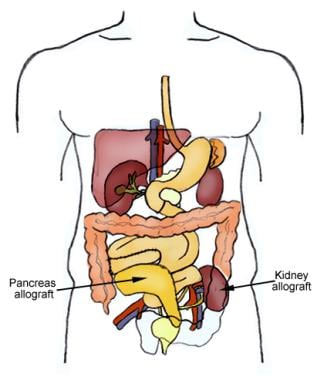 Colocación de aloinjertos de riñón y páncreas
Colocación de aloinjertos de riñón y páncreas Se calcula que 30,3 millones de personas -el 9,4% del total de la población de Estados Unidos- tienen diabetes mellitus. Sin embargo, 1 de cada 4 adultos afectados desconoce que tiene diabetes, y de los 84,1 millones de adultos estadounidenses con prediabetes, sólo el 11,6% es consciente de su condición. La nefropatía diabética es la principal causa de enfermedad renal crónica en los EE.UU., y cada año, más de 50.000 personas desarrollan una enfermedad renal terminal (ESRD) con la diabetes como causa principal.
Este artículo se centra principalmente en el trasplante de páncreas. Para una discusión completa del trasplante de riñón, consulte Trasplante renal pediátrico y Trasplante renal.
Formas de trasplante de páncreas
Un páncreas de un donante puede utilizarse para la terapia de sustitución endocrina de una de las siguientes maneras:
1. Trasplante de páncreas solo (PTA): Indicado para pacientes con diabetes tipo 1 que presentan episodios frecuentes de hipoglucemia con o sin desconocimiento, deterioro de la calidad de vida u otros problemas de tolerancia a la terapia con insulina. Estos pacientes tienen una función renal adecuada y el trasplante de riñón no está indicado.
2. Trasplante de SPK: Los órganos proceden del mismo donante. El uso principal ha sido en pacientes con diabetes tipo 1 que tienen una tasa de filtración glomerular estimada (TFGe) de 2</sup> o están en tratamiento de sustitución renal.
3. Páncreas tras trasplante de riñón (PAK): Trasplante de páncreas de donante fallecido tras un trasplante renal previo; las indicaciones son similares a las de la ATP
4. Trasplante de células de los islotes pancreáticos: Ofrece una menor morbilidad pero resultados inferiores a largo plazo en comparación con el trasplante de órgano sólido (páncreas).
Alrededor del 80% de los trasplantes de páncreas se realizan como un trasplante SPK. Aproximadamente el 10% de los trasplantes de páncreas se realizan como un trasplante PAK después de un trasplante renal previamente exitoso de un donante vivo o fallecido. Los casos restantes se realizan como PTA. En 2015, se realizaron 80 PTA en los Estados Unidos.
El trasplante de páncreas y de islotes pueden considerarse opciones de trasplante complementarias y someterse a uno u otro no es excluyente. En un análisis de 40 trasplantes de páncreas (50% PTA, 27,5% SPK, 22,5% PAK) tras el fracaso del injerto de células de islotes, las tasas de supervivencia global (97% a 1 año y 83% a 5 años) no se vieron afectadas negativamente.
Pruebas de evaluación del trasplante
En la evaluación de un paciente para el trasplante de SPK, la cuantificación de las necesidades diarias de insulina y los niveles séricos de péptido C en ayunas se utilizan para determinar el tipo de diabetes presente, la gravedad de la resistencia a la insulina y el posible beneficio del trasplante de páncreas. Un paciente muy resistente a la insulina tendrá unas necesidades elevadas de insulina (>1-1,5 unidades/kg) y un nivel elevado de péptido C en ayunas (>4 ng/mL). Estos pacientes podrían seguir siendo dependientes de la insulina a pesar de un trasplante de páncreas.
Sin embargo, estos valores deben considerarse dentro del cuadro clínico general. Por ejemplo, un paciente en diálisis peritoneal con un dializador que contiene dextrosa tendrá mayores necesidades de insulina que disminuirán una vez que el trasplante de riñón elimine la necesidad de diálisis. El péptido C no es un marcador exacto en los pacientes con enfermedad renal crónica, ya que su aclaramiento varía en estos pacientes. Además, en un paciente que está tomando insulina, el nivel de péptido C será falsamente bajo si la muestra se extrae cuando el paciente está hipoglucémico; por lo tanto, el resultado del péptido C debe interpretarse a la luz de una medición concomitante de la glucosa.
Se debe medir la hemoglobina A1C, para evaluar la gravedad de la diabetes del paciente.
Si el paciente tiene una diabetes de tipo 1, se debe considerar la evaluación basal de los marcadores autoinmunes, incluidos los anticuerpos contra la descarboxilasa del ácido glutámico. Un aumento en el nivel de anticuerpos después del trasplante de páncreas sugeriría una posible disfunción del injerto de páncreas e hiperglucemia debido a una reacción autoinmune en lugar de un rechazo.
Indicciones y contraindicaciones
El número de trasplantes de páncreas ha disminuido cada año desde 2004, cuando se realizaron aproximadamente 1500; en 2016 se realizaron 181 trasplantes de páncreas. El trasplante multiorgánico más común es el de riñón-páncreas, con casi 23.000 realizados entre 1988 y 2017. En 2016 se realizaron 795 trasplantes de SPK. Los pacientes con diabetes tipo 2 constituyeron el 12,5% de los trasplantes de SPK.
La Red Unida de Distribución de Órganos (UNOS) incluirá en la lista a un posible candidato a trasplante de páncreas si el paciente cumple uno de los siguientes criterios de elegibilidad :
-
Insulinodependiente con un péptido C de 2 ng/mL o menos (pacientes con diabetes tipo 1)
-
Insulinodependiente con un péptido C-péptido mayor de 2 ng/mL y un índice de masa corporal de 2</sup> (presumiblemente pacientes con diabetes tipo 2)
El clínico debe ser consciente del cuadro clínico al interpretar estos valores, como se ha indicado anteriormente.El uso del péptido C es controvertido.
Los siguientes son los criterios para el tipo específico de trasplante de páncreas:
-
PTA – Complicaciones metabólicas frecuentes y agudas, incluyendo hipoglucemia o cetoacidosis, incapacidad para tolerar la terapia con insulina exógena, y persistencia de complicaciones agudas a pesar del tratamiento con insulina
-
SPK – Enfermedad renal terminal y elegibilidad para trasplante de páncreas
-
PAK – Elegibilidad para trasplante de páncreas y un trasplante de riñón previo con éxito
El paciente elegible también tendrá que someterse a una evaluación médica adecuada en particular para la estratificación del riesgo cardiovascular y la enfermedad vascular periférica. También tendrán que mostrar un historial de cumplimiento médico. El límite de edad histórico para el trasplante de páncreas, que algunos centros han seguido empleando, es de 55 años. Sin embargo, el número de receptores de trasplante de páncreas mayores de 55 años ha aumentado constantemente. En 2016, el 24,5% de todos los receptores de trasplante de páncreas eran mayores de 50 años (PTA: 38,3%, SPK: 22,7%, PAK: 25,7%). La supervivencia de los pacientes es comparable para los receptores de trasplante de páncreas más jóvenes y mayores, pero los receptores de mayor edad tuvieron eventos cardiovasculares más frecuentes.
Las contraindicaciones absolutas, como se indica a continuación, son similares a las de otros trasplantes de órganos sólidos:
-
Riesgo cardiovascular excesivo
-
Malignidad activa o infección que tendría que ser tratada y eliminada antes del trasplante
-
Factores de riesgo social elevados como la falta de adherencia a la medicación, la falta de seguro y el consumo de drogas ilícitas
Las contraindicaciones relativas incluyen las siguientes:
-
Índice de masa corporal superior a 30 kg/m 2
-
Necesidad de insulina de >1.5 U/kg al día
-
Enfermedad cerebrovascular, aórtica/ilíaca, cardiovascular o vascular periférica
Beneficios del trasplante de páncreas
Las complicaciones microvasculares de la diabetes están directamente relacionadas con la concentración de glucosa. Por lo tanto, cabe esperar que la normalización de la glucosa mediante un trasplante de páncreas exitoso estabilice o revierta las complicaciones microvasculares. Los beneficios resultantes del trasplante de páncreas y riñón se analizan a continuación.
Retinopatía diabética
La mayoría de los candidatos a trasplante de páncreas han tenido diabetes durante 20-25 años de media antes de ser considerados para el trasplante y, en consecuencia, muchos de ellos se han sometido a cirugía láser para la retinopatía. Este fue un hallazgo común peritransplante en la mayoría de los estudios. La gravedad de estos cambios oftalmológicos puede obviar un claro efecto saludable del trasplante de PTA o SPK sobre la retinopatía.
Los estudios sugieren, sin embargo, que la retinopatía puede mejorar 3 años después del SPK y que la necesidad de más cirugía láser es menor después del SPK que del trasplante de riñón solo (KTA). Se cree que el trasplante de páncreas y el mantenimiento de un estado euglucémico estabilizan como mínimo la retinopatía diabética. Se necesitan ensayos prospectivos para comparar los dos grupos, porque la mayoría de los estudios han carecido de suficientes grupos de control.
Nefropatía diabética
Un número significativo de candidatos a trasplante de páncreas tienen una enfermedad renal avanzada. El escenario más común para el trasplante de páncreas es en combinación con un trasplante de riñón para tratar a pacientes con uremia diabética. La SPK ayudaría a prevenir los efectos deletéreos de la diabetes en el nuevo trasplante de riñón.
Los estudios que comparan la función renal en los receptores de trasplante de SPK frente a los receptores de KTA diabéticos no demostraron diferencias significativas durante el periodo postrasplante temprano. Sin embargo, la nefropatía diabética recurrente se observa ya 2 años después del KTA en un receptor diabético o al fallar el injerto de páncreas después del SPK, pero nunca se ha informado con un trasplante de SPK en funcionamiento. Se ha demostrado que los pacientes con un trasplante de páncreas presentan un retraso en la progresión o reversión de la nefropatía diabética.
Neuropatía diabética
La neuropatía mejora después del trasplante de riñón y páncreas, lo que sugiere que la insuficiencia renal y la diabetes contribuyen a la neuropatía sensorial que se observa habitualmente en el momento del trasplante. Las neuropatías autonómicas, como la gastroparesia, tardan años en desarrollarse y pueden ser difíciles de cuantificar. Sin embargo, se ha informado de una mejora objetiva de los hallazgos neuropáticos autonómicos 4 años después de la SPK y se observa que es mayor después de la SPK que después de la KTA.
Retinopatía diabética
La retinopatía diabética es un hallazgo generalizado en los pacientes con diabetes y ERS. Puede observarse una pérdida de visión/ceguera significativa. La ceguera no es una contraindicación absoluta para el trasplante, ya que muchos pacientes ciegos llevan una vida muy independiente.
Enfermedad cardiovascular
La enfermedad cardiovascular es la causa más común de muerte en pacientes con diabetes con insuficiencia renal. Pocos estudios prospectivos han examinado la relación entre el establecimiento de la normoglucemia en pacientes con diabetes de larga duración y la reducción de la morbilidad y mortalidad cardiovascular. En un estudio transversal, la fracción de eyección del ventrículo izquierdo fue mayor, la relación entre la tasa de llenado máxima y la tasa de eyección máxima fue mayor y la dilatación dependiente del endotelio de la arteria braquial mejoró en los receptores de SPK en comparación con los pacientes con diabetes tipo 1 que recibieron KTA. Otras pruebas demuestran que el trasplante de SPK reduce las tasas de mortalidad cardiovascular con una reducción concomitante de la presión arterial.
Otro estudio observó una mayor disminución de la masa ventricular izquierda y una mayor normalización de la disfunción diastólica en los receptores de SPK que en los que se sometieron a KTA. En este informe, se realizó una ecocardiografía bidimensional (2-D) y en modo M antes y 1 año después del trasplante en receptores de SPK y KTA. Un amplio estudio retrospectivo sugirió una asociación con reducciones en la incidencia de infarto de miocardio, edema pulmonar agudo e hipertensión en los receptores de SPK frente a los de KTA.
La enfermedad arterial coronaria (EAC) es la comorbilidad más importante a considerar en los pacientes con diabetes tipo 1 y nefropatía diabética. Se estima que los pacientes con diabetes y nefropatía diabética tienen un riesgo 50 veces mayor de sufrir eventos cardiovasculares que la población general. La prevalencia de la EAC significativa (>50% de estenosis) en los pacientes con diabetes que inician el tratamiento de la ERS se estima en un 45-55%. Debido a la neuropatía diabética, es posible que los pacientes no experimenten angina durante los episodios de isquemia miocárdica.
Infarto y ataque isquémico transitorio
Los pacientes con ERS y diabetes tienen una mayor tasa de accidentes cerebrovasculares y ataques isquémicos transitorios. Las muertes relacionadas con la enfermedad vascular cerebral en pacientes con ERS son aproximadamente dos veces más frecuentes en los que tienen diabetes que en los que no la tienen. Los accidentes cerebrovasculares se producen con mayor frecuencia y a una edad más temprana en los pacientes con diabetes que en los pacientes no diabéticos emparejados por edad y sexo.
Enfermedad vascular periférica
La enfermedad vascular periférica de las extremidades inferiores es significativa en los pacientes con diabetes. Los pacientes con enfermedad renal terminal corren el riesgo de sufrir la amputación de una extremidad inferior. Estos problemas suelen comenzar con una úlcera en el pie asociada a una neuropatía somatosensorial avanzada.
Neuropatía autonómica
La neuropatía autonómica es prevalente y puede manifestarse como gastropatía, cistopatía e hipotensión ortostática. La magnitud de la neuropatía autonómica diabética suele subestimarse.
La alteración del vaciado gástrico (gastroparesia) es una consideración importante debido a sus implicaciones significativas en el curso postrasplante. Los pacientes con gastroparesia grave pueden tener dificultades para tolerar los medicamentos inmunosupresores orales que son esenciales para prevenir el rechazo de los órganos trasplantados. Los episodios de depleción de volumen con azotemia asociada ocurren con frecuencia en pacientes con trasplantes de SPK. La morbilidad gastrointestinal es una indicación común de reingreso tras el trasplante de páncreas.
La disfunción neurogénica de la vejiga es una consideración importante en los pacientes sometidos a un trasplante de páncreas solo o a un trasplante SPK. La incapacidad de percibir la plenitud de la vejiga y de vaciarla predispone a un elevado residuo postmiccional y a la posibilidad de reflujo vesicoureteral. Esto puede afectar negativamente a la función del aloinjerto renal, aumentar la incidencia de infecciones de la vejiga y pielonefritis, y predisponer a la pancreatitis del injerto.
La combinación de hipotensión ortostática e hipertensión en decúbito es el resultado de la desregulación del tono vascular. Esto tiene implicaciones para el control de la presión arterial tras el trasplante, especialmente en pacientes con trasplantes de páncreas con drenaje vesical que están predispuestos a la depleción de volumen. Por lo tanto, es importante reevaluar cuidadosamente la necesidad de medicación antihipertensiva tras el trasplante.
Neuropatías sensoriales y motoras
Estas afecciones son comunes en pacientes con diabetes de larga duración. Esto puede tener implicaciones para la rehabilitación después del trasplante. La neuropatía periférica es también un indicador de un mayor riesgo de lesiones en los pies y de las subsiguientes úlceras del pie diabético.
Enfermedades mentales o emocionales
Las enfermedades mentales, incluyendo la neurosis y la depresión, son comunes en la población diabética insulinodependiente. El diagnóstico y el tratamiento adecuado de estas enfermedades antes de obtener un trasplante de páncreas pueden mejorar significativamente el cumplimiento médico.
Resultados
La evaluación de las tasas de resultados de los injertos de páncreas se ha visto dificultada por la falta de uniformidad en los criterios de fracaso del injerto. Algunos programas no informan del fracaso del injerto si la producción de péptido C continúa, mientras que otros informan del fracaso del injerto si el receptor ya no es independiente de la insulina. El Comité de Trasplante de Páncreas de la OPTN/UNOS ha propuesto las siguientes definiciones más precisas para el fracaso del injerto de páncreas, que actualmente están pendientes de aplicación :
-
Extirpación del páncreas trasplantado
-
Reinscripción para un trasplante de páncreas
-
Inscripción para un trasplante de islotes tras recibir un trasplante de páncreas
-
Uso de insulina de ≥0.5 unidades/kg/día durante 90 días consecutivos
-
Muerte del receptor
El número de receptores vivos con un aloinjerto de páncreas funcional ha seguido aumentando en la última década y superó los 18.000 en 2016. La mortalidad ha disminuido sistemáticamente entre todos los grupos de trasplante de páncreas como resultado de regímenes inmunosupresores más seguros y eficaces. La mortalidad a un año para el ATP disminuyó del 4,6% en 2012-2013 al 0,8% para los trasplantes realizados en 2014-2015. En el caso de la SPK, las tasas de supervivencia de los pacientes a 5 años fueron similares en los pacientes con diabetes tipo 1 y tipo 2 (90,5% y 91,5% respectivamente), a pesar de la mayor edad y la comorbilidad asociada a la diabetes tipo 2. Esto se debe probablemente a la selección de candidatos con diabetes tipo 2 cuyo estado cardiovascular puede tolerar los altos riesgos operativos.
El mayor riesgo de pérdida del injerto se produce en el primer año tras el trasplante y, en particular, en los primeros 3 meses, independientemente del tipo de trasplante de páncreas. Los análisis de datos del Registro Internacional de Trasplante de Páncreas han utilizado la independencia de la insulina como criterio principal para la supervivencia del injerto. Las mejores tasas de supervivencia del injerto de páncreas con trasplante SPK han sido del 86% al año y del 73% a los 5 años. Los resultados del SPK son superiores a los del trasplante de PAK y PTA. Una ventaja del trasplante SPK es que el rechazo agudo puede detectarse más fácilmente, ya que la creatinina sérica puede utilizarse como marcador.
En el trasplante PAK, las tasas de supervivencia del injerto de páncreas a un año y a 5 años son del 80% y del 58%, respectivamente. En el caso de la ATP, las tasas comparables son del 77% y el 56%.
Las tasas de rechazo agudo son similares para el SPK y el PAK, en torno al 4% para cada uno. La vida media estimada de los injertos ha mejorado a lo largo de los años, ya que la SPK dura unos 14 años, la PAK 7 años y la PTA 7 años.