Download dette nummer Tilbage til oversigt
Steven E. ZIMMET2,3
Austin, USA
ABSTRACT
Endovenøs laserablation (EVLA) er et mindre invasivt alternativ til venestripning. Resultaterne synes at være lige så gode eller bedre end ved stripping, med bedre livskvalitetsscore i den postoperative periode. EVLA har vist sig at kunne korrigere eller væsentligt forbedre hæmodynamisk abnormitet hos patienter med kronisk venøs insufficiens (CVI) med overfladisk venøs refluks. Tidlige rapporter tyder på, at endovenøse ablationsteknikker, i modsætning til kirurgisk stripping, er forbundet med en lav forekomst af neovaskularisering.
Der anvendes en række forskellige bølgelængder til at udføre EVLA. Mens den oprindelige kromofore er vand eller hæmoglobin, afhængigt af den anvendte bølgelængde, synes kulstof at være en sekundær, men vigtig kromofore, som sandsynligvis er uafhængig af bølgelængden.
Anvendelsen af principperne for tumescentanæstesi på venøse behandlinger giver sammen med udviklingen af endovenøse ablationsteknikker mulighed for at behandle langt de fleste patienter med åreknuder på kontoret uden generel anæstesi eller kirurgiske snit, samtidig med at resultaterne maksimeres og recidiv minimeres.
INDLEDNING
Saphenous vein reflux er den underliggende primære abnormitet i de fleste tilfælde af overfladisk venøs insufficiens. Derfor har tilgange til behandling af saphenofemoral junction og saphenous truncal inkompetence domineret phlebologernes tankegang. Trendelenburg beskrev i 1890’erne, at saphenofemoral junction kun blev ligeret uden stripping af den inkompetente vena saphena saphena. Fordelene ved ligation alene frem for ligation og stripping, som stadig fremhæves den dag i dag,1 omfatter bevarelse af den saphene stamme med henblik på eventuel fremtidig brug som bypass-transplantat2 og undgåelse af skade på saphenusnerven.3 Høj ligation alene er mindre invasiv, hurtigere og enklere at udføre og er forbundet med en lettere helbredelse sammenlignet med stripping af venen. Selv om det er rigtigt, at det rutinemæssigt “skåner” saphenusstammen,4 er brugen af en syg saphenusåre som conduit blevet forbundet med en øget risiko for transplantationssvigt.5 Vigtigst af alt er det, at der ikke længere er tvivl om, at høj ligation alene normalt resulterer i vedvarende refluks i saphenusstammen.6,7 Varicose-recidiv er betydeligt reduceret7-9 , og reoperationsraten er 60 % til 70 % lavere, hvis saphenusåren strippes sammenlignet med ligation alene.10,11 Efter ligation alene blev der også fundet tilbagefald eller tilbageværende kommunikation med sammenløbet i lysken hos 80 % af patienterne, mens 34 % også havde perforatorinkompetence midt på låret via den ikke-afstribede vena saphena magna (GSV).12 Som Neglen konkluderede, er stripning af GSV i låret afgørende for at minimere tilbagefald, der skyldes genudvikling af inkompetent kommunikation med det saphenofemorale sammenløb og på grund af lårperforatorinkompetence.13 Kort sagt opvejer manglerne ved ligation alene fordelene.
Det er vigtigt at bemærke, at recidiv er almindeligt, selv efter ligation og stripping af saphenus vina saphena. Mens utilstrækkelig kirurgi af saphenofemoral junction og sygdomsprogression er mekanismer, der forklarer nogle tilfælde af recidiv, er en anden vigtig mekanisme neovaskularisering omkring junctionen efter venekirurgi.11,14 Faktisk er neovaskularisering blevet rapporteret som den vigtigste årsag til recidiv,9 med neovaskulære kanaler af varierende størrelse, antal og tortuositet, der i størstedelen af tilfældene står for refluks til recidiverende varicer.15 Selv om nogle har udtrykt tvivl om sandheden af ægte neovaskularisering, er der klare histologiske beviser for, at neovaskularisering er en årsag til tilbagevendende åreknuder.16 Tidlige rapporter tyder derimod på, at endovenøse ablationsteknikker er forbundet med en meget lav forekomst af neovaskularisering. 17 Det kan være, at udviklingen af neovaskularisering i høj grad forhindres ved at undgå lyskendissektion og ved at bevare venedrænage i normale junctional tributaries.18,19
EVLA er ligesom radiofrekvensablation og skumskleroterapi et mindre invasivt alternativ til venestripning. EVLA er indiceret hos en ambulant patient med stor, lille eller accessorisk venus saphena reflux med overfladiske varicer og/eller symptomer eller komplikationer relateret til overfladisk venøs insufficiens. EVLA udføres rutinemæssigt ved hjælp af fortyndet lokalbedøvelse med eller uden supplerende orale anxiolytika på et kontor. Det tager normalt 30-60 minutter at udføre proceduren, men den afhænger af længden af det behandlede segment, operatørens erfaring, og om der udføres supplerende procedurer som f.eks. ambulant flebectomi. Uanset hvordan den underliggende saphenøse inkompetence behandles, er det typisk nødvendigt med supplerende behandlinger for at behandle resterende varicer (figur 1).
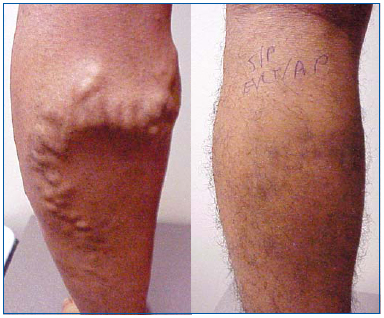
Figur 1. Mand på 26 år før og 1 måned efter endovenøs laserablation af den store saphenøse vene og ambulant flebectomi af varicerøse biflodder.
EFFICACY
Kort- og midtvejsstudier af EVLA, uanset hvilken bølgelængde der anvendes, synes bemærkelsesværdigt konsistente og rapporterer typisk om ablation af refluerende saphenusvener i 90 % eller mere af tilfældene.18,20-23 EVLA af vena saphena saphena har vist sig at korrigere eller væsentligt forbedre den hæmodynamiske abnormitet og de kliniske symptomer på kronisk venøs insufficiens (CVI) hos patienter i klinisk, etiologisk, anatomisk og patofysiologisk (CEAP) klinisk klasse 3-6 (CEAP) med overfladisk venøs refluks.24,25 Resultaterne synes at være lige så gode eller bedre end ved stripping, med bedre livskvalitetsscore i den postoperative periode sammenlignet med stripping.20,25-27 Der er rapporteret om høj patienttilfredshed.18,28,29 De samlede omkostninger (omkostninger til proceduren plus samfundsomkostninger) ved endovenøse procedurer er sandsynligvis lig med eller lavere end ved kirurgi.27
Første data om behandling af GSV med 810 nm- og 940 nm-enheder tyder på, at behandlingssvigt er ualmindeligt hos patienter, der behandles med > 70 J/cm.30,31 En tilbagetrækningshastighed på 2 mm/sek. ved 14 watt giver 70 J/cm.
VIRKNINGSMÆKANISME
Følgende bølgelængder anvendes i øjeblikket til EVLA: 810, 940, 980, 1064, 1319, 1320 og 2068 nm. Det er blevet postuleret, at skade på venevæggen formidles både ved direkte virkning og indirekte via laserinduceret damp, der genereres ved opvarmning af små mængder blod i venen.32 Nogle har antydet, at valget af bølgelængde har stor indflydelse på resultaterne.23
Den vigtigste kromofore i 1320 og 2078 nm lasere er, i det mindste i begyndelsen, vand, mens andre bølgelængder, der anvendes til EVLA, primært er rettet mod hæmoglobin. Det er naturligvis bydende nødvendigt at beskadige venevæggen tilstrækkeligt termisk for at opnå effektiv ablation. En vis opvarmning kan ske ved direkte absorption af fotonenergi (stråling) af venevæggen samt ved konvektion fra dampbobler og konduktion fra opvarmet blod. Det er dog usandsynligt, at disse sidstnævnte mekanismer tegner sig for størstedelen af påvirkningen af venen. Blodets maksimale temperatur er 100 °C. Laserbehandling har vist sig at producere karbonisering af venevæggen.33 Karbonisering af laserspidsen, som opstår ved ca. 300°C, er konstateret efter EVLA og synes at forekomme uanset den anvendte bølgelængde.34 Karbonisering af laserfiberspidsen skaber en punktvarmekilde og reducerer i det væsentlige lysets indtrængning i vævet til nul.34,35 Mordon et al. udtalte: “Den damp, der produceres ved absorption af laserenergi fra blodet, er en lille brøkdel af den energi, der er nødvendig for at beskadige venevæggen, og kan ikke være den primære mekanisme for skade på venen med endovenøs laser. Den karbonisering og tractus i venevæggene, der ses ved histologi efter endovenøs laser, kan kun være resultatet af direkte kontakt mellem laserfiberspidsen og venevæggen. “36 Dr. Rox Anderson, direktør for The Wellman Center for Photomedicine på Massachusetts General Hospital, rapporterede, at kulstof synes at være en sekundær, men vigtig kromofor, der sandsynligvis er uafhængig af bølgelængden (figur 2).34 Bemærk, at fiberspids og form kan have indflydelse på udviklingen af karbonisering.37

Figur 2. Karbonisering af 600-micron laserfiberspids sekundært til endovenøs laserablation med en 1320 nm laser (Foto venligst udlånt af Mark Forrestal, MD, FACPh).
TUMESCENT ANÆSTHESI
EVLA bør udføres under lokalbedøvelse ved hjælp af store mængder af en fortyndet opløsning af lidocain og epinephrin (gennemsnitligt volumen på 200-400 mL 0,1 % lidocain med 1:1.000.000 epinephrin), der er bufferet med natriumbicarbonat. Denne opløsning skal gives enten manuelt eller med en infusionspumpe under ultralydsvejledning, således at venen er omgivet af den anæstetiske væske i hele længden af det segment, der skal behandles (Figur 3).
Fordelene ved tumescent anæstesi til endovenøs ablation omfatter:
– anæstesi,
– adskillelse af den vene, der skal behandles, fra de omkringliggende strukturer,
– termisk sænkning, som reducerer spidstemperaturerne i perivenøst væv,
– venekompression, som maksimerer effekten af behandlingen på venevæggen.
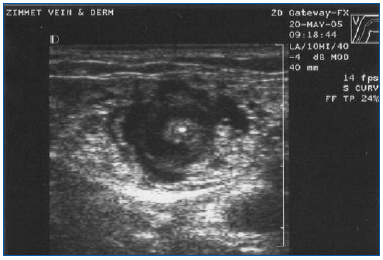
Figur 3. Tværgående ultralydsbillede af tumescent anæstetisk væske, der omgiver en centralt placeret stor saphenusåre og laserfiber/sheath.
Og selv om den maksimale sikre dosis lidocain ved anvendelse af tumescentteknikken til venøse procedurer ikke er velundersøgt, er en dosis på 35 mg/kg et rimeligt skøn.
Med disse parametre har tumescentanæstesi i forbindelse med fedtsugning vist sig at være overordentligt sikker. Yderligere oplysninger findes på http://www.liposuction.com/pharmacology/drug_inter act.php.
KONTRAINDIKATIONER TIL EVLA
Kontraindikationer til EVLA-teknikken er summeret i tabel I.

Tabel I. Kontraindikationer for endovenøs laser.
ADVERSE SEQUELAE
Kortvarige smerter og ekchymoser er almindeligt observeret efter EVLA. Intermitteret pulseret laserfiber pullback er i en retrospektiv gennemgang blevet rapporteret til at forårsage betydeligt større niveauer af postoperative smerter og blå mærker sammenlignet med en kontinuerlig pullback-protokol.38 Tilføjelse af en kort strækbandage i 3 dage efter EVLA i intermitterende tilstand reducerede i væsentlig grad patientrapporterede blå mærker og smerter. Anvendelse af kontinuerlig pullback-mode reducerede yderligere smerter og blå mærker i en sådan grad, at niveauerne svarede til dem, der blev rapporteret af patienter, der blev behandlet med radiofrekvensablation (tabel II og III). Foreløbige rapporter tyder på, at der kan være visse forskelle i det postoperative forløb afhængigt af den bølgelængde, der anvendes til at udføre EVLA.22,39 Dette er imidlertid baseret på sparsomme data med kortvarig opfølgning.
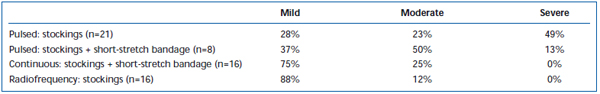
Tabel II. Patientvurderede postoperative blå mærker 3-7 dage efter pulseret endovenøs laserablation (EVLA) med klasse II-strømper, pulseret EVLA med strømper plus kortstrækningsbandage, EVLA i kontinuerlig tilstand med strømper og kortstrækningsbandage og radiofrekvensablation med strømper.
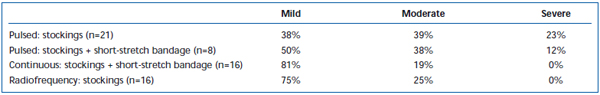
Tabel III. Patientvurderede postoperative smerter 3-7 dage efter pulseret endovenøs laserablation (EVLA) med klasse II-strømper, pulseret EVLA med strømper plus kortstrækningsbandage, kontinuerlig EVLA med strømper og kortstrækningsbandage og radiofrekvensablation med strømper.
PERIVENOUS THERMAL INJURY
De gennemsnitlige intravaskulære spidstemperaturer under EVLA (ged jugular vene, 12 watt, 1-sekunders pulser, 1-sekunders intervaller), målt lige ved laserspidsen, var i gennemsnit 729°C, mens de 4 mm distalt fra spidsen var i gennemsnit 93°C.40 Risikoen for kollaterale termiske skader afhænger imidlertid af den perivenøse vævsopvarmning og ikke af den intravaskulære temperatur.
Kollagen er blevet bemærket at trække sig sammen ved ca. 50 °C, mens nekrose opstår mellem 70 °C og 100 °C.41 Omfanget af termiske skader på væv afhænger i høj grad af mængden og varigheden af den varme, vævet udsættes for. Henriques og Moritz undersøgte tid-temperaturreaktionen for væv, der udsættes for op til 70°C.42 De fandt, at huden kunne modstå temperaturstigninger i meget korte eksponeringstider, og at reaktionen synes at være logaritmisk, efterhånden som eksponeringstiderne bliver kortere. F.eks. vil en stigning i kropstemperaturen til 58 °C medføre celledestruktion, hvis eksponeringstiden er længere end 10 sekunder. Vævene kan imidlertid tåle temperaturer på op til 70 °C, hvis eksponeringen varer mindre end 1 sekund. Li et al. rapporterede, at opvarmning af endothelceller til 48 °C i 10 minutter ikke forårsagede celledød.43 De fandt også, at osteoblaster efter eksponering i 10 minutter eller mindre ved 45 °C undergik forbigående og reversible ændringer. En anden undersøgelse fandt reversible vævsskader på baglåret hos mus efter nedsænkning i et vandbad ved 44°C.44
En nyere undersøgelse målte spidstemperaturen ved den ydre venevæg under EVLA i en levende griseøreåreåre og i eksponerede bagledsårer.45 EVLA-indstillingerne varierede fra 8 watt (1-2 sekunders pulsvarighed), 10 watt (1-1,5 sekunders pulsvarighed), 12 watt (0,5-1,5 sekunders pulsvarighed) til 15 watt (0,5-1,0 sekunders pulsvarighed), med og uden tumescent anæstesi. Resultaterne viser, at spidstemperaturerne varierede fra 34,6 °C til 49,1 °C som en funktion af de leverede joule, med lavere spidstemperaturer opnået, når der var tumescentvæske til stede (figur 4).
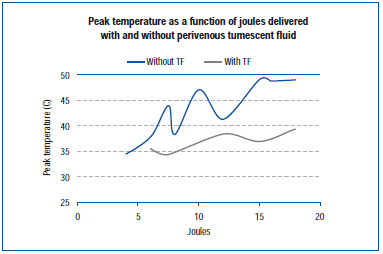
Figur 4. Tilpasset fra Zimmet SE, Min RJ. Temperaturændringer i perivenøst væv under endovenøs laserbehandling i en svinemodel. J Vasc Interv Radiol. 2003;14:911-915 (ref 45).
Peak-temperaturen målt under EVLA (63 patienter, 980 nm, 15 watt, 1,5 sek. pulser) ved den ydre venevæg hos mennesker, 3 cm under den saphenofemorale overgang, var henholdsvis 40,9 °C og 49,8 °C med og uden tumescent væske.46 Lignende resultater blev rapporteret fra en anden undersøgelse på mennesker under EVLA (12 patienter, 810 nm, 12 W, 1 sekunds pulser, 1 sekunds intervaller, tumescentteknik) med spidstemperaturer på henholdsvis 43,3 °C, 42,0 °C og 36,0 °C 3 mm, 5 mm og 10 mm fra GSV. 47
Der synes at være et meget hurtigt fald i temperaturen over korte afstande under EVLA. Dette er sandsynligvis i modsætning til radiofrekvent energi, hvor mikrobølgeopvarmning sker omkring vævs-elektrodegrænsefladen. Dataene fra dyr og mennesker tyder på, at de perivenøse spidstemperaturer, der genereres under endovenøs laser, sandsynligvis ikke vil forårsage permanent skade på perivenøst væv i de fleste situationer. Den højeste temperatur, der genereres, reduceres ved brug af perivenøs tumescentvæske. Disse resultater synes at forklare den meget lave rapporterede forekomst af nerveskader og hudforbrændinger efter EVLA. I en undersøgelse, hvor der blev anvendt en 1064 nm Nd: YAG-laser, blev der rapporteret en meget høj forekomst af paræstesi hos 36,5 % og hudforbrændinger hos 4,8 %.48 Det skal bemærkes, at den leverede energimængde var ca. tre gange højere end den, der typisk anvendes, og at behandlingen blev udført uden tumescentanæstesi. På trods af de lave perivenøse temperaturer, der er rapporteret med EVLA, er det vigtigt at bemærke, at der skal udvises særlig forsigtighed, når man overvejer endovenøs intervention i visse tilfælde, f.eks. ved iskiasnervevaricer.49,50
MAJOR KOMPLIKATIONER
Større komplikationer efter EVLA er sjældent blevet rapporteret. Raterne af dyb venetrombose (DVT), samlet fra flere serier, er meget lavere end 1 %.17,18,20,28 En gruppe rapporterede en forekomst af trombusudvidelse i femoralvenen på 7,7 %.51 I denne undersøgelse blev EVLA imidlertid udført under generel eller spinal anæstesi. Det forhold, at patienterne ikke var i stand til at bevæge sig umiddelbart postoperativt, kan have bidraget til den høje forekomst af trombusudvidelse. Der er en enkelt rapport om en arteriovenøs fistel, der udviklede sig efter EVLA af den korte sapheneus vene (SSV).52 En patient udviklede septisk tromboflebitis efter EVLA kombineret med åben ligatur af perforatorer og stabflebectomi.53 Dette gik over med antibiotikabehandling og debridering.
ALTERNATIVE TILGANGER
EVLA og radiofrekvensablation (RFA)54,55 synes begge at være effektive behandlinger for saphenus inkompetence. Fordelene ved EVLA i forhold til RFA omfatter kortere proceduretider og lavere omkostninger pr. behandling. De rapporterede okklusionsrater for EVLA er generelt lidt højere end dem, der opnås med RFA.56 Ulemperne ved EVLA kan omfatte flere blå mærker og mere ubehag i den tidlige postoperative periode, selv om dette kan være afhængig af teknikken. Begge teknikker vil fortsat blive forfinet, hvilket vil forbedre resultaterne. Begge procedurer er, når de udføres under tumescent anæstesi, forbundet med lave komplikationsrater.
En anden ny behandling af saphenøs refluks er brugen af skummede sclerosanter, der leveres under ultralydsstyring. En gas, f.eks. luft eller CO2, kan blandes med flydende detergentsklerosanter for at skabe skum, der skønnes at være ca. fire gange mere potent end den flydende form af det samme middel. De første resultater tyder på, at dette kan være en værdifuld metode, da den er hurtig og billig at udføre med en rapporteret succesrate på kort og mellemlang sigt på ca. 75 % til 90 %. Der er mange variabler i forbindelse med skum (f.eks. type og mængde af gas, teknik til fremstilling af skum, koncentration og type af anvendt sklerosant, injiceret mængde osv.) Der kan være en højere risiko for dyb venetrombose efter skumskleroterapi sammenlignet med standardskleroterapi. Korrekt teknik er vigtig for at minimere risikoen for denne komplikation. Andre bivirkninger, der er rapporteret efter skumskleroterapi, omfatter visuelle og neurologiske hændelser. Der er en offentliggjort rapport om slagtilfælde efter skumskleroterapi (20 mL polidocanolskum) hos en patient med et 1,8 cm patent foramen ovale.57 Yderligere erfaring og forskning med denne modalitet vil bedre afgrænse dens risici samt langtidseffekt.
KONKLUSION
De nuværende accepterede principper for behandling af åreknuder tjener til at maksimere resultaterne ud fra et hæmodynamisk og patientmæssigt synspunkt og samtidig minimere risikoen for recidiv. En hensigtsmæssig behandling af åreknuder begynder med en nøjagtig vurdering af den underliggende venøse patologi og identifikation af kilderne til venøs hypertension. Målet med behandlingen er bl.a. at fjerne de inkompetente forbindelser mellem det dybe og det overfladiske system samt at udslette veje med venøs inkompetence og inkompetente åreknuder. Det er tydeligt, at recidiv reduceres, hvis det inkompetente segment af den saphenøse stamme ableres.
Endovenøs laserablation er et mindre invasivt alternativ til vene stripping. Resultaterne synes at være lige så gode eller bedre end ved stripning, med bedre livskvalitetsscore i den postoperative periode. EVLA har vist sig at korrigere eller væsentligt forbedre den hæmodynamiske abnormitet hos patienter med kronisk venøs insufficiens med overfladisk venøs refluks. Tidlige rapporter tyder på, at endovenøse ablationsteknikker, i modsætning til kirurgisk stripping, er forbundet med en lav forekomst af neovaskularisering.
Anvendelsen af principperne for tumescentanæstesi på venøse behandlinger giver sammen med udviklingen af endovenøse ablationsteknikker mulighed for at behandle langt størstedelen af patienter med overfladisk venøs insufficiens på kontoret uden generel anæstesi eller kirurgiske snit, samtidig med at resultaterne maksimeres og recidiv minimeres.
Denne artikel blev indsendt i juli 29, 2006.

2. Large J. Surgical treatment of saphenous varices, with preservation of the main great saphenous trunk. J Vasc Surg. 1985;2:886-891.
3. Holme JB, Holme K, Sorensen LS. Det anatomiske forhold mellem den lange saphenøse vene og den saphenøse nerve. Relevans for radikal åreknuderkirurgi. Acta Chir Scand. 1988;154;154:631-633.
4. Rutherford RB, Sawyer JD, Jones DN. Skæbnen for resterne af saphenous vein efter delvis fjernelse eller ligation. J Vasc Surg. 1990;12:422-426.
5. Panetta TF, Marin ML, Marin ML, Veith FJ, et al. Uforstået forud eksisterende saphenous vein disease: an unrecognized cause of vein bypass failure. J Vasc Surg. 1992;15:102- 110.
6. McMullin GM, Coleridge-Smith PD, Scurr JH. Objektiv vurdering af ligation uden stripping af den lange saphenous vene. Br J Surg. 1991;78:1139-1142.
7. Sarin S, Scurr JH, Coleridge Smith PD. Vurdering af stripping af den lange saphena vene ved behandling af primære åreknuder. Br J Surg. 1992;79:889-893.
8. Munn SR, Morton JB, Macbeth WA, McLeish AR. At fjerne eller ikke fjerne den lange saphenusåre? Et forsøg med åreknuder. Br J Surg. 1981;68:426-481.
9. Jones L, Braithwaite BD, Selwyn D, Cooke S, Earnshaw JJ. Neovaskularisering er den vigtigste årsag til tilbagefald af åreknuder: resultater af et randomiseret forsøg med stripping af den lange sapheneusåre. Eur J Vasc Endovasc Surg. 1996;12:442-445.
10. Dwerryhouse S, Davies B, Harradine K, Earnshaw JJ. Stripping af den lange saphenous vein reducerer antallet af reoperationer for tilbagevendende åreknuder: femårsresultater af et randomiseret forsøg. J Vasc Surg. 1999;29:589-592.
11. Winterborn RJ, Foy C, Earnshaw JJ. Årsager til tilbagefald af åreknuder: sene resultater af et randomiseret kontrolleret forsøg med stripping af den lange saphenus-åre. J Vasc Surg. 2004;40:634-639.
12. Corbett CR, Runcie JJ, Lea TM, Jamieson CW. Årsager til stripning af den lange saphena vene. Phlebologie. 1988;41:766-769.
13. Neglen P. Behandling af åreknuder af saphenøs oprindelse: sammenligning af ligation, selektiv excision og scleroterapi. In: Bergan JJ, Goldman MP eds. Varicose Veins and Telangiectasias: Diagnosis and Treatment. St. Louis, Mo, USA: Quality Medical Publishing; 1993:148-165.
14. Kostas T, Ioannou CV, Touloupakis E, et al. Recurrent varicose veins after surgery: a new appraisal of a common and complex problem in vascular surgery. Eur J Vasc Endovasc Surg. 2004;27:275-282.
15. Van Rij AM, Jones GT, Hill GB, Jiang P. Neovascularization and recurrent varicose veins: more histologic and ultrasound evidence. J Vasc Surg. 2004;40:296-302.
16. Nyamekye I, Shephard NA, Davies B, et al. Clinicopathological evidence that neovascularization is a cause of recurrent varicose veins. Eur J Vasc Endovasc Surg. 1998;15;15: 412-415.
17. Ravi R, Rodriguez-Lopez JA, Trayler EA, et al. Endovenøs ablation af inkompetente sapheneusårer: en stor enkeltcenter-erfaring. J Endovasc Ther. 2006;13:244- 248.
18. Min RJ, Khilnani N, Zimmet SE. Endovenøs laserbehandling af saphenous vein reflux: langtidsresultater. J Vasc Interv Radiol. 2003;14:991-996.
19. Bergan JJ, Rattner Z. Endovenous therapy-2005. Acta Chir Bel. 2005;105:12- 15.
20. Agus GB, Mancini S, Magi G. The first 1000 cases of Italian endovenous-laser Working Group (IEWG). Rationale, og langtidsresultater for perioden 1999-2003. Int Angiol. 2006;25:209-215.
21. Kalra M, Gloviczki P. For femten år siden skulle laser åbne arterier, nu skal den lukke vener: Hvad er virkeligheden bag værktøjet? Perspect Vasc Surg Endovasc Ther. 2006;18;18:3-8 (diskussion 9- 10).
22. Kabnick LS. Resultater af forskellige endovenøse laserbølgelængder til ablation af store saphenusvener. J Vasc Surg. 2006;43: 88-93.
23. Goldman MP, Maritess M, Rao J. Intravaskulær 1320-nm laserlaserlukning af den store vene saphena magna: en 6-12 måneders opfølgningsundersøgelse. Dermatol Surg. 2004;30;30: 1380-1385.
24. Marston WA, Owens LV, Davies S, et al. Endovenøs saphenøs ablation korrigerer den hæmodynamiske abnormitet hos patienter med CEAP-klinisk klasse 3-6 CVI på grund af overfladisk refluks. Vasc Endovascular Surg. 2006;40;40:125-130.
25. De Medeiros CA, Luccas GC. Sammenligning af endovenøs behandling med en 810 nm laser i forhold til konventionel stripping af den store sapheneusåre hos patienter med primære åreknuder. Dermatol Surg. 2005;31:1685-1694.
26. Mekako AI, Hatfield J, Bryce J, et al. A nonrandomised controlled trial of endovenous laser therapy and surgery in the treatment of varicose veins. Ann Vasc Surg. 2006;Jun 27:.
27. Vuylsteke M, Van den Bussche D, Audenaert EA, Lissens P. Endovenous laser obliteration for the treatment of primary varicose veins. Phlebology. 2006;21:80-87. 28. Perkowski P, Ravi R, Gowda RC, et al. Endovenøs laserablation af vena saphena magna til behandling af venøs insufficiens og åreknuder: tidlige resultater fra en stor singlecenter-erfaring. J Endovasc Ther. 2004;11:132-138.
29. Sharif MA, Soong CV, Lau LL, et al. Endovenøs laserbehandling af inkompetence af lange sapheneusvener. Br J Surg. 2006;93:831-835.
30. Proebstle TM, Krummenauer F, Gul D, Knop J. Nonocclusion and early reopening of the great saphenous vein after endovenous laser treatment is fluence dependent. Dermatol Surg. 2004;30:174-178.
31. Timperman PE, Sichlau M, Ryu RK. Større energitilførsel forbedrer behandlingssuccesen af endovenøs laserbehandling af inkompetente saphenous vener. J Vasc Interv Radiol. 2004;15:1061-1063.
32. Proebstle TM, Sandhofer M, Kargl A, et al. Termisk beskadigelse af den indre venevæg under endovenøs laserbehandling: Energiens absorption af intravaskulært blod spiller en afgørende rolle. Dermatol Surg. 2002;28;28:596-600.
33. Schmedt CG, Sroka R, Steckmeier S, et al. Undersøgelse af radiofrekvens- og lasereffekter (980 nm) efter endoluminal behandling af insufficiens i sapheneusvenen i en ex-vivo-model. Eur J Vasc Endovasc Surg. 2006;Jun 14;.
34. Anderson RR. Endovenøs laser: virkningsmekanisme. Paper præsenteret på det årlige møde i American Academy of Dermatology; March 3-7, 2006; San Francisco, California, USA.
35. Izzo F. Other thermal ablation techniques: microwave and interstitial laser ablation of liver tumors. Annals of Surgical Oncology. 2003;10:491-497.
36. Mordon SR, Wassmer B og Zemmouri J. Matematisk modellering af endovenøs laserbehandling (ELT). BioMedical Engineering OnLine. 2006;5:26. Tilgængelig på: http://www.biomedical-engineeringonline. com/content/5/1/26. Tilgået den 19. juli 2006.
37. De-Fei Hong, Shu-You Peng, Song-Ying Li, Li-Min Tong. Eksperimentel undersøgelse af diodelaserinduceret termokoagulation af levervæv med scannerfiberspids. World J Gastroenterol. 2003;9:2350-2352.
38. Zimmet SE. Smerter, blå mærker og korttidseffekt efter endovenøs laserbehandling af den store saphenous vene: effekten af operationsteknik og postoperativ pleje. Paper præsenteret ved den 16th Annual Congress of the American College of Phlebology; Nov 7-10, 2002; Fort Lauderdale, Florida, USA.
39. Proebstle TM, Moehler T, Gul D, Herdemann S. Endovenous treatment of the great saphenous vein using a 1320 nm Nd:YAG laser causes fewer side effects than using a 940 nm diode laser. Dermatol Surg. 2005;31:1678-1683.
40. Weiss RA. Sammenligning af endovenøs radiofrekvens versus 810 nm diode laser okklusion af store vener i en dyremodel. Dermatol Surg. 2002;28:56-61.
41. Biesman BS, Khan J. Laser incisionskirurgi. Clinics in Plastic Surg. 2000;27:213- 220.
42. Moritz AR, Henriques Jr EC. Undersøgelser af termisk skade II: den relative betydning af tid og overfladetemperatur i forbindelse med forårsagelse af kutane bumser. Am J Pathol. 1947;23:695-720.
43. Li S, Chien S, Branemark P. Heat shockinduced necrosis and apoptosis in osteoblasts. J Orthop Res. 1999;17:891-899.
44. Jansen W, Haveman J. Histopatologiske ændringer i huden og det subkutane væv i museben efter behandling med hypertermi. Path Res Pract. 1990;186: 247-253.
45. Zimmet SE, Min RJ. Temperaturændringer i perivenøst væv under endovenøs laserbehandling i en svinemodel. J Vasc Interv Radiol. 2003;14:911-915.
46. Lahl W. Termometriske undersøgelser af perivenøs temperatur under endovenøs laserbehandling af åreknuder. Paper præsenteret på den 15th World Congress of the Union Internationale de Phlébologie; October 2-7, 2005; Rio de Janeiro, Brazil.
47. Beale RJ, Mavor AID, Gough MJ. Varmeafgivelse under endovenøs laserbehandling af åreknuder – er der risiko for nerveskader? Phlebology. 2006;21:32-35.
48. Chang CJ, Chua JJ. Endovenøs laserfotocoagulation (EVLP) til behandling af åreknuder. Lasers Surg Med. 2002;31:257-262.
49. Ricci S, Georgiev M, Jawien A, Zamboni P. Iskiasnerven varicer. Eur J Vasc Endovasc Surg. 2005;29:83-87.
50 Ricci S. Ultralydsobservation af iskiasnerven og dens grene ved poplitea fossa: altid synlig, aldrig set. Eur J Vasc Endovasc Surg. 2005;30:659-663. 51 Mozes G, Kalra M, Carmo M, Swenson L, Gloviczki P. Extension of saphenous thrombus into the femoral vein: a potential complication of new endovenous ablation techniques. J Vasc Surg. 2005;41:130-135.
52 Timperman, PE. Arteriovenøs fistel efter endovenøs laserbehandling af den korte saphenous vene. J Vasc Interv Radiol. 2004;15;15:625-627.
53 Dunst KM, Huemer GM, Wayand W, Shamiyeh A. Diffus flegmonøs flebitis efter endovenøs laserbehandling af den store saphena vene. J Vasc Surg. 2006;43;43:1056-1058.
54 Lurie F, Creton D, Eklof B, et al. Prospektiv randomiseret undersøgelse af endovenøs radiofrekvent obliteration (lukningsprocedure) versus ligation og stripping i en udvalgt patientpopulation (EVOLVeS Study). J Vasc Surg. 2003;38:207-214.
55 Merchant RF, DePalma RG, Kabnick LS. Endovaskulær obliteration af saphenous reflux: en multicenterundersøgelse. J Vasc Surg. 2002;35:1190-1196.
56 Puggioni A, Kalra M, Carmo M, Mozes G, Gloviczki P. Endovenøs laserterapi og radiofrekvensablation af den store vene saphena magna: analyse af tidlig effekt og komplikationer. J Vasc Surg. 2005;42;42; 488-493.
57 Forlee MV, Grouden M, Moore DJ, Shanik G. Stroke after varicose vein foam injection sclerotherapy. J Vasc Surg. 2006;43;43: 162-164.