US Pharm. 2017;42(6)(Generic Drugs suppl):38-42.
ABSTRACT: Protonenpumpeninhibitoren (PPIs) sind eine Klasse von Antisekretionsmitteln, die zur Behandlung verschiedener Magen-Darm-Erkrankungen eingesetzt werden, wie z. B. der gastroösophagealen Refluxkrankheit, Helicobacter pylori-Erkrankungen und Magen- und Zwölffingerdarmgeschwüren. Obwohl es sich bei diesen Wirkstoffen um wirksame Säurehemmer handelt, wird der Einsatz von PPIs aufgrund von Berichten über neue potenzielle unerwünschte Wirkungen häufig kontrovers diskutiert. Übermäßiger Gebrauch und Wechselwirkungen mit anderen Medikamenten sind Probleme, die mit PPIs in Verbindung gebracht werden. Da mehrere PPIs auch rezeptfrei erhältlich sind, stellt die unsachgemäße Verwendung dieser Mittel ein großes Problem dar. Apotheker können in allen Bereichen einen großen Einfluss auf den unangemessenen Gebrauch von PPI haben, indem sie für eine angemessene Einleitung und Fortsetzung der Therapie, Dosierung und Behandlungsdauer sorgen.
Protonenpumpeninhibitoren (PPI) sind eine Medikamentenklasse, die häufig zur Behandlung verschiedener Magen-Darm-Erkrankungen eingesetzt wird, darunter die gastroösophageale Refluxkrankheit (GERD), Erkrankungen im Zusammenhang mit Helicobacter pylori sowie Magen- und Zwölffingerdarmgeschwüre. Obwohl diese sekretionshemmenden Wirkstoffe die bevorzugte Behandlung für zahlreiche Erkrankungen sind, wird die Klasse durch eine übermäßige Anwendung und Berichte über potenziell schwerwiegende unerwünschte Wirkungen und Wechselwirkungen zwischen Arzneimitteln geplagt.1 Darüber hinaus wird das Patientenmanagement bei Erkrankungen, die mit PPIs behandelt werden, durch die rezeptfreie Verfügbarkeit einiger dieser Wirkstoffe erschwert. Dieser Artikel soll den angemessenen Gebrauch hervorheben und eine evidenzbasierte Beschreibung mehrerer neuer oder heftig diskutierter Nachteile dieser Wirkstoffe liefern.
Verfügbarkeit von PPIs
Sechs einzelne PPIs, von denen fünf als Generika erhältlich sind, sind auf Rezept erhältlich (TABELLE 1).2-7 Niedrige Dosen von Omeprazol, Lansoprazol und eine Markenversion von Esomeprazol-Magnesium sind rezeptfrei erhältlich. Omeprazol wird auch in einer Co-Formulierung mit Natriumbicarbonat verwendet. Dieser Artikel konzentriert sich in erster Linie auf generisch erhältliche, oral verabreichte PPIs.
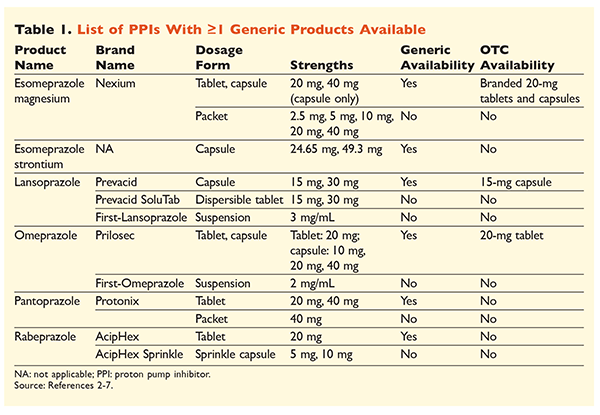
Esomeprazol Strontium wurde von der FDA aufgrund seiner Bioäquivalenz zu Esomeprazol Magnesium zugelassen.3 Obwohl die Produktkennzeichnung für diese beiden Wirkstoffe sehr ähnlich ist, gibt es drei bemerkenswerte Unterschiede. Erstens ist Esomeprazol-Strontium in Kapseln zu 24,65 mg und 49,3 mg erhältlich, die Esomeprazol-Magnesium 20 mg bzw. 40 mg entsprechen. Zweitens ist Esomeprazol-Strontium nicht von der FDA für die Verwendung bei pädiatrischen Patienten zugelassen, während Esomeprazol-Magnesium für die Verwendung bei Patienten ab 1 Monat zugelassen ist. Schließlich sollte die Anwendung von Esomeprazol-Strontium bei schwerer Niereninsuffizienz vermieden werden, da es in dieser Bevölkerungsgruppe nicht untersucht wurde. Für Esomeprazol-Magnesium wird keine Dosisanpassung empfohlen.3 Für die Zwecke dieses Artikels wird der Begriff Esomeprazol verwendet, um Esomeprazol-Magnesium zu beschreiben.
Verabreichung
Alle generisch erhältlichen PPIs, einschließlich Kapseln und Tabletten, sollten im Ganzen geschluckt werden, ohne sie zu teilen, zu zerkleinern oder zu kauen.2-7 Bei Patienten, die orale Darreichungsformen nicht schlucken können, können Omeprazol-, Lansoprazol- und Esomeprazol-Kapseln geöffnet und der Inhalt auf Apfelmus gestreut werden. Zusätzlich können Lansoprazol-Kapseln in 2 oz. Apfel-, Tomaten- oder Orangensaft gestreut werden. Alle Mischungen, die den Inhalt geöffneter Kapseln enthalten, sollten sofort geschluckt werden und dürfen nicht für den späteren Gebrauch aufbewahrt werden.2,4,5
Lansoprazol, Omeprazol und Esomeprazol sollten vor den Mahlzeiten verabreicht werden, aber die spezifischen Empfehlungen für die Einnahmezeiten variieren. Omeprazol sollte 30 bis 60 Minuten vor einer Mahlzeit und Esomeprazol mindestens 60 Minuten vorher verabreicht werden; für Lansoprazol ist kein Zeitrahmen angegeben.2,4,5 Pantoprazol kann mit oder ohne Nahrung verabreicht werden.6 Rabeprazol sollte bei Zwölffingerdarmgeschwüren nach einer Mahlzeit und bei der H. pylori-Eradikation mit einer Mahlzeit eingenommen werden; bei allen anderen Indikationen kann Rabeprazol mit oder ohne Nahrung eingenommen werden.7
Dosierung und Therapiedauer
Angesichts des Rufs der PPIs, sehr wirksam und im Allgemeinen sicher zu sein, ist die erhebliche Überversorgung mit PPIs ein großes Problem.1 PPIs werden nicht nur häufig für Indikationen verabreicht, für die es keine Belege gibt, die ihren Einsatz rechtfertigen, sondern diese Medikamente werden auch häufig in höheren Dosen als notwendig verschrieben und die Behandlungsdauer geht über die empfohlenen Zeiträume hinaus.8,9 Die zugelassenen Dosierungen und die empfohlene Therapiedauer für jeden PPI sind in den TABELLEN 2 und 3 angegeben. Behandlungsempfehlungen, die von den von der FDA genehmigten abweichen, sowie bemerkenswerte klinische Perlen im Zusammenhang mit der Einleitung, Dosierung und Dauer der PPI-Behandlung sind im Folgenden aufgeführt.
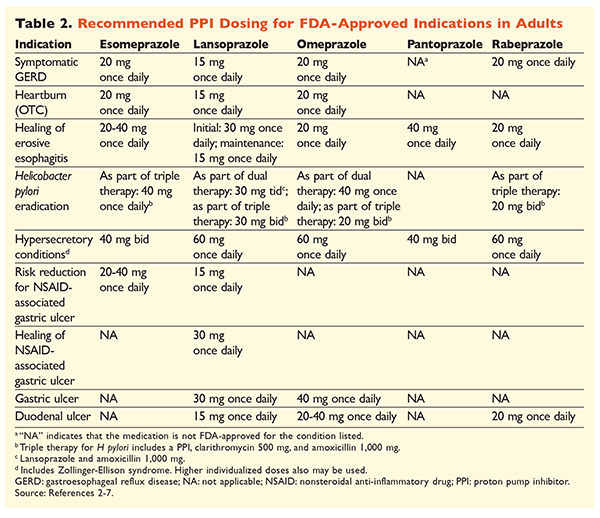
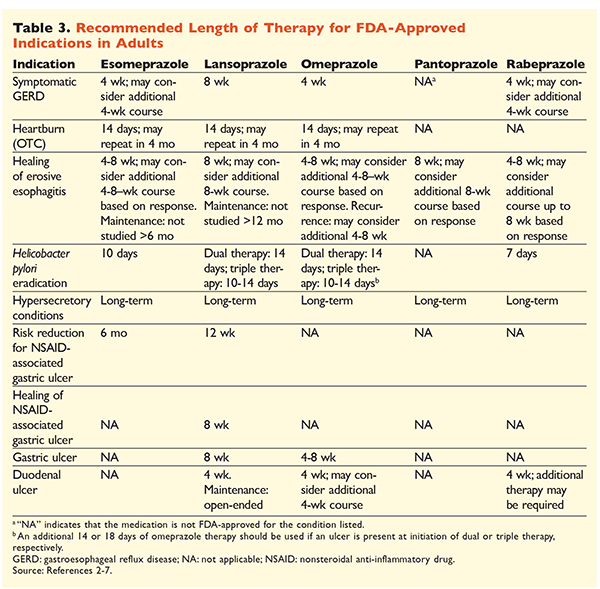
GERD: Bei Patienten mit GERD gelten alle PPI als gleichermaßen wirksam, und eine 8-wöchige Therapie mit jedem verfügbaren Wirkstoff wird empfohlen.10 Patienten, deren Symptome nach 2 bis 3 Monaten therapierefraktär sind, benötigen möglicherweise eine langfristige Erhaltungstherapie mit zweimal täglicher Gabe. Es sollte jedoch die niedrigste wirksame Dosis verwendet werden, und wenn der Patient nicht auf die Therapie anspricht, sollte ein anderer PPI in Betracht gezogen werden.10 Alternativ kann eine bedarfsgerechte PPI-Therapie oder ein schrittweiser Übergang zu einem Histamin2-Rezeptor-Antagonisten (H2RA) in Betracht gezogen werden.10 Die Behandlung mit einem rezeptfreien PPI sollte auf 14 Tage begrenzt sein, wobei eine erneute Behandlung nicht häufiger als alle 4 Monate erfolgen sollte.11
H pylori-assoziierte Geschwüre: Je nach verwendetem PPI umfassen die von der FDA zugelassenen Therapieschemata zur Eradikation von H. pylori eine Zweifachtherapie mit Amoxicillin oder Clarithromycin und eine Dreifachtherapie mit beiden Wirkstoffen für 7 bis 14 Tage.2-5,7 Spezifische leitliniengestützte Behandlungsschemata unterscheiden sich von den von der FDA zugelassenen, aber die empfohlene Therapiedauer ist ähnlich, wobei alle Schemata einen Dosierungszeitraum von 10 bis 14 Tagen haben.12 Nach der Eradikation von H. pylori ist eine PPI-Erhaltungstherapie nicht erforderlich.13 Eine detailliertere Diskussion spezifischer Schemata würde den Rahmen dieses Artikels sprengen.
Prophylaxe und Behandlung von NSAID-induzierten Geschwüren: Nach dem Auftreten eines NSAID-assoziierten Ulcus sollte die Notwendigkeit einer NSAID-Therapie neu bewertet werden. Wenn eine fortgesetzte NSAID-Therapie als angemessen erachtet wird, sollten die Patienten mit einer selektiven Cyclooxygenase-2-Therapie in der niedrigsten wirksamen Dosis für die kürzest mögliche Dauer in Kombination mit einem PPI behandelt werden.13
Zur Prophylaxe wird die Einführung eines PPI nur bei Patienten mit mäßigem oder hohem Risiko für NSAID-bedingte GI-Toxizität empfohlen. Zu den Risikofaktoren gehören ein Alter von >65 Jahren, eine hochdosierte NSAID-Therapie, ein unkompliziertes Ulkus in der Vorgeschichte und die gleichzeitige Einnahme von Aspirin (auch in niedriger Dosierung), Kortikosteroiden oder Antikoagulantien. Zu den Patienten mit einem mäßigen Risiko für NSAID-induzierte GI-Toxizität gehören Patienten mit einem oder zwei dieser Risikofaktoren, während Patienten mit einem hohen Risiko mehr als zwei Risikofaktoren oder eine Vorgeschichte eines komplizierten Magengeschwürs aufweisen, insbesondere wenn dieses erst kürzlich aufgetreten ist.14 Es ist sinnvoll, die PPI-Therapie fortzusetzen, solange der Patient mit mäßigem oder hohem Risiko weiterhin eine NSAID-Therapie erhält.13
Idiopathisches Geschwür: Bei Patienten, die nicht mit einer säuresuppressiven Therapie behandelt werden, treten Geschwüre ohne eindeutig identifizierbare Ursache wahrscheinlich wieder auf. In den Leitlinien wird nicht eindeutig empfohlen, wie lange Patienten mit einer Erhaltungstherapie behandelt werden sollten, aber sie legen nahe, dass eine fortlaufende PPI-Therapie das Risiko einer erneuten Ulkusbildung verringert.13
Sicherheit
PPIs gelten allgemein als eine gut verträgliche Medikamentenklasse.1 Mehrere Sicherheitsbedenken haben jedoch lange Zeit ihren Ruf getrübt, darunter ein erhöhtes Risiko für Clostridium-difficile-assoziierte Diarrhöe, ambulant erworbene Lungenentzündung und Knochenbrüche.15,16 In jüngerer Zeit wurden Bedenken hinsichtlich Demenz und chronischer Nierenerkrankungen geäußert, und die Debatten über Hypomagnesiämie und eine theoretische Wechselwirkung mit Clopidogrel wurden fortgesetzt.
Demenz: Zwei neuere Studien deuten auf ein potenziell erhöhtes Demenzrisiko bei langfristiger Einnahme von PPI bei älteren Menschen hin.17,18 Ein vorgeschlagener Mechanismus hinter diesem Befund ist, dass PPI die Entwicklung von Beta-Amyloid-Plaques fördern, eine vorgeschlagene Pathophysiologie der Alzheimer-Krankheit.15 Allerdings sprechen die Einschränkungen der Studien nicht für einen schlüssigen kausalen Zusammenhang zwischen der Einnahme von PPI und einem erhöhten Auftreten von Demenz.19
Renale Komplikationen: Obwohl PPIs weithin als häufige Ursache einer akuten interstitiellen Nephritis anerkannt sind, deuten neuere Daten darauf hin, dass diese Wirkstoffe auch für die Entwicklung anderer Nierenkomplikationen verantwortlich sind.15,20 Drei neuere Studien legen nahe, dass PPIs für ein erhöhtes Risiko für chronische Nierenerkrankungen und das Fortschreiten bis zum Endstadium der Nierenerkrankung verantwortlich sein könnten.20-22 Diese Beobachtungsstudien müssen jedoch mit Vorsicht interpretiert werden, da die Kausalität nicht bestätigt werden kann.23
Hypomagnesiämie: Im Jahr 2011 gab die FDA eine Warnung heraus, dass eine längere Einnahme von PPIs über einen Zeitraum von mehr als einem Jahr zu einer Hypomagnesiämie führen kann.24 Seitdem haben mehrere große Studien dieses Ergebnis gestützt.25-29 Der Zusammenhang zwischen PPIs und Hypomagnesiämie ist jedoch nicht eindeutig und wird durch externe Risikofaktoren erschwert.30-32 Derzeit wird eine klinisch signifikante PPI-induzierte Hypomagnesiämie als selten angesehen und tritt häufiger bei gleichzeitiger Einnahme von Diuretika auf.31,32 Eine Überwachung wird nur bei Patienten mit zusätzlichen Risikofaktoren empfohlen.32
Wechselwirkung mit Clopidogrel: Clopidogrel spielt eine wichtige Rolle bei der Senkung des kardiovaskulären Risikos, wird jedoch mit GI-Blutungen in Verbindung gebracht, insbesondere bei Patienten mit erhöhtem Risiko. Ein Schutz vor Magen-Darm-Blutungen mit PPIs wird häufig bei Patienten eingesetzt, bei denen ein erhöhtes Risiko für Magen-Darm-Blutungen besteht, z. B. bei Patienten mit einer früheren Blutung im oberen Teil des Magen-Darm-Trakts, fortgeschrittenem Alter, gleichzeitiger Einnahme von Antikoagulantien, Kortikosteroiden oder NSAIDs (einschließlich Aspirin) und/oder einer H. pylori-Infektion.33
PPIs hemmen vermutlich das Enzym CYP2C19, den primären Weg, über den Clopidogrel aktiviert wird.33 Diese Wechselwirkung kann theoretisch die thrombozytenaggregationshemmende Wirkung von Clopidogrel abschwächen und das Risiko nachteiliger kardiovaskulärer Folgen erhöhen.33 Aufgrund widersprüchlicher Ergebnisse sowohl aus pharmakokinetischen Studien als auch aus Ergebnisstudien ist die klinische Bedeutung dieser Wechselwirkung jedoch ungewiss.34
Außerdem fehlt es an konsistenten Erkenntnissen über die tatsächliche Auswirkung einzelner PPIs auf die Wirkung von Clopidogrel.33 Die jüngsten FDA-Empfehlungen legen nahe, dass Pantoprazol eine sicherere Wahl ist als andere PPIs, während Omeprazol als das riskanteste gilt.35 Die aktuellen Daten stützen diese Schlussfolgerung weiterhin, aber es sind weitere Studien erforderlich, um zu bestätigen, ob es einen Unterschied zwischen den PPIs gibt.36
Es ist wichtig, die Vorteile und Risiken einer Thrombozytenaggregationshemmer-Therapie allein oder in Kombination mit einem PPI abzuwägen, wenn eine Entscheidung über eine zusätzliche Therapie zum Schutz des Magen-Darm-Trakts getroffen wird. Bei Patienten mit hohem Risiko für gastrointestinale Komplikationen kann der Nutzen einer PPI-Therapie größer sein als die geringere Wirksamkeit einer Thrombozytenaggregationshemmer-Therapie, die inkonsistent nachgewiesen wurde. Für Patienten mit einem geringeren Risiko für gastrointestinale Komplikationen kann ein H2RA eine sinnvolle Behandlungsoption sein, obwohl sich diese Klasse für diese Indikation als weniger wirksam erwiesen hat als PPIs.33
Schlussfolgerung
Apotheker in allen Bereichen können einen tiefgreifenden Einfluss auf den unangemessenen Gebrauch von PPIs haben, indem sie für eine korrekte Einleitung und Fortführung der Therapie, Dosierung und Behandlungsdauer sorgen. Da immer wieder widersprüchliche Daten zu den Sicherheitsprofilen dieser Medikamente auftauchen, wird der langfristige Einsatz von PPIs immer komplizierter. Indem sie sicherstellen, dass die niedrigste geeignete Dosis für die kürzeste erforderliche Dauer verwendet wird, können Apotheker dazu beitragen, dass Patienten nicht unnötig potenziellen Schäden ausgesetzt werden.
1. Heidelbaugh JJ, Kim AH, Chang R, Walker PC. Übermäßiger Einsatz von Protonenpumpenhemmern: Was der Kliniker wissen muss. Therap Adv Gastroenterol. 2012;5:219-232.
2. Nexium (Esomeprazol-Magnesium) package insert. Wilmington, DE: AstraZeneca Pharmaceuticals LP; Dezember 2016.
3. Esomeprazol Strontium package insert. Glasgow, KY: Amneal Pharmaceuticals; Dezember 2014.
4. Prevacid (Lansoprazol) Packungsbeilage. Deerfield, IL: Takeda Pharmaceuticals America, Inc; Oktober 2016.
5. Prilosec (Omeprazol) package insert. Wilmington, DE: AstraZeneca Pharmaceuticals LP; Dezember 2016.
6. Protonix (Pantoprazol) Packungsbeilage. Philadelphia, PA: Wyeth Pharmaceuticals Inc. October 2016.
7. AcipHex (Rabeprazol) package insert. Woodcliff Lake, NJ: Eisai Inc; April 2016.
8. Chia CT, Lim WP, Vu CK. Inappropriate use of proton pump inhibitors in a local setting. Singapore Med J. 2014;55:363-366.
9. Kelly OB, Dillane C, Patchett SE, et al. The inappropriate prescription of oral proton pump inhibitors in the hospital setting: a prospective cross-sectional study. Dig Dis Sci. 2015;60:2280-2286.
10. Katz PO, Gerson LB, Vela MF. Leitlinien für die Diagnose und Behandlung der gastroösophagealen Refluxkrankheit. Am J Gastroenterol. 2013;108:308-328.
11. FDA Drug Safety Communication: possible increased risk of fractures of the hip, wrist, and spine with the use of proton pump inhibitors. www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPatientsandProviders/ucm213206.htm. Accessed February 17, 2017.
12. Chey WD, Leontiadis GI, Howden CW, Moss SF. ACG clinical guideline: treatment of Helicobacter pylori infection. Am J Gastroenterol. 2017;112:212-239.
13. Laine L, Jensen DM. Management von Patienten mit Ulkusblutungen. Am J Gastroenterol. 2012;107:345-360.
14. Lanza FL, Chan FK, Quigley EM. Leitlinien zur Prävention von NSAID-bedingten Ulkuskomplikationen. Am J Gastroenterol. 2009;104:728-738.
15. Eusebi LH, Rabitti S, Artesiani ML, et al. Protonenpumpenhemmer: Risiken bei Langzeitanwendung. J Gastroenterol Hepatol. 2017; Jan 16.
16. Abramowitz J, Thakkar P, Isa A, et al. Adverse event reporting for proton pump inhibitor therapy: an overview of systematic reviews. Otolaryngol Head Neck Surg. 2016;155:547-554.
17. Haenisch B, von Holt K, Wiese B, et al. Risiko einer Demenz bei älteren Patienten unter der Verwendung von Protonenpumpenhemmern. Eur Arch Psychiatry Clin Neurosci. 2015;265:419-428.
18. Gomm W, von Holt K, Thomé F, et al. Association of proton pump inhibitors with risk of dementia: a pharmacoepidemiological claims data analysis. JAMA Neurol. 2016;73:410-416.
19. Kuller LH. Erhöhen Protonenpumpeninhibitoren das Risiko einer Demenz? JAMA Neurol. 2016;73:379-381.
20. Arora P, Gupta A, Golzy M, et al. Protonenpumpenhemmer sind mit einem erhöhten Risiko für die Entwicklung einer chronischen Nierenerkrankung verbunden. BMC Nephrol. 2016;17:112.
21. Xie Y, Bowe B, Li T, et al. Protonenpumpeninhibitoren und das Risiko für das Auftreten von CKD und das Fortschreiten zu ESRD. J Am Soc Nephrol. 2016;27:3153-3163.
22. Lazarus B, Chen Y, Wilson FP, et al. Protonenpumpeninhibitor use and the risk of chronic kidney disease. JAMA Intern Med. 2016;176:238-246.
23. Kia L, Kahrilas PJ. Therapie: Risiken im Zusammenhang mit chronischem PPI-Gebrauch – Signal oder Rauschen? Nat Rev Gastroenterol Hepatol. 2016;13(5):253-254.
24. FDA Drug Safety Communication: Niedrige Magnesiumwerte können mit der Langzeiteinnahme von Protonenpumpenhemmern (PPIs) in Verbindung gebracht werden. www.fda.gov/Drugs/DrugSafety/ucm245011.htm. Accessed February 17, 2017.
25. Kieboom BC, Kiefte-de Jong JC, Eijgelsheim M, et al. Protonenpumpenhemmer und Hypomagnesiämie in der Allgemeinbevölkerung: eine bevölkerungsbasierte Kohortenstudie. Am J Kidney Dis. 2015;66:775-782.
26. Park CH, Kim EH, Roh YH, et al. The association between the use of proton pump inhibitors and the risk of hypomagnesemia: a systematic review and meta-analysis. PLoS One. 2014;9:e112558.
27. Luk CP, Parsons R, Lee YP, Hughes JD. Protonenpumpeninhibitor-assoziierte Hypomagnesiämie: Was sagen uns die FDA-Daten? Ann Pharmacother. 2013;47:773-780.
28. Cheungpasitporn W, Thongprayoon C, Kittanamongkolchai W, et al. Protonenpumpeninhibitoren im Zusammenhang mit Hypomagnesiämie: eine systematische Überprüfung und Meta-Analyse von Beobachtungsstudien. Ren Fail. 2015;37:1237-1241.
29. Markovits N, Loebstein R, Halkin H, et al. The association of proton pump inhibitors and hypomagnesemia in the community setting. J Clin Pharmacol. 2014;54:889-895.
30. Park SH, Lee SH, Lee JS, et al. Changes in serum magnesium concentration after use of a proton pump inhibitor in patients undergoing percutaneous coronary intervention. Kidney Res Clin Pract. 2015;34:98-102.
31. Danziger J, William JH, Scott DJ, et al. Protonenpumpeninhibitor use is associated with low serum magnesium concentrations. Kidney Int. 2013;83:692-699.
32. Begley J, Smith T, Barnett K, et al. Protonenpumpeninhibitor-assoziierte Hypomagnesiämie – ein Grund zur Sorge? Br J Clin Pharmacol. 2016;81:753-758.
33. Abraham NS, Hlatky MA, Antman EM, et al. ACCF/ACG/AHA 2010 expert consensus document on the concomitant use of proton pump inhibitors and thienopyridines: a focused update of the ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use. Am J Gastroenterol. 2010;105:2533-2549.
34. Melloni C, Washam JB, Jones WS, et al. Conflicting results between randomized trials and observational studies on the impact of proton pump inhibitors on cardiovascular events when coadministered with dual antiplatelet therapy: systematic review. Circ Cardiovasc Qual Outcomes. 2015;8:47-55.
35. FDA-Erinnerung zur Vermeidung der gleichzeitigen Anwendung von Plavix (Clopidogrel) und Omeprazol. www.fda.gov/Drugs/DrugSafety/ucm231161.htm. Accessed February 17, 2017.
36. Bundhun PK, Teeluck AR, Bhurtu A, Huang WQ. Ist die gleichzeitige Verwendung von Clopidogrel und Protonenpumpeninhibitoren immer noch mit erhöhten negativen kardiovaskulären Ergebnissen nach einer Koronarangioplastie assoziiert: eine systematische Überprüfung und Meta-Analyse kürzlich veröffentlichter Studien (2012-2016). BMC Cardiovasc Disord. 2017;17:3.