US Pharm. 2017;42(6)(Generic Drugs suppl):38-42.
ABSTRACT: Protonipumpun estäjät (Proton pump inhibitors, PPI) ovat erilaisten ruoansulatuskanavan sairauksien, kuten gastroesofageaalisen refluksitaudin, Helicobacter pyloriin liittyvien sairauksien sekä maha- ja pohjukaissuolihaavojen hoitoon käytettävien antisekretoristen aineiden luokka. Vaikka nämä aineet ovat tehokkaita happoja ehkäiseviä lääkkeitä, PPI-lääkkeiden käytöstä käydään usein keskustelua uusia mahdollisia haittavaikutuksia koskevien raporttien perusteella. Ylikäyttö ja lääkkeiden yhteisvaikutukset ovat PPI-valmisteisiin liittyviä ongelmia. Koska useita PPI-lääkkeitä on saatavana ilman reseptiä, niiden epätarkoituksenmukainen käyttö on lisäksi merkittävä huolenaihe. Apteekkarit voivat kaikissa toimintaympäristöissä vaikuttaa merkittävästi PPI-lääkkeiden epätarkoituksenmukaiseen käyttöön varmistamalla hoidon asianmukaisen aloittamisen ja jatkamisen, annostelun ja hoidon keston.
Protonipumpun estäjät (PPI-lääkkeet) ovat lääkeryhmä, jota käytetään yleisesti erilaisten gastrointestinaalisten häiriöiden hoitoon, mukaan lukien gastroesofageaalinen refluksitauti (gastroesofageal refluks disease, GERD), helikobakteerin aiheuttamat häiriöt sekä mahalaukun ja pohjukaissuolen haavat. Vaikka nämä eritystä ehkäisevät aineet ovat ensisijainen hoitomuoto monissa sairauksissa, luokkaa vaivaa ylikäyttö sekä raportit mahdollisesti vakavista haittavaikutuksista ja lääkkeiden yhteisvaikutuksista.1 Lisäksi PPI-valmisteilla hoidettujen sairauksien hoitoa hankaloittaa se, että useat näistä aineista ovat saatavilla ilman reseptiä. Tässä artikkelissa pyritään korostamaan asianmukaista käyttöä ja antamaan näyttöön perustuva kuvaus useista näiden aineiden uusista tai paljon keskustelua herättäneistä haittapuolista.
PPI-valmisteiden saatavuus
Kuusi erillistä PPI-valmistetta, joista viisi on saatavissa geneerisinä lääkkeinä, on saatavissa reseptillä (TAULUKKO 1).2-7 Pieniä annoksia omepratsolia, lansopratsolia ja tuotemerkillä varustettua versiota esomepratsolimagnesiumista on saatavana ilman reseptiä. Omepratsolia käytetään myös yhdessä natriumbikarbonaatin kanssa. Tässä artikkelissa keskitytään ensisijaisesti geneerisesti saatavilla oleviin, suun kautta annosteltaviin PPI-lääkkeisiin.
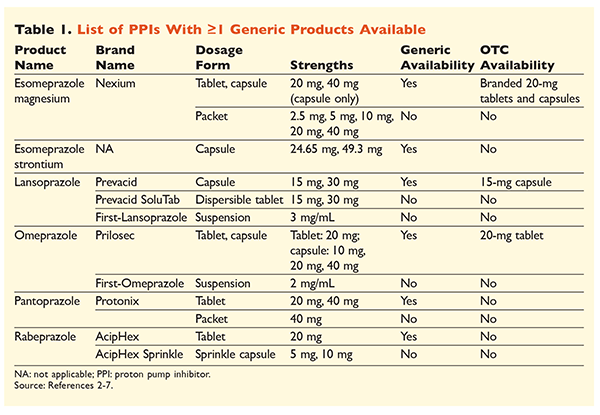
Esomepratsolistrontium hyväksyttiin FDA:ssa sen bioekvivalenssin perusteella esomepratsolimagnesiumin kanssa.3 Vaikka näiden kahden lääkkeen tuoteselosteet ovat hyvin samankaltaiset, niissä on kolme merkittävää eroa. Ensinnäkin esomepratsolistrontium on saatavana 24,65 mg:n ja 49,3 mg:n kapseleina, jotka vastaavat 20 mg:n ja 40 mg:n esomepratsolimagnesiumia. Toiseksi esomepratsolistrontiumilla ei ole FDA:n hyväksyntää käytettäväksi lapsipotilailla, kun taas esomepratsolimagnesium on hyväksytty käytettäväksi 1 kuukauden ikäisillä ja sitä vanhemmilla potilailla. Lopuksi esomepratsolistrontiumin käyttöä on vältettävä vaikeassa munuaisten vajaatoiminnassa, koska sitä ei ole tutkittu tässä väestössä. Esomepratsolimagnesiumille ei suositella annostuksen mukauttamista.3 Tässä artikkelissa käytetään termiä esomepratsoli kuvaamaan esomepratsolimagnesiumia.
Antotapa
Kaikki yleisesti saatavilla olevat PPI-valmisteet, mukaan lukien kapselit ja tabletit, on nieltävä kokonaisina jakamatta, murskaamatta tai pureskelematta.2-7 Omepratsoli-, lansopratsoli- ja esomepratsolikapselit voidaan avata ja ripotella sisältö omenasoseeseen potilaille, jotka eivät pysty nielemään suun kautta otettavia lääkemuotoja. Lisäksi lansopratsolikapselit voidaan ripotella 2 unssin omena-, tomaatti- tai appelsiinimehuun. Kaikki avattujen kapselien sisältöä sisältävät seokset on nieltävä välittömästi, eikä niitä saa säilyttää myöhempää käyttöä varten.2,4,5
Lansopratsoli, omepratsoli ja esomepratsoli on annettava ennen aterioita, mutta antoajankohtia koskevat erityissuositukset vaihtelevat. Omepratsoli tulisi antaa 30-60 minuuttia ennen ateriaa ja esomepratsoli vähintään 60 minuuttia ennen ateriaa; lansopratsolille ei ole määritetty ajankohtaa.2,4,5 Pantopratsoli voidaan antaa ruuan kanssa tai ilman ruokaa.6 Rabepratsoli tulisi ottaa aterian jälkeen pohjukaissuolihaavojen hoidossa ja aterian yhteydessä H pylori -bakteerin eliminoinnissa; kaikissa muissa käyttöaiheissa rabepratsoli voidaan ottaa ruuan kanssa tai ilman ruokaa.7
annostus ja hoidon kesto
Kun otetaan huomioon PPI-lääkkeiden maine erittäin tehokkaina ja yleisesti ottaen turvallisina, PPI-lääkkeiden merkittävä liikakäyttö on suuri huolenaihe.1 PPI-lääkkeitä annetaan usein käyttöaiheisiin, joiden käytöstä ei ole näyttöä, ja lisäksi näitä lääkkeitä määrätään usein suurempina annoksina kuin on tarpeen, ja niiden hoidon kesto on suositeltua pidempi.8,9 Kunkin PPI-lääkkeen hyväksytyt annostukset ja suositeltu hoidon kesto on esitetty TAULUKOISSA 2 ja 3. Seuraavassa esitetään hoitosuositukset, jotka poikkeavat FDA:n hyväksymistä suosituksista, sekä PPI-hoidon aloittamiseen, annosteluun ja kestoon liittyviä merkittäviä kliinisiä helmiä.
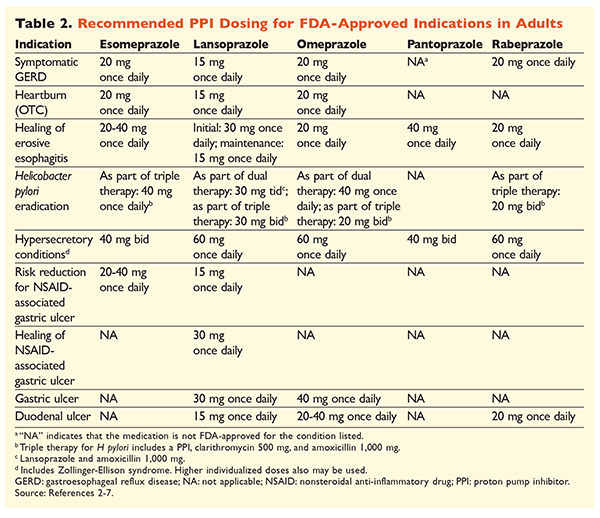
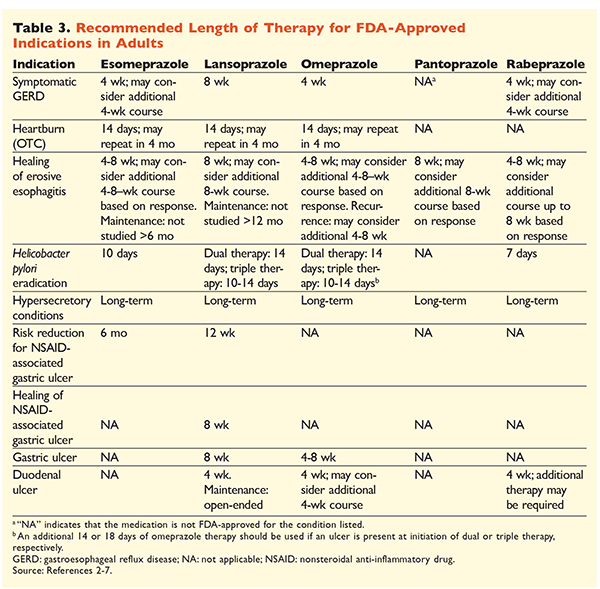
GLERD: GERD-potilailla kaikkia PPI-lääkkeitä pidetään yhtä tehokkaina, ja suositellaan kahdeksan viikon hoitoa millä tahansa saatavissa olevalla lääkkeellä.10 Potilaat, joiden oireet ovat hoidon jälkeen refraktäärisiä, voivat tarvita pitkäkestoista ylläpitävää hoitoa, jota annetaan kahdesti päivässä. On kuitenkin käytettävä pienintä tehokasta annosta, ja jos potilas ei reagoi hoitoon, on harkittava toista PPI-valmistetta.10 Vaihtoehtoisesti voidaan harkita tarpeen mukaan annettavaa PPI-hoitoa tai asteittaista siirtymistä histamiini2-reseptorin antagonistiin (H2RA).10 Hoito reseptivapaasti myytävällä PPI-valmisteella on rajoitettava 14 päivään, ja hoito on jatkettava korkeintaan neljän kuukauden välein.11
H pylorin aiheuttamat haavaumat: Käytettävästä PPI:stä riippuen FDA:n hyväksymiin H pylori -haavaumien hävittämisohjelmiin kuuluu kaksoishoito joko amoksisilliinilla tai klaritromysiinillä ja kolmoishoito molemmilla aineilla 7-14 vuorokauden ajan.2-5,7 Erityiset ohjeiden tukemat hoito-ohjelmat vaihtelevat FDA:n hyväksymiin hoito-ohjelmiin verrattuna, mutta hoidon suositeltu kesto on samankaltainen, ja kaikkien hoito-ohjelmien annosteluajankohta on 10-14 vuorokautta. 12 H pylorin hävittämisen jälkeen PPI-ylläpitohoito ei ole tarpeen.13 Yksityiskohtaisempi keskustelu erityisistä hoito-ohjelmista ei kuulu tämän artikkelin aihepiiriin.
Prophylaxis and Treatment of NSAID-Induced Ulcers: Kun ei-steroidisten tulehduskipulääkkeiden (NSAID) aiheuttama haavauma on kehittynyt, NSAID-hoidon tarve on arvioitava uudelleen. Jos NSAID-hoidon jatkaminen katsotaan aiheelliseksi, potilaille on jatkettava selektiivistä syklo-oksygenaasi-2-hoitoa pienimmällä tehokkaalla annoksella mahdollisimman lyhyen ajan yhdessä PPI:n kanssa.13
Profylaksiaa varten PPI:n aloittamista suositellaan vain potilailla, joilla on kohtalainen tai suuri NSAID:iin liittyvän GI-toksisuuden riski. Riskitekijöitä ovat ikä >65 vuotta, suuriannoksinen NSAID-hoito, aiempi komplisoitumaton haavauma ja samanaikainen aspiriinin (myös pieniannoksisen), kortikosteroidien tai antikoagulanttien käyttö. Potilaita, joilla katsotaan olevan kohtalainen riski saada NSAID:n aiheuttamaa GI-toksisuutta, ovat potilaat, joilla on yksi tai kaksi näistä riskitekijöistä, kun taas suuren riskin potilailla on enemmän kuin kaksi riskitekijää tai heillä on aiemmin ollut komplisoitunut mahahaava, erityisesti jos se on ollut hiljattain.14 PPI-hoitoa on perusteltua jatkaa niin kauan kuin kohtalaisen tai suuren riskin potilas jatkaa NSAID-hoitoa.13
Idiopaattinen haavauma: Haavaumat, joilla ei ole selvästi tunnistettavaa syytä, uusiutuvat todennäköisesti potilailla, joita ei hoideta happamuudensäätöhoidolla. Suuntaviivoissa ei suositella selkeästi, kuinka kauan potilaita tulisi hoitaa ylläpitohoidolla, mutta niiden mukaan jatkuva PPI-hoito vähentää toistuvien haavaumien muodostumisen riskiä.13
Turvallisuus
PPI:itä pidetään yleisesti hyvin siedettynä lääkeryhmänä.1 Useat turvallisuusongelmat ovat kuitenkin pitkään varjostaneet niiden mainetta, mukaan lukien Clostridium difficile -bakteerin aiheuttaman ripulin, keuhkokuumeen ja luunmurtumien lisääntynyt riski.15,16 Viime aikoina on esitetty huolia dementiasta ja kroonisesta munuaissairaudesta, ja keskustelut hypomagnesemiasta ja teoreettisesta lääkeaineinteraktiosta klopidogreelin kanssa ovat jatkuneet.
Dementia: Kahdessa viimeaikaisessa tutkimuksessa on esitetty, että pitkäaikainen PPI:n käyttö iäkkäillä saattaa lisätä dementian riskiä.17,18 Ehdotettu mekanismi tämän havainnon taustalla on se, että PPI:t edistävät beeta-amyloidiplakkien kehittymistä, joka on ehdotettu Alzheimerin taudin patofysiologiaksi.15 Tutkimuksen rajoitukset eivät kuitenkaan tue lopullista syy-yhteyttä PPI:n käytön ja dementian lisääntyneen esiintyvyyden välille.19
Renaaliset komplikaatiot: Vaikka PPI:t on laajalti tunnustettu akuutin interstitiaalisen nefriitin yleiseksi aiheuttajaksi, uudemmat tiedot viittaavat siihen, että nämä aineet ovat osallisina myös muiden munuaiskomplikaatioiden kehittymisessä.15,20 Kolmessa viimeaikaisessa tutkimuksessa on saatu viitteitä siitä, että PPI:t saattaisivat olla vastuussa kroonisen munuaissairauden lisääntyneestä riskistä ja etenemisestä loppuvaiheen munuaissairaudeksi.20-22 Näitä havainnointitutkimuksia on kuitenkin tulkittava varovaisuutta osoittaen, sillä kausaliteettia ei voida vahvistaa.23
Hypomagnesemia: Vuonna 2011 FDA antoi varoituksen, jonka mukaan PPI-lääkkeiden pitkäaikainen, yli vuoden kestävä käyttö voi johtaa hypomagnesemiaan.24 Sittemmin useat mittavat tutkimukset ovat tukeneet tätä havaintoa.25-29 PPI-lääkkeiden ja hypomagnesemian välinen yhteys ei kuitenkaan ole yksiselitteinen, ja sitä vaikeuttavat ulkopuoliset riskitekijät.30-32 Tällä hetkellä kliinisesti merkittävää PPI:n aiheuttamaa hypomagnesemiaa pidetään harvinaisena, ja sitä esiintyy yleisemmin samanaikaisen diureettien käytön yhteydessä.31,32 Seurantaa suositellaan vain potilaille, joilla on muita riskitekijöitä.32
Lääkeinteraktio klopidogreelin kanssa: Klopidogreelillä on tärkeä rooli kardiovaskulaarisen riskin vähentämisessä, mutta siihen liittyy ruoansulatuskanavan verenvuotoja, erityisesti potilailla, joilla on suurentunut riski. GI-suojaus PPI:llä otetaan usein käyttöön potilailla, joilla on suurempi todennäköisyys saada GI-verenvuoto, mukaan lukien potilaat, joilla on aiempi ylemmän GI:n verenvuoto; korkea ikä; antikoagulanttien, kortikosteroidien tai NSAID-lääkkeiden (mukaan lukien aspiriini) samanaikainen käyttö; ja/tai H pylori-infektio.33
PPI:iden ajatellaan estävän CYP2C19-entsyymiä, joka on ensisijainen reitti, jonka kautta klopidogreeli aktivoituu.33 Tämä yhteisvaikutus voi teoriassa vähentää klopidogreelin verihiutaleiden muodostumista estäviä vaikutuksia ja lisätä haitallisten sydän- ja verisuonitautitapahtumien riskiä.33 Sekä farmakokineettisistä tutkimuksista että lopputulostutkimuksista saatujen epäjohdonmukaisten tulosten perusteella tämän yhteisvaikutuksen kliininen merkitys on kuitenkin epävarma.34
Ei myöskään ole johdonmukaista näyttöä yksittäisten PPI:iden todellisesta vaikutuksesta klopidogreelin vaikutuksiin.33 Viimeisimpien FDA:n suositusten mukaan pantopratsoli on muita PPI:itä turvallisempi valinta, kun taas omepratsolin katsotaan olevan riskialttein.35 Tämänhetkiset tiedot tukevat edelleen tätä päätelmää, mutta lisätutkimukset ovat tarpeen sen varmistamiseksi, onko PPI:iden välillä eroa.36
On tärkeää punnita verihiutaleiden muodostumista estävän hoidon hyötyjä ja riskejä yksinään tai yhdessä PPI:n kanssa, kun päätetään ruoansulatuskanavaa suojaavan hoidon lisäämisestä. Potilailla, joilla on suuri GI-komplikaatioiden riski, PPI-hoidon hyödylliset vaikutukset voivat olla suuremmat kuin trombosyyttihoidon heikentynyt teho, mikä on osoitettu epäjohdonmukaisesti. Potilaille, joilla GI-komplikaatioiden riski on pienempi, H2RA-hoito voi olla järkevä hoitovaihtoehto, vaikka tämän luokan on osoitettu olevan vähemmän tehokas kuin PPI-valmisteet tässä käyttöaiheessa.33
Johtopäätökset
Apteekkarit kaikissa toimintaympäristöissä voivat vaikuttaa merkittävästi PPI-valmisteiden epätarkoituksenmukaiseen käyttöön varmistamalla hoidon asianmukaisen aloittamisen ja jatkamisen, annostelun ja hoidon keston. Koska näiden lääkkeiden turvallisuusprofiileista saadaan jatkuvasti ristiriitaisia tietoja, PPI-lääkkeiden pitkäaikainen käyttö monimutkaistuu. Varmistamalla, että pienintä sopivaa annosta käytetään lyhimmän tarvittavan ajan, farmaseutit voivat auttaa estämään potilaiden tarpeettoman altistumisen mahdollisille haitoille.
1. Heidelbaugh JJ, Kim AH, Chang R, Walker PC. Protonipumpun estäjien liikakäyttö: mitä kliinikon on tiedettävä. Therap Adv Gastroenterol. 2012;5:219-232.
2. Nexiumin (esomepratsolimagnesium) pakkausseloste. Wilmington, DE: AstraZeneca Pharmaceuticals LP; joulukuu 2016.
3. Esomepratsoli-strontium-pakkausseloste. Glasgow, KY: Amneal Pharmaceuticals; joulukuu 2014.
4. Prevacid (lansopratsoli) pakkausseloste. Deerfield, IL: Takeda Pharmaceuticals America, Inc; lokakuu 2016.
5. Prilosec (omepratsoli) pakkausseloste. Wilmington, DE: AstraZeneca Pharmaceuticals LP; joulukuu 2016.
6. Protonix (pantopratsoli) pakkausseloste. Philadelphia, PA: Wyeth Pharmaceuticals Inc. Lokakuu 2016.
7. AcipHex (rabepratsoli) pakkausseloste. Woodcliff Lake, NJ: Eisai Inc; huhtikuu 2016.
8. Chia CT, Lim WP, Vu CK. Protonipumpun estäjien epätarkoituksenmukainen käyttö paikallisessa ympäristössä. Singapore Med J. 2014;55:363-366.
9. Kelly OB, Dillane C, Patchett SE, et al. The inappropriate prescription of oral proton pump inhibitors in the hospital setting: a prospective cross-sectional study. Dig Dis Sci. 2015;60:2280-2286.
10. Katz PO, Gerson LB, Vela MF. Suuntaviivat gastroesofageaalisen refluksitaudin diagnostiikkaa ja hoitoa varten. Am J Gastroenterol. 2013;108:308-328.
11. FDA Drug Safety Communication: Mahdollisesti lisääntynyt lonkan, ranteen ja selkärangan murtumien riski protonipumpun estäjien käytön yhteydessä. www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPatientsandProviders/ucm213206.htm. Viitattu 17. helmikuuta 2017.
12. Chey WD, Leontiadis GI, Howden CW, Moss SF. ACG:n kliininen ohje: Helicobacter pylori -infektion hoito. Am J Gastroenterol. 2017;112:212-239.
13. Laine L, Jensen DM. Haavaista verenvuotoa sairastavien potilaiden hoito. Am J Gastroenterol. 2012;107:345-360.
14. Lanza FL, Chan FK, Quigley EM. Suuntaviivat tulehduskipulääkkeisiin liittyvien haavakomplikaatioiden ehkäisemiseksi. Am J Gastroenterol. 2009;104:728-738.
15. Eusebi LH, Rabitti S, Artesiani ML, et al. Protonipumpun estäjät: pitkäaikaisen käytön riskit. J Gastroenterol Hepatol. 2017; Jan 16 .
16. Abramowitz J, Thakkar P, Isa A, et al. Adverse event reporting for proton pump inhibitor therapy: an overview of systematic reviews. Otolaryngol Head Neck Surg. 2016;155:547-554.
17. Haenisch B, von Holt K, Wiese B, ym. dementian riski iäkkäillä potilailla protonipumpun estäjien käytön yhteydessä. Eur Arch Psychiatry Clin Neurosci. 2015;265:419-428.
18. Gomm W, von Holt K, Thomé F, et al. Association of proton pump inhibitors with risk of dementia: a pharmacoepidemiological claims data analysis. JAMA Neurol. 2016;73:410-416.
19. Kuller LH. Lisäävätkö protonipumpun estäjät dementian riskiä? JAMA Neurol. 2016;73:379-381.
20. Arora P, Gupta A, Golzy M, et al. Protonipumpun estäjiin liittyy lisääntynyt riski kroonisen munuaissairauden kehittymiselle. BMC Nephrol. 2016;17:112.
21. Xie Y, Bowe B, Li T, et al. Protonipumpun estäjät ja riski sairastua CKD:hen ja etenemiseen ESRD:hen. J Am Soc Nephrol. 2016;27:3153-3163.
22. Lazarus B, Chen Y, Wilson FP, et al. Protonipumpun estäjän käyttö ja kroonisen munuaissairauden riski. JAMA Intern Med. 2016;176:238-246.
23. Kia L, Kahrilas PJ. Terapia: Krooniseen PPI:n käyttöön liittyvät riskit – signaali vai kohina? Nat Rev Gastroenterol Hepatol. 2016;13(5):253-254.
24. FDA Drug Safety Communication: matalat magnesiumpitoisuudet voivat liittyä protonipumpun estäjälääkkeiden (PPI) pitkäaikaiseen käyttöön. www.fda.gov/Drugs/DrugSafety/ucm245011.htm. Viitattu 17. helmikuuta 2017.
25. Kieboom BC, Kiefte-de Jong JC, Eijgelsheim M, et al. Protonipumpun estäjät ja hypomagnesemia väestössä: väestöpohjainen kohorttitutkimus. Am J Kidney Dis. 2015;66:775-782.
26. Park CH, Kim EH, Roh YH, et al. The association between the use of proton pump inhibitors and the risk of hypomagnesemia: a systematic review and meta-analysis. PLoS One. 2014;9:e112558.
27. Luk CP, Parsons R, Lee YP, Hughes JD. Protonipumpun estäjiin liittyvä hypomagnesemia: mitä FDA:n tiedot kertovat meille? Ann Pharmacother. 2013;47:773-780.
28. Cheungpasitporn W, Thongprayoon C, Kittanamongkolchai W, et al. Protonipumpun estäjät yhteydessä hypomagnesemiaan: systemaattinen katsaus ja meta-analyysi havainnointitutkimuksista. Ren Fail. 2015;37:1237-1241.
29. Markovits N, Loebstein R, Halkin H, et al. The association of proton pump inhibitors and hypomagnesemia in the community setting. J Clin Pharmacol. 2014;54:889-895.
30. Park SH, Lee SH, Lee JS, et al. Seerumin magnesiumpitoisuuden muutokset protonipumpun estäjän käytön jälkeen potilailla, joille tehdään perkutaaninen sepelvaltimotoimenpide. Kidney Res Clin Pract. 2015;34:98-102.
31. Danziger J, William JH, Scott DJ, et al. Protonipumpun estäjän käyttö liittyy alhaisiin seerumin magnesiumpitoisuuksiin. Kidney Int. 2013;83:692-699.
32. Begley J, Smith T, Barnett K, et al. Protonipumpun estäjiin liittyvä hypomagnesemia-a cause for concern? Br J Clin Pharmacol. 2016;81:753-758.
33. Abraham NS, Hlatky MA, Antman EM, et al. ACCF/ACG/AHA 2010 expert consensus document on the concomitant use of proton pump inhibitors and thienopyridines: a focused update of the ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use. Am J Gastroenterol. 2010;105:2533-2549.
34. Melloni C, Washam JB, Jones WS, et al. Ristiriitaisia tuloksia satunnaistettujen tutkimusten ja havainnointitutkimusten välillä protonipumpun estäjien vaikutuksesta sydän- ja verisuonitapahtumiin silloin, kun niitä annetaan yhdessä trombosyyttien kaksoishoidon kanssa: systemaattinen katsaus. Circ Cardiovasc Qual Outcomes. 2015;8:47-55.
35. FDA:n muistutus Plavixin (klopidogreelin) ja omepratsolin samanaikaisen käytön välttämisestä. www.fda.gov/Drugs/DrugSafety/ucm231161.htm. Viitattu 17. helmikuuta 2017.
36. Bundhun PK, Teeluck AR, Bhurtu A, Huang WQ. Liittyykö klopidogreelin ja protonipumpun estäjien samanaikainen käyttö edelleen lisääntyneisiin haitallisiin kardiovaskulaarisiin tuloksiin sepelvaltimoiden pallolaajennuksen jälkeen: Systemaattinen katsaus ja meta-analyysi äskettäin julkaistuista tutkimuksista (2012-2016). BMC Cardiovasc Disord. 2017;17:3.