US Pharm. 2017;42(6)(Generic Drugs suppl):38-42.
ABSTRACT: Gli inibitori della pompa protonica (PPI) sono una classe di agenti antisecretori usati per trattare varie condizioni gastrointestinali, come la malattia da reflusso gastroesofageo, i disturbi legati all’Helicobacter pylori e le ulcere gastriche e duodenali. Anche se questi agenti sono efficaci soppressori dell’acido, l’uso dei PPI è frequentemente discusso sulla base delle segnalazioni di nuovi potenziali eventi avversi. L’uso eccessivo e le interazioni farmaco-farmaco sono problemi associati ai PPI. Inoltre, poiché molti PPI sono disponibili OTC, l’uso inappropriato di questi agenti è una preoccupazione significativa. I farmacisti in tutti i contesti possono avere un profondo impatto sull’uso inappropriato dei PPI assicurando l’inizio e la continuazione appropriati della terapia, il dosaggio e la durata del trattamento.
Gli inibitori della pompa protonica (PPI) sono una classe di farmaci comunemente usati per il trattamento di vari disturbi gastrointestinali (GI), compresa la malattia da reflusso gastroesofageo (GERD), i disturbi legati all’Helicobacter pylori e le ulcere gastriche e duodenali. Sebbene questi agenti antisecretori siano il trattamento preferito per numerose condizioni, la classe è afflitta da un uso eccessivo e da segnalazioni di effetti avversi potenzialmente gravi e interazioni farmaco-farmaco.1 Inoltre, la gestione del paziente delle condizioni trattate con i PPI è complicata dalla disponibilità OTC di molti di questi agenti. Questo articolo ha lo scopo di evidenziare l’uso appropriato e di fornire una descrizione basata sull’evidenza di diversi svantaggi nuovi o molto discussi di questi agenti.
Disponibilità degli IPP
Sei unici IPP, cinque dei quali sono disponibili genericamente, sono ottenibili su prescrizione (TABELLA 1).2-7 Basse dosi di omeprazolo, lansoprazolo, e una versione di marca di esomeprazolo magnesio sono disponibili OTC. L’omeprazolo è anche usato in un prodotto coformulato con bicarbonato di sodio. Questo articolo si concentrerà principalmente sui PPI genericamente disponibili, dosati per via orale.
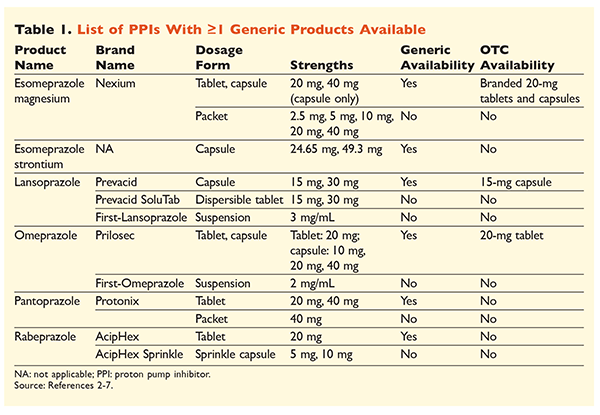
L’esomeprazolo stronzio è stato approvato dalla FDA sulla base della sua bioequivalenza all’esomeprazolo magnesio.3 Sebbene l’etichetta del prodotto per questi due agenti sia molto simile, esistono tre notevoli differenze. In primo luogo, esomeprazolo stronzio è disponibile in capsule da 24,65 mg e 49,3 mg, che sono equivalenti a esomeprazolo magnesio 20 mg e 40 mg, rispettivamente. In secondo luogo, l’esomeprazolo stronzio non è approvato dalla FDA per l’uso in pazienti pediatrici, mentre l’esomeprazolo magnesio è approvato per l’uso in quelli di 1 mese e più. Infine, l’uso di esomeprazolo stronzio deve essere evitato nella compromissione renale grave perché non è stato studiato in questa popolazione. Nessun aggiustamento del dosaggio è raccomandato per l’esomeprazolo magnesio.3 Per gli scopi di questo articolo, il termine esomeprazolo sarà usato per descrivere l’esomeprazolo magnesio.
Somministrazione
Tutti gli IPP genericamente disponibili, comprese le capsule e le compresse, devono essere deglutiti interi senza essere divisi, schiacciati o masticati.2-7 Le capsule di omeprazolo, lansoprazolo ed esomeprazolo possono essere aperte e il contenuto cosparso su salsa di mele per i pazienti incapaci di deglutire le forme di dosaggio orali. Inoltre, le capsule di lansoprazolo possono essere spruzzate in 2 once di succo di mela, pomodoro o arancia. Qualsiasi miscela contenente il contenuto di capsule aperte deve essere inghiottita immediatamente e non deve essere conservata per uso futuro.2,4,5
Lansoprazolo, omeprazolo ed esomeprazolo devono essere somministrati prima dei pasti, ma le raccomandazioni specifiche sui tempi di somministrazione variano. L’omeprazolo deve essere somministrato da 30 a 60 minuti prima di un pasto, e l’esomeprazolo almeno 60 minuti prima; un lasso di tempo non è specificato per il lansoprazolo.2,4,5 Il pantoprazolo può essere somministrato con o senza cibo.6 Il rabeprazolo deve essere assunto dopo un pasto per le ulcere duodenali e con un pasto per l’eradicazione dell’H pylori; per tutte le altre indicazioni, il rabeprazolo può essere assunto con o senza cibo.7
Dosaggio e durata della terapia
Data la reputazione dei PPI di essere molto efficaci e generalmente sicuri, un significativo sovrautilizzo dei PPI è una grande preoccupazione.1 Non solo i PPI sono spesso somministrati per indicazioni senza prove a sostegno del loro uso, ma questi farmaci sono anche frequentemente prescritti a dosi più elevate del necessario per una durata del trattamento che si estende oltre i tempi raccomandati.8,9 Il dosaggio approvato di ogni PPI e la durata raccomandata della terapia sono riportati nelle TABELLE 2 e 3.
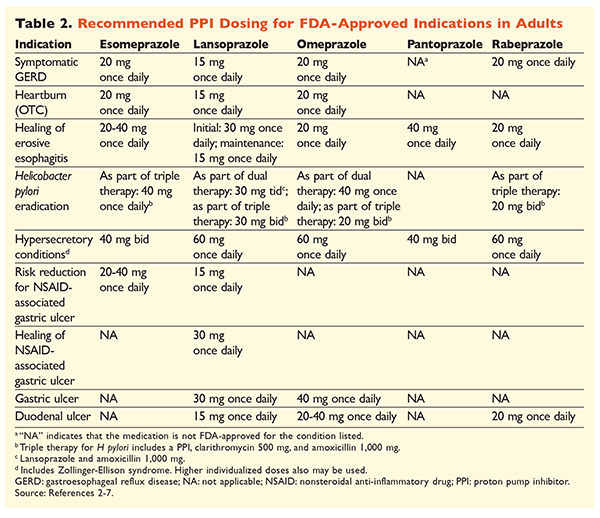
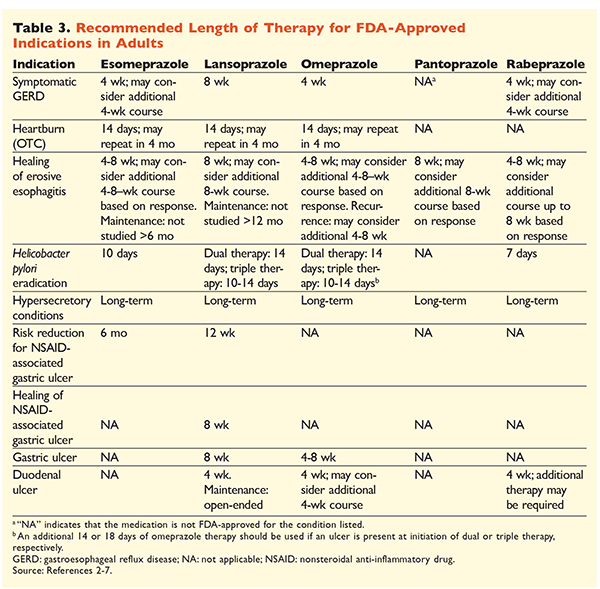
GERD: Nei pazienti con GERD, tutti gli IPP sono considerati ugualmente efficaci, e si raccomanda un ciclo di 8 settimane di terapia con qualsiasi agente disponibile.10 I pazienti con sintomi refrattari alla terapia dopo 2 o 3 mesi possono richiedere una terapia di mantenimento a lungo termine con dosi biorarie. Tuttavia, dovrebbe essere usata la dose efficace più bassa, e dovrebbe essere preso in considerazione un diverso PPI se il paziente non risponde alla terapia.10 In alternativa, può essere presa in considerazione una terapia PPI al bisogno o un approccio graduale ad un antagonista del recettore dell’istamina2 (H2RA).10 Il trattamento con un PPI da banco dovrebbe essere limitato a 14 giorni, con un ritiro non più frequente di ogni 4 mesi.11
Ulcere associate all’H pylori: A seconda del PPI utilizzato, i regimi approvati dalla FDA per l’eradicazione dell’H pylori includono una doppia terapia con amoxicillina o claritromicina e una tripla terapia con entrambi gli agenti per 7-14 giorni.2-5,7 I regimi di trattamento specifici supportati dalle linee guida variano rispetto a quelli approvati dalla FDA, ma la durata raccomandata della terapia è simile, con tutti i regimi che prevedono un periodo di dosaggio da 10 a 14 giorni.12 Dopo l’eradicazione dell’H pylori, la terapia di mantenimento con PPI non è necessaria.13 Una discussione più dettagliata dei regimi specifici va oltre lo scopo di questo articolo.
Profilassi e trattamento delle ulcere indotte da FANS: Dopo lo sviluppo di un’ulcera associata a un farmaco antinfiammatorio non steroideo (FANS), la necessità della terapia con FANS dovrebbe essere rivalutata. Se si ritiene opportuno continuare la terapia con FANS, i pazienti devono essere mantenuti in terapia con cicloossigenasi-2 selettiva alla dose più bassa efficace per la durata più breve possibile in combinazione con un PPI.13
Per la profilassi, l’inizio di un PPI è raccomandato solo in pazienti con rischio moderato o alto di tossicità gastrointestinale legata ai FANS. I fattori di rischio includono l’età >65 anni, la terapia con FANS ad alto dosaggio, una precedente storia di ulcera non complicata e l’uso concomitante di aspirina (anche a basso dosaggio), corticosteroidi o anticoagulanti. I pazienti considerati a rischio moderato per la tossicità GI indotta dai FANS includono quelli con uno o due di questi fattori di rischio, mentre i pazienti ad alto rischio hanno più di due fattori di rischio o una storia di ulcera peptica complicata in precedenza, specialmente se recente.14 È ragionevole continuare la terapia con PPI finché il paziente a rischio moderato o alto rimane in terapia con FANS.13
Ulcera idiopatica: Le ulcere senza una causa chiaramente identificabile hanno la probabilità di ripresentarsi nei pazienti che non sono trattati con la terapia antiacida. Le linee guida non raccomandano chiaramente per quanto tempo i pazienti debbano essere trattati con la terapia di mantenimento, ma suggeriscono che la terapia PPI in corso riduce il rischio di formazione di ulcere ricorrenti.13
Sicurezza
Gli IPP sono generalmente considerati una classe di farmaci ben tollerata.1 Tuttavia, diversi problemi di sicurezza hanno a lungo afflitto la loro reputazione, tra cui un aumento del rischio di diarrea associata a Clostridium difficile, polmonite acquisita in comunità e fratture ossee.15,16 Più recentemente, sono state sollevate preoccupazioni per la demenza e la malattia renale cronica, e sono continuati i dibattiti riguardanti l’ipomagnesiemia e una teorica interazione farmaco-farmaco con clopidogrel.
Dementia: Due studi recenti hanno suggerito un potenziale aumento del rischio di demenza con l’uso a lungo termine di PPI negli anziani.17,18 Un meccanismo proposto dietro questa scoperta è che i PPI promuovono lo sviluppo di placche beta-amiloidi, una proposta patofisiologica del morbo di Alzheimer.15 Tuttavia, i limiti degli studi non supportano una relazione causale conclusiva tra l’uso di PPI e un’aumentata incidenza di demenza.19
Complicazioni renali: Sebbene i PPI siano stati ampiamente riconosciuti come causa comune di nefrite interstiziale acuta, dati più recenti implicano anche questi agenti nello sviluppo di altre complicazioni renali.15,20 Tre studi recenti hanno suggerito che i PPI possono essere responsabili di un aumento del rischio di malattia renale cronica e di progressione verso la malattia renale allo stadio terminale.20-22 Tuttavia, questi studi osservazionali devono essere interpretati con cautela, poiché la causalità non può essere confermata.23
Ipomagnesemia: Nel 2011, la FDA ha emesso un avviso che l’uso prolungato di PPI per periodi superiori a 1 anno può provocare ipomagnesiemia.24 Da allora, diversi studi importanti hanno sostenuto questa scoperta.25-29 La relazione tra PPI e ipomagnesiemia non è definitiva, tuttavia, ed è complicata da fattori di rischio esterni.30-32 Attualmente, l’ipomagnesiemia clinicamente significativa indotta da PPI è considerata rara e si verifica più comunemente con l’uso concomitante di diuretici.31,32 Il monitoraggio è raccomandato solo nei pazienti con fattori di rischio aggiuntivi.32
Interazione farmacologica con Clopidogrel: Il clopidogrel gioca un ruolo importante nella riduzione del rischio cardiovascolare, ma è associato a sanguinamenti gastrointestinali, soprattutto nei pazienti a rischio aumentato. La protezione gastrointestinale con gli IPP è spesso attuata in pazienti che hanno maggiori probabilità di avere un’emorragia gastrointestinale, compresi quelli con una precedente emorragia gastrointestinale superiore; età avanzata; uso concomitante di anticoagulanti, corticosteroidi o FANS (compresa l’aspirina); e/o infezione da H pylori.33
Si ritiene che gli IPP inibiscano l’enzima CYP2C19, la via primaria attraverso la quale il clopidogrel viene attivato.33 Questa interazione può teoricamente diminuire gli effetti antipiastrinici del clopidogrel e aumentare il rischio di esiti cardiovascolari avversi.33 Sulla base di risultati incoerenti provenienti sia da studi farmacocinetici che da studi sugli esiti, tuttavia, il significato clinico di questa interazione è incerto.34
Inoltre, c’è una mancanza di coerenza nelle prove riguardanti il vero impatto dei singoli PPI sugli effetti del clopidogrel.33 Le ultime raccomandazioni della FDA suggeriscono che il pantoprazolo è una scelta più sicura rispetto agli altri PPI, mentre l’omeprazolo è ritenuto il più rischioso.35 I dati attuali continuano a sostenere questa conclusione, ma sono necessari ulteriori studi per confermare se esiste una differenza tra i PPI.36
È importante soppesare i benefici e i rischi della terapia antipiastrinica da sola o in combinazione con un PPI quando si decide di aggiungere una terapia gastroprotettiva. Nei pazienti ad alto rischio di complicazioni gastrointestinali, gli effetti benefici della terapia con PPI possono essere maggiori della minore efficacia della terapia antiaggregante, che è stata dimostrata in modo incoerente. Per i pazienti a basso rischio di complicazioni gastrointestinali, un H2RA può essere un’opzione di trattamento ragionevole, anche se questa classe ha dimostrato di essere meno efficace degli IPP per questa indicazione.33
Conclusione
I farmacisti in tutti i contesti possono avere un profondo impatto sull’uso inappropriato degli IPP assicurando un corretto inizio e proseguimento della terapia, il dosaggio e la durata del trattamento. Poiché continuano ad emergere dati contrastanti sui profili di sicurezza di questi farmaci, l’uso a lungo termine degli IPP diventa più complicato. Assicurandosi che la dose più bassa appropriata sia usata per la durata più breve necessaria, i farmacisti possono aiutare a prevenire l’inutile esposizione dei pazienti a potenziali danni.
1. Heidelbaugh JJ, Kim AH, Chang R, Walker PC. L’uso eccessivo di inibitori della pompa protonica: ciò che il medico deve sapere. Therap Adv Gastroenterol. 2012;5:219-232.
2. Nexium (esomeprazolo magnesio) foglietto illustrativo. Wilmington, DE: AstraZeneca Pharmaceuticals LP; dicembre 2016.
3. Esomeprazolo stronzio foglietto illustrativo. Glasgow, KY: Amneal Pharmaceuticals; dicembre 2014.
4. Prevacid (lansoprazolo) foglietto illustrativo. Deerfield, IL: Takeda Pharmaceuticals America, Inc; ottobre 2016.
5. Prilosec (omeprazolo) foglietto illustrativo. Wilmington, DE: AstraZeneca Pharmaceuticals LP; dicembre 2016.
6. Protonix (pantoprazolo) foglietto illustrativo. Philadelphia, PA: Wyeth Pharmaceuticals Inc. Ottobre 2016.
7. AcipHex (rabeprazolo) foglietto illustrativo. Woodcliff Lake, NJ: Eisai Inc; aprile 2016.
8. Chia CT, Lim WP, Vu CK. Uso inappropriato di inibitori di pompa protonica in un ambiente locale. Singapore Med J. 2014;55:363-366.
9. Kelly OB, Dillane C, Patchett SE, et al. La prescrizione inappropriata di inibitori di pompa protonica orale nel contesto ospedaliero: uno studio prospettico cross-sectional. Dig Dis Sci. 2015;60:2280-2286.
10. Katz PO, Gerson LB, Vela MF. Linee guida per la diagnosi e la gestione della malattia da reflusso gastroesofageo. Am J Gastroenterol. 2013;108:308-328.
11. FDA Drug Safety Communication: possibile aumento del rischio di fratture dell’anca, del polso e della colonna vertebrale con l’uso di inibitori della pompa protonica. www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPatientsandProviders/ucm213206.htm. Accesso 17 febbraio 2017.
12. Chey WD, Leontiadis GI, Howden CW, Moss SF. Linea guida clinica ACG: trattamento dell’infezione da Helicobacter pylori. Am J Gastroenterol. 2017;112:212-239.
13. Laine L, Jensen DM. Gestione dei pazienti con sanguinamento dell’ulcera. Am J Gastroenterol. 2012;107:345-360.
14. Lanza FL, Chan FK, Quigley EM. Linee guida per la prevenzione delle complicazioni dell’ulcera legate ai FANS. Am J Gastroenterol. 2009;104:728-738.
15. Eusebi LH, Rabitti S, Artesiani ML, et al. Inibitori di pompa protonica: rischi di uso a lungo termine. J Gastroenterol Hepatol. 2017; Jan 16 .
16. Abramowitz J, Thakkar P, Isa A, et al. Segnalazione di eventi avversi per la terapia con inibitori della pompa protonica: una panoramica delle revisioni sistematiche. Otolaryngol Head Neck Surg. 2016;155:547-554.
17. Haenisch B, von Holt K, Wiese B, et al. Rischio di demenza nei pazienti anziani con l’uso di inibitori della pompa protonica. Eur Arch Psychiatry Clin Neurosci. 2015;265:419-428.
18. Gomm W, von Holt K, Thomé F, et al. Associazione di inibitori della pompa protonica con il rischio di demenza: un’analisi dei dati di reclami pharmacoepidemiologici. JAMA Neurol. 2016;73:410-416.
19. Kuller LH. Gli inibitori della pompa protonica aumentano il rischio di demenza? JAMA Neurol. 2016;73:379-381.
20. Arora P, Gupta A, Golzy M, et al. Gli inibitori della pompa protonica sono associati ad un aumento del rischio di sviluppo di malattia renale cronica. BMC Nephrol. 2016;17:112.
21. Xie Y, Bowe B, Li T, et al. Inibitori della pompa protonica e rischio di incidente CKD e progressione verso ESRD. J Am Soc Nephrol. 2016;27:3153-3163.
22. Lazarus B, Chen Y, Wilson FP, et al. Uso di inibitore di pompa protonica e il rischio di malattia renale cronica. JAMA Intern Med. 2016;176:238-246.
23. Kia L, Kahrilas PJ. Terapia: rischi associati all’uso cronico di PPI – segnale o rumore? Nat Rev Gastroenterol Hepatol. 2016;13(5):253-254.
24. FDA Drug Safety Communication: bassi livelli di magnesio possono essere associati all’uso a lungo termine di farmaci inibitori della pompa protonica (PPI). www.fda.gov/Drugs/DrugSafety/ucm245011.htm. Accesso 17 febbraio 2017.
25. Kieboom BC, Kiefte-de Jong JC, Eijgelsheim M, et al. Inibitori della pompa protonica e ipomagnesiemia nella popolazione generale: uno studio di coorte basato sulla popolazione. Am J Kidney Dis. 2015;66:775-782.
26. Park CH, Kim EH, Roh YH, et al. L’associazione tra l’uso di inibitori della pompa protonica e il rischio di ipomagnesiemia: una revisione sistematica e meta-analisi. PLoS One. 2014;9:e112558.
27. Luk CP, Parsons R, Lee YP, Hughes JD. Ipomagnesiemia associata a inibitori della pompa protonica: cosa ci dicono i dati della FDA? Ann Pharmacother. 2013;47:773-780.
28. Cheungpasitporn W, Thongprayoon C, Kittanamongkolchai W, et al. Inibitori della pompa protonica legati a ipomagnesiemia: una revisione sistematica e meta-analisi di studi osservazionali. Ren Fail. 2015;37:1237-1241.
29. Markovits N, Loebstein R, Halkin H, et al. L’associazione di inibitori della pompa protonica e ipomagnesiemia nel contesto della comunità. J Clin Pharmacol. 2014;54:889-895.
30. Park SH, Lee SH, Lee JS, et al. Cambiamenti nella concentrazione di magnesio nel siero dopo l’uso di un inibitore di pompa protonica in pazienti sottoposti a intervento coronarico percutaneo. Kidney Res Clin Pract. 2015;34:98-102.
31. Danziger J, William JH, Scott DJ, et al. uso inibitore della pompa protonica è associato a basse concentrazioni di magnesio nel siero. Kidney Int. 2013;83:692-699.
32. Begley J, Smith T, Barnett K, et al. Inibitore della pompa protonica associato ipomagnesiemia-un motivo di preoccupazione? Br J Clin Pharmacol. 2016;81:753-758.
33. Abraham NS, Hlatky MA, Antman EM, et al. ACCF/ACG/AHA 2010 expert consensus document on the concomitant use of proton pump inhibitors and thienopyridines: a focused update of the ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use. Am J Gastroenterol. 2010;105:2533-2549.
34. Melloni C, Washam JB, Jones WS, et al. Risultati contrastanti tra studi randomizzati e studi osservazionali sull’impatto degli inibitori di pompa protonica sugli eventi cardiovascolari quando co-somministrati con doppia terapia antipiastrinica: revisione sistematica. Circ Cardiovasc Qual Outcomes. 2015;8:47-55.
35. FDA promemoria per evitare l’uso concomitante di Plavix (clopidogrel) e omeprazolo. www.fda.gov/Drugs/DrugSafety/ucm231161.htm. Accessed February 17, 2017.
36. Bundhun PK, Teeluck AR, Bhurtu A, Huang WQ. L’uso concomitante di clopidogrel e inibitori di pompa protonica è ancora associato a un aumento degli esiti cardiovascolari avversi dopo l’angioplastica coronarica?: una revisione sistematica e meta-analisi di studi pubblicati di recente (2012-2016). BMC Cardiovasc Disord. 2017;17:3.