Download dit nummer Terug naar samenvatting
Steven E. ZIMMET2,3
Austin, USA
ABSTRACT
Endoveneuze laserablatie (EVLA) is een minder invasief alternatief voor aderstripping. De resultaten lijken gelijk aan of beter dan die van stripping, met betere kwaliteit van leven scores in de post-operatieve periode. Er is aangetoond dat EVLA de hemodynamische abnormaliteit kan corrigeren of aanzienlijk verbeteren bij patiënten met chronische veneuze insufficiëntie (CVI) met oppervlakkige veneuze reflux. De eerste rapporten suggereren dat endoveneuze ablatietechnieken, in tegenstelling tot chirurgische stripping, geassocieerd worden met een lage incidentie van neovascularisatie.
Er worden verschillende golflengtes gebruikt om EVLA uit te voeren. Terwijl de aanvankelijke chromofoor water of hemoglobine is, afhankelijk van de gebruikte golflengte, blijkt koolstof een secundaire maar belangrijke chromofoor te zijn die waarschijnlijk onafhankelijk van de golflengte is.
De toepassing van de principes van tumescente anesthesie op veneuze behandelingen, samen met de ontwikkeling van endoveneuze ablatietechnieken, bieden de mogelijkheid om de overgrote meerderheid van patiënten met spataderen in-office te behandelen zonder algehele anesthesie of chirurgische incisies, terwijl tegelijkertijd de resultaten worden gemaximaliseerd en recidieven tot een minimum worden teruggebracht.
INLEIDING
Sapheneuze veneuze reflux is de onderliggende primaire afwijking in de meerderheid van de gevallen van oppervlakkige veneuze insufficiëntie. Bijgevolg hebben de benaderingen van de behandeling van de saphenofemorale junctie en de saphenous truncal incompetentie het denken van flebologen gedomineerd. Trendelenburg beschreef ligatie van de saphenofemorale junctie alleen, zonder strippen van de incompetente vena saphena, in de jaren 1890. De voordelen van ligatie alleen ten opzichte van ligatie en stripping, die vandaag de dag nog steeds worden geprezen,1 zijn onder andere het behoud van de vena saphena voor mogelijk toekomstig gebruik als bypass2 en het vermijden van letsel aan de nervus saphenus.3 Ligatie alleen is minder invasief, sneller en eenvoudiger uit te voeren en wordt geassocieerd met een gemakkelijker herstel in vergelijking met aderstripping. Hoewel het waar is dat de slurf van de venus routinematig wordt “gespaard “4 , wordt het gebruik van een zieke vena saphena als conduit in verband gebracht met een verhoogd risico op falen van de graft.5 Het belangrijkste is dat er geen twijfel meer over bestaat dat ligatie alleen meestal resulteert in persisterende reflux in de slurf van de venus.6,7 Het recidief van spataderen wordt aanzienlijk verminderd7-9 en het heroperatiepercentage is 60% tot 70% lager als de vena saphena wordt gestript in vergelijking met ligatie alleen.10,11 Na ligatie alleen werd recidief of residuele communicatie met de verbinding in de lies gevonden bij 80% van de patiënten, terwijl 34% ook midden-dij perforator incompetentie had via de niet gestripte grote vena saphena (GSV).12 Zoals Neglen concludeerde, is strippen van de GSV van het bovenbeen essentieel voor het minimaliseren van recidief dat wordt veroorzaakt door herontwikkeling van incompetente communicatie met de saphenofemorale confluentie, en als gevolg van dij perforator incompetentie.13 Eenvoudig gezegd, de tekortkomingen van ligatie alleen zijn groter dan de voordelen.
Het is belangrijk op te merken dat recidief vaak voorkomt, zelfs na ligatie en stripping van de vena saphena. Hoewel inadequate chirurgie van de saphenofemorale junctie en progressie van de ziekte mechanismen zijn die sommige gevallen van recidief verklaren, is een ander belangrijk mechanisme neovascularisatie rond de junctie na veneuze chirurgie.11,14 In feite is neovascularisatie gerapporteerd als de belangrijkste oorzaak van recidief,9 waarbij neovasculaire kanalen van variabele grootte, aantal en tortuositeit in de meerderheid van de gevallen verantwoordelijk zijn voor de reflux naar terugkerende varicositeiten.15 Hoewel sommigen twijfels hebben geuit over het waarheidsgehalte van echte neovascularisatie, is er duidelijk histologisch bewijs dat neovascularisatie een oorzaak is van terugkerende spataderen.16 De eerste rapporten suggereren daarentegen dat endoveneuze ablatietechnieken geassocieerd worden met een zeer lage incidentie van neovascularisatie. 17 Het is mogelijk dat de ontwikkeling van neovascularisatie grotendeels wordt voorkomen door liesdissectie te vermijden en door veneuze drainage in normale junctionele zijrivieren te behouden.18,19
EVLA is, net als radiofrequente ablatie en schuimsclerotherapie, een minder invasief alternatief voor het strippen van de aderen. EVLA is geïndiceerd bij een ambulante patiënt met reflux van de grote, kleine of accessoire vena saphena met oppervlakkige varices en/of symptomen of complicaties die verband houden met oppervlakkige veneuze insufficiëntie. EVLA wordt routinematig uitgevoerd met verdunde plaatselijke verdoving, met of zonder aanvullende orale anxiolytica, in een kantooromgeving. De procedure neemt in het algemeen 30-60 minuten in beslag, maar de duur is afhankelijk van de lengte van het behandelde segment, de ervaring van de operateur en of er aanvullende procedures, zoals ambulante flebectomie, worden uitgevoerd. Ongeacht hoe de onderliggende ader incompetentie van de vena saphena wordt behandeld, zijn aanvullende behandelingen meestal nodig om de resterende varices te behandelen (afbeelding 1).
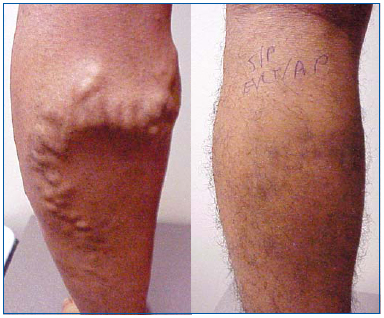
Figuur 1. Man van 26 jaar voor en 1 maand na endoveneuze laserablatie van de grote vena saphena en ambulante flebectomie van de zijtakken met varicose.
EFFICIËNTIE
Tussentijdse en kortetermijnstudies van EVLA, ongeacht de gebruikte golflengte, lijken opmerkelijk consistent, en melden meestal ablatie van refluxerende vena saphena in 90% of meer van de gevallen.18,20-23 Van EVLA van de vena saphena is aangetoond dat het de hemodynamische afwijking en klinische symptomen van chronische veneuze insufficiëntie (CVI) corrigeert of aanzienlijk verbetert bij patiënten van klinische klasse 3-6 van de CEAP (Clinical, Etiological, Anatomical, Pathophysiological) met oppervlakkige veneuze reflux.24,25 De resultaten lijken gelijk aan of beter dan die van strippen, met betere scores voor levenskwaliteit in de postoperatieve periode in vergelijking met strippen.20,25-27 Er zijn hoge tevredenheidspercentages van patiënten gemeld.18,28,29 De totale kosten (kosten van de procedure plus maatschappelijke kosten) van endoveneuze procedures zijn waarschijnlijk gelijk aan of lager dan die van chirurgie.27
Eerst recente gegevens over de behandeling van het GSV met apparaten van 810 nm en 940 nm suggereren dat mislukking van de behandeling ongewoon is bij patiënten die zijn behandeld met > 70 J/cm.30,31 Een onttrekkingssnelheid van 2 mm/sec bij 14 watt levert 70 J/cm.
MECHANISME VAN WERKING
De volgende golflengten worden momenteel gebruikt voor EVLA: 810, 940, 980, 1064, 1319, 1320, en 2068 nm. Er is gesteld dat aderwandschade zowel door direct effect als indirect via laser geïnduceerde stoom, gegenereerd door verhitting van kleine hoeveelheden bloed in de ader, wordt gemedieerd.32 Sommigen hebben gesuggereerd dat de keuze van de golflengte een grote invloed heeft op de resultaten.23
De belangrijkste chromofoor van 1320 en 2078 nm lasers, althans in het begin, is water, terwijl andere golflengtes, gebruikt voor EVLA, zich voornamelijk richten op hemoglobine. Het is duidelijk dat het noodzakelijk is de aderwand voldoende thermisch te beschadigen om een effectieve ablatie te verkrijgen. Er kan enige verwarming optreden door directe absorptie van fotonenergie (straling) door de aderwand, alsook door convectie van stoombellen en geleiding van verwarmd bloed. Het is echter onwaarschijnlijk dat deze laatste mechanismen verantwoordelijk zijn voor het grootste deel van de impact op de ader. De maximumtemperatuur van bloed is 100°C. Er werd vastgesteld dat laserbehandeling carbonisatie van de aderwand veroorzaakt.33 Carbonisatie van de laserpunt, die optreedt bij ongeveer 300°C, wordt vastgesteld na EVLA, en lijkt op te treden ongeacht de gebruikte golflengte.34 Carbonisatie van de laservezelpunt creëert een puntwarmtebron en vermindert in wezen de lichtpenetratie in weefsel tot nul.34,35 Mordon et al verklaarden “De stoom die geproduceerd wordt door absorptie van laserenergie door het bloed is een uiterst kleine fractie van de energie die nodig is om de aderwand te beschadigen en kan niet het primaire mechanisme zijn van letsel aan de ader met endoveneuze laser. De carbonisatie en het spoor binnen de aderwanden die door histologie na endoveneuze laser worden waargenomen, kunnen alleen het resultaat zijn van direct contact tussen de laservezeltip en de aderwand. “36 Dr. Rox Anderson, directeur van het Wellman Center for Photomedicine in het Massachusetts General Hospital, meldde dat koolstof een secundaire maar belangrijke chromofoor lijkt te zijn die waarschijnlijk onafhankelijk is van de golflengte (figuur 2).34 Merk op dat de vezeltip en -vorm van invloed kunnen zijn op de ontwikkeling van carbonisatie.37

Figuur 2. Verkoling van een 600 micron laservezelpunt na endoveneuze laserablatie met een laser van 1320 nm (foto met dank aan Mark Forrestal, MD, FACPh).
TUMESCENT ANESTHESIA
EVLA moet worden uitgevoerd onder plaatselijke verdoving met behulp van grote volumes van een verdunde oplossing van lidocaïne en epinefrine (gemiddeld volume van 200-400 mL 0,1% lidocaïne met 1:1.000.000 epinefrine) die is gebufferd met natriumbicarbonaat. Deze oplossing moet handmatig of met een infuuspomp onder echogeleiding worden toegediend, zodat de ader over de gehele lengte van het te behandelen segment met de verdovingsvloeistof is omgeven (figuur 3).
De voordelen van tumescente anesthesie voor endoveneuze ablatie zijn:
– anesthesie,
– scheiding van de te behandelen ader van de omringende structuren,
– thermal sink, waardoor de piektemperaturen in periveneuze weefsels worden verminderd,
– adercompressie, waardoor het effect van de behandeling op de aderwand wordt gemaximaliseerd.
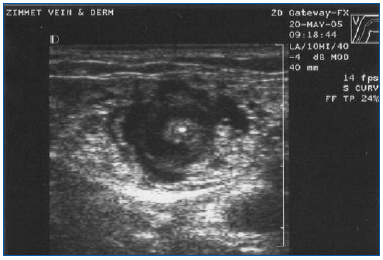
Figuur 3. Transversaal echografisch beeld van verdovingsvloeistof met tumescente anesthesie rond centraal gelegen grote vena saphena en laservezel/sheath.
Hoewel de maximale veilige dosering van lidocaïne bij gebruik van de tumescentietechniek voor veneuze procedures niet goed is bestudeerd, is een dosering van 35 mg/kg een redelijke schatting.
Met gebruikmaking van deze parameters is aangetoond dat tumescente anesthesie in het kader van liposuctie buitengewoon veilig is. Meer informatie is beschikbaar op http://www.liposuction.com/pharmacology/drug_inter act.php.
CONTRA-INDICATIES VOOR EVLA
Contra-indicaties voor de EVLA techniek worden in tabel I samengevat.

Tabel I. Contra-indicaties voor endoveneuze laser.
ADVERSE SEQUELAE
Pijn op korte termijn en ecchymosen zijn vaak waargenomen na EVLA. In een retrospectief onderzoek is gemeld dat intermitterend gepulseerde laser fiber terugtrekking aanzienlijk meer postoperatieve pijn en blauwe plekken veroorzaakt in vergelijking met een continu terugtrekprotocol.38 Door na EVLA met intermitterende modus gedurende 3 dagen een kort rekverband aan te brengen, werden de door de patiënt gerapporteerde blauwe plekken en pijn aanzienlijk verminderd. Het gebruik van een pullback in continue modus verminderde de ernst van de pijn en de bloeduitstortingen verder, zodanig dat de niveaus vergelijkbaar waren met de niveaus die werden gerapporteerd door patiënten die werden behandeld met radiofrequente ablatie (Tabellen II en III). Voorlopige rapporten suggereren dat er enige verschillen in het postoperatieve beloop kunnen zijn, afhankelijk van de golflengte die wordt gebruikt om EVLA uit te voeren.22,39 Dit is echter gebaseerd op schaarse gegevens met een follow-up op korte termijn.
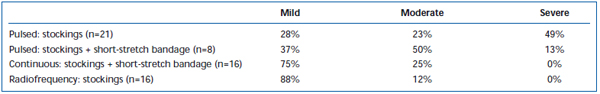
Tabel II. Door de patiënt beoordeelde postoperatieve bloeduitstortingen 3-7 dagen na gepulseerde endoveneuze laserablatie (EVLA) met klasse II kousen, gepulseerde EVLA met kousen plus kort elastisch verband, continue modus EVLA met kousen en kort elastisch verband, en radiofrequente ablatie met kousen.
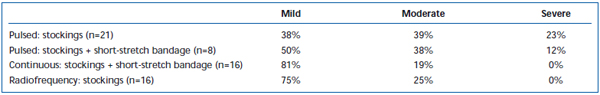
Tabel III. Door de patiënt beoordeelde postoperatieve pijn 3-7 dagen na gepulseerde endoveneuze laserablatie (EVLA) met klasse II kousen, gepulseerde EVLA met kousen plus korterekverband, continue modus EVLA met kousen en korterekverband, en radiofrequente ablatie met kousen.
PERIVENOUS THERMAL INJURY
Mean peak intravascular temperatures during EVLA (goat jugular vene, 12 watt, 1 seconde pulses, 1 seconde intervals), measured flush with the laser tip, a average 729°C, while those 4 mm distal to the tip a average 93°C.40 Het risico van bijkomend thermisch letsel hangt echter af van de perifere verwarming van het weefsel, niet van de intravasculaire temperatuur.
Collageen trekt samen bij ongeveer 50°C, terwijl necrose optreedt tussen 70°C en 100°C.41 De mate van thermisch letsel aan weefsel is sterk afhankelijk van de hoeveelheid en de duur van de hitte waaraan het weefsel wordt blootgesteld. Henriques en Moritz onderzochten de tijd-temperatuurrespons voor weefsel dat tot 70°C wordt blootgesteld.42 Zij ontdekten dat de huid temperatuurstijgingen voor zeer korte blootstellingstijden kan weerstaan, en dat de respons logaritmisch lijkt te zijn naarmate de blootstellingstijden korter worden. Een stijging van de lichaamstemperatuur tot 58°C leidt bijvoorbeeld tot celvernietiging als de blootstelling langer dan 10 seconden duurt. Weefsels zijn echter bestand tegen temperaturen tot 70°C als de blootstelling minder dan 1 seconde duurt. Li et al. meldden dat verhitting van endotheelcellen tot 48°C gedurende 10 minuten geen celdood veroorzaakte.43 Zij stelden ook vast dat osteoblasten, na blootstelling gedurende 10 minuten of minder aan 45°C, voorbijgaande en omkeerbare veranderingen ondergingen. Een andere studie vond omkeerbare weefselschade aan de achterste ledematen van muizen na onderdompeling in een waterbad van 44°C.44
Een recente studie mat de piektemperatuur aan de buitenste aderwand tijdens EVLA in een levende varkensoorader en in blootgestelde aderen van de achterste ledematen.45 De EVLA-instellingen varieerden van 8 watt (pulsduur van 1-2 seconden), 10 watt (pulsduur van 1-1,5 seconde), 12 watt (pulsduur van 0,5-1,5 seconde) tot 15 watt (pulsduur van 0,5-1,0 seconde), met en zonder tumescente anesthesie. De resultaten tonen aan dat de piektemperaturen varieerden van 34,6°C tot 49,1°C als functie van de geleverde joules, met lagere piektemperaturen verkregen wanneer tumescente vloeistof aanwezig was (figuur 4).
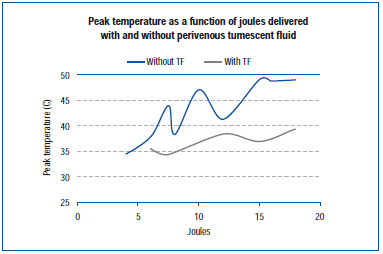
Figuur 4. Aangepast uit Zimmet SE, Min RJ. Temperatuurveranderingen in periveneus weefsel tijdens endoveneuze laserbehandeling in een varkensmodel. J Vasc Interv Radiol. 2003;14:911-915 (ref 45).
Piektemperatuur gemeten tijdens EVLA (63 patiënten, 980 nm, 15 watt, 1,5 sec pulsen) aan de buitenste aderwand bij mensen, 3 cm onder de saphenofemorale junctie, was 40,9°C en 49,8°C met en zonder tumescente vloeistof, respectievelijk.46 Vergelijkbare resultaten werden gerapporteerd in een ander onderzoek bij mensen tijdens EVLA (12 patiënten, 810 nm, 12 W, pulsen van 1 seconde, intervallen van 1 seconde, opzwellende techniek), met piektemperaturen van 43,3°C, 42,0°C en 36,0°C op respectievelijk 3 mm, 5 mm en 10 mm van de GSV. 47
Er lijkt een zeer snelle daling van de temperatuur over korte afstanden te zijn tijdens EVLA. Dit is waarschijnlijk in tegenstelling tot radiofrequente energie waarbij microgolfverwarming optreedt rond het raakvlak tussen weefsel en elektrode. De gegevens van dieren en mensen suggereren dat het onwaarschijnlijk is dat de piektemperaturen die tijdens endoveneuze laser worden opgewekt, in de meeste situaties permanente schade aan het periveneuze weefsel zullen toebrengen. De gegenereerde piektemperatuur wordt verlaagd bij gebruik van periveneuze tumescentievloeistof. Deze bevindingen lijken de zeer lage incidentie te verklaren van zenuwschade en huidverbranding na EVLA. Eén studie, waarbij een 1064 nm Nd: YAG laser werd gebruikt, meldde een zeer hoge incidentie van paresthesie bij 36,5% en huidverbranding bij 4,8%.48 Hierbij moet worden opgemerkt dat de hoeveelheid toegediende energie ongeveer drie keer hoger was dan wat gewoonlijk wordt gebruikt en dat de behandeling werd uitgevoerd zonder tumescente anesthesie. Ondanks de lage periveneuze temperaturen die met EVLA werden gemeld, is het belangrijk op te merken dat speciale voorzichtigheid is geboden wanneer endoveneuze interventie wordt overwogen in bepaalde gevallen zoals ischiaszenuwvarices.49,50
MAJORE COMPLICATIES
Grote complicaties na EVLA zijn zelden gemeld. De percentages diepe veneuze trombose (DVT), gepoold uit meerdere series, zijn veel lager dan 1%.17,18,20,28 Eén groep meldde een incidentie van trombusuitbreiding in de femorale vene van 7,7%.51 In die studie werd EVLA echter uitgevoerd onder algehele of spinale anesthesie. Het feit dat patiënten niet in staat waren om direct na de operatie te lopen, kan hebben bijgedragen aan de hoge incidentie van trombusuitbreiding. Er is één melding van een arterioveneuze fistel die ontstond na EVLA van de korte vena saphena (SSV).52 Eén patiënt ontwikkelde een septische tromboflebitis na EVLA gecombineerd met open ligatie van perforatoren en steekflebectomie.53 Dit loste op met antibiotische behandeling en debridement.
ALTERNATIEVE BEHANDELINGEN
EVLA en radiofrequente ablatie (RFA)54,55 lijken beide effectieve behandelingen te zijn voor incompetentie van de vena saphena. Voordelen van EVLA ten opzichte van RFA zijn kortere proceduretijden en lagere kosten per behandeling. De gerapporteerde occlusiepercentages van EVLA zijn over het algemeen iets hoger dan die van RFA.56 Nadelen van EVLA kunnen zijn meer blauwe plekken en ongemak in de vroege postoperatieve periode, hoewel dit afhankelijk kan zijn van de techniek. Beide technieken worden nog steeds verfijnd, waardoor de resultaten zullen verbeteren. Beide procedures, wanneer uitgevoerd met behulp van tumescente anesthesie, worden geassocieerd met lage complicatiepercentages.
Een andere opkomende behandeling voor reflux van de venus is het gebruik van sclerosanten met schuim die onder ultrasone controle worden toegediend. Een gas, zoals lucht of CO2, kan worden gemengd met vloeibaar detergent sclerosantia om schuim te creëren, waarvan wordt geschat dat het ongeveer vier keer krachtiger is dan de vloeibare vorm van hetzelfde middel. De eerste resultaten suggereren dat dit een waardevolle methode kan zijn, aangezien deze snel en goedkoop kan worden uitgevoerd met gerapporteerde succespercentages op korte en middellange termijn van ongeveer 75% tot 90%. Er zijn veel variabelen met betrekking tot foam (bv. soort en hoeveelheid gas, techniek die wordt gebruikt om foam te maken, concentratie en soort sclerosant dat wordt gebruikt, volume dat wordt geïnjecteerd, enz). Er kan een hoger risico zijn op diep-veneuze trombose na foam sclerotherapie in vergelijking met standaard sclerotherapie. Een goede techniek is belangrijk om het risico op deze complicatie tot een minimum te beperken. Andere gerapporteerde bijwerkingen na foam sclerotherapie zijn visuele en neurologische voorvallen. Er is een gepubliceerd verslag van een beroerte na foam sclerotherapie (20 ml polidocanol schuim) bij een patiënt met een 1,8 cm patent foramen ovale.57 Verdere ervaring met en onderzoek naar deze modaliteit zal de risico’s en de werkzaamheid op lange termijn beter afbakenen.
CONCLUSIE
De huidige aanvaarde principes voor de behandeling van spataderen dienen om de resultaten te maximaliseren vanuit hemodynamisch en patiëntenstandpunt, terwijl het risico op herhaling wordt geminimaliseerd. De juiste behandeling van spataderen begint met een nauwkeurige beoordeling van de onderliggende veneuze pathologie en identificatie van de bronnen van veneuze hypertensie. De behandeling heeft tot doel de incompetente verbindingen tussen het diepe en het oppervlakkige systeem te elimineren en de veneuze incompetentiewegen en incompetente spataderen uit te wissen. Het is duidelijk dat recidief vermindert als het incompetente segment van de vena saphena wordt geablateerd.
Endoveneuze laserablatie is een minder invasief alternatief voor veneuze stripping. De resultaten lijken gelijk aan of beter dan die van strippen, met betere kwaliteit van leven scores in de post-operatieve periode. Van EVLA is aangetoond dat het de hemodynamische abnormaliteit corrigeert of aanzienlijk verbetert bij patiënten met chronische veneuze insufficiëntie met oppervlakkige veneuze reflux. De eerste rapporten suggereren dat endoveneuze ablatietechnieken, in tegenstelling tot chirurgische stripping, geassocieerd zijn met een lage incidentie van neovascularisatie.
De toepassing van de principes van tumescente anesthesie op veneuze behandelingen, samen met de ontwikkeling van endoveneuze ablatietechnieken, bieden de mogelijkheid om de overgrote meerderheid van patiënten met oppervlakkige veneuze insufficiëntie in-office te behandelen zonder algehele anesthesie of chirurgische incisies, terwijl tegelijkertijd de resultaten worden gemaximaliseerd en de recidieven tot een minimum worden beperkt.
Dit artikel werd ingediend op 29 juli 2006.

2. Large J. Surgical treatment of saphenous varices, with preservation of the main great saphenous trunk. J Vasc Surg. 1985;2:886-891.
3. Holme JB, Holme K, Sorensen LS. The anatomic relationship between the long saphenous vein and the saphenous nerve. Relevantie voor radicale spataderchirurgie. Acta Chir Scand. 1988;154:631-633.
4. Rutherford RB, Sawyer JD, Jones DN. The fate of residual saphenous vein after partial removal or ligation. J Vasc Surg. 1990;12:422-426.
5. Panetta TF, Marin ML, Veith FJ, et al. Unsuspected preexisting saphenous vein disease: an unrecognized cause of vein bypass failure. J Vasc Surg. 1992;15:102- 110.
6. McMullin GM, Coleridge-Smith PD, Scurr JH. Objective assessment of ligation without stripping the long saphenous vein. Br J Surg. 1991;78:1139-1142.
7. Sarin S, Scurr JH, Coleridge Smith PD. Assessment of stripping the long saphenous vein in the treatment of primary varicose veins. Br J Surg. 1992;79:889-893.
8. Munn SR, Morton JB, Macbeth WA, McLeish AR. To strip or not to strip the long saphenous vein? Een varicose ader proef. Br J Surg. 1981;68:426-481.
9. Jones L, Braithwaite BD, Selwyn D, Cooke S, Earnshaw JJ. Neovascularisation is the principal cause of varicose vein recurring: results of a randomised trial of stripping the long saphenous vein. Eur J Vasc Endovasc Surg. 1996;12:442-445.
10. Dwerryhouse S, Davies B, Harradine K, Earnshaw JJ. Stripping the long saphenous vein reduces the rate of reoperation for recurrent varicose veins: five-year results of a randomized trial. J Vasc Surg. 1999;29:589-592.
11. Winterborn RJ, Foy C, Earnshaw JJ. Causes of varicose vein recurrence: late results of a randomized controlled trial of stripping the long saphenous vein. J Vasc Surg. 2004;40:634-639.
12. Corbett CR, Runcie JJ, Lea TM, Jamieson CW. Reasons to strip the long saphenous vein. Flebologie. 1988;41:766-769.
13. Neglen P. Treatment of varicosities of saphenous origin: comparison of ligation, selective excision, and sclerotherapy. In: Bergan JJ, Goldman MP eds. Spataderen en teleangiëctasieën: Diagnosis and Treatment. St. Louis, Mo, USA: Quality Medical Publishing; 1993:148-165.
14. Kostas T, Ioannou CV, Touloupakis E, et al. Recurrent varicose veins after surgery: a new appraisal of a common and complex problem in vascular surgery. Eur J Vasc Endovasc Surg. 2004;27:275-282.
15. Van Rij AM, Jones GT, Hill GB, Jiang P. Neovascularization and recurrent varicose veins: more histologic and ultrasound evidence. J Vasc Surg. 2004;40:296-302.
16. Nyamekye I, Shephard NA, Davies B, et al. Clinicopathological evidence that neovascularization is a cause of recurrent varicose veins. Eur J Vasc Endovasc Surg. 1998;15: 412-415.
17. Ravi R, Rodriguez-Lopez JA, Trayler EA, et al. Endovenous ablation of incompetent saphenous veins: a large single-center experience. J Endovasc Ther. 2006;13:244- 248.
18. Min RJ, Khilnani N, Zimmet SE. Endovenous laser treatment of saphenous vein reflux: long-term results. J Vasc Interv Radiol. 2003;14:991-996.
19. Bergan JJ, Rattner Z. Endoveneuze therapie-2005. Acta Chir Bel. 2005;105:12- 15.
20. Agus GB, Mancini S, Magi G. De eerste 1000 gevallen van de Italiaanse endoveneuze-laser Werkgroep (IEWG). Rationale, and long-term outcomes for the 1999-2003 period. Int Angiol. 2006;25:209-215.
21. Kalra M, Gloviczki P. Fifteen years ago laser was supposed to open arteries, now it is supposed to close ains: what is the reality behind the tool? Perspect Vasc Surg Endovasc Ther. 2006;18:3-8 (discussie 9- 10).
22. Kabnick LS. Outcome of different endovenous laser wavelengths for great saphenous vein ablation. J Vasc Surg. 2006;43: 88-93.
23. Goldman MP, Maritess M, Rao J. Intravasculaire 1320-nm laserlasersluiting van de grote vena saphena: een 6- tot 12-maanden follow-upstudie. Dermatol Surg. 2004;30: 1380-1385.
24. Marston WA, Owens LV, Davies S, et al. Endovenous saphenous ablation corrects the hemodynamic abnormality in patients with CEAP clinical class 3-6 CVI due to superficial reflux. Vasc Endovascular Surg. 2006;40:125-130.
25. De Medeiros CA, Luccas GC. Comparison of endovenous treatment with an 810 nm laser versus conventional stripping of the great saphenous vein in patients with primary varicose veins. Dermatol Surg. 2005;31:1685-1694.
26. Mekako AI, Hatfield J, Bryce J, et al. A nonrandomised controlled trial of endovenous laser therapy and surgery in the treatment of spaticose veins. Ann Vasc Surg. 2006;Jun 27:.
27. Vuylsteke M, Van den Bussche D, Audenaert EA, Lissens P. Endoveneuze laser obliteratie voor de behandeling van primaire spataderen. Flebologie. 2006;21:80-87. 28. Perkowski P, Ravi R, Gowda RC, et al. Endovenous laser ablation of the saphenous vein for treatment of venous insufficiency and varicose veins: early results from a large single-center experience. J Endovasc Ther. 2004;11:132-138.
29. Sharif MA, Soong CV, Lau LL, et al. Endovenous laser treatment for long saphenous vein incompetence. Br J Surg. 2006;93:831-835.
30. Proebstle TM, Krummenauer F, Gul D, Knop J. Nonocclusion and early reopening of the great saphenous vein after endovenous laser treatment is fluence dependent. Dermatol Surg. 2004;30:174-178.
31. Timperman PE, Sichlau M, Ryu RK. Greater energy delivery improves treatment success of endovenous laser treatment of incompetent saphenous veins. J Vasc Interv Radiol. 2004;15:1061-1063.
32. Proebstle TM, Sandhofer M, Kargl A, et al. Thermal damage of the inner vein wall during endovenous laser treatment: key role of energy absorption by intravascular blood. Dermatol Surg. 2002;28:596-600.
33. Schmedt CG, Sroka R, Steckmeier S, et al. Onderzoek naar de effecten van radiofrequentie en laser (980 nm) na endoluminale behandeling van aderinsufficiëntie van de vena saphena in een ex-vivomodel. Eur J Vasc Endovasc Surg. 2006;Jun 14;.
34. Anderson RR. Endoveneuze laser: werkingsmechanisme. Paper gepresenteerd op de jaarlijkse bijeenkomst van de American Academy of Dermatology; 3-7 maart 2006; San Francisco, California, USA.
35. Izzo F. Other thermal ablation techniques: microwave and interstitial laser ablation of liver tumors. Annals of Surgical Oncology. 2003;10:491-497.
36. Mordon SR, Wassmer B and Zemmouri J. Mathematical modeling of endovenous laser treatment (ELT). BioMedical Engineering OnLine. 2006;5:26. Beschikbaar op: http://www.biomedical-engineeringonline. com/content/5/1/26. Accessed July 19, 2006.
37. De-Fei Hong, Shu-You Peng, Song-Ying Li, Li-Min Tong. Experimentele studie van diodelaser geïnduceerde thermocoagulatie op leverweefsel met scanner fiber tip. World J Gastroenterol. 2003;9:2350-2352.
38. Zimmet SE. Pain, bruising and short-term efficacy after endovenous laser treatment of the greater saphenous vein: the effect of operative technique and postoperative care. Paper gepresenteerd op het 16e jaarlijkse congres van het American College of Phlebology; 7-10 november 2002; Fort Lauderdale, Florida, USA.
39. Proebstle TM, Moehler T, Gul D, Herdemann S. Endoveneuze behandeling van de grote vena saphena met een 1320 nm Nd:YAG laser veroorzaakt minder neveneffecten dan het gebruik van een 940 nm diodelaser. Dermatol Surg. 2005;31:1678-1683.
40. Weiss RA. Comparison of endovenous radiofrequency versus 810 nm diode laser occlusion of large veins in an animal model. Dermatol Surg. 2002;28:56-61.
41. Biesman BS, Khan J. Laser incisional surgery. Clinics in Plastic Surg. 2000;27:213- 220.
42. Moritz AR, Henriques Jr EC. Studies of thermal injury II: the relative importance of time and surface temperature in the causation of cutaneous bums. Am J Pathol. 1947;23:695-720.
43. Li S, Chien S, Branemark P. Heat shockinduced necrosis and apoptosis in osteoblasts. J Orthop Res. 1999;17:891-899.
44. Jansen W, Haveman J. Histopathological changes in the skin and subcutaneous tissues of mouse legs after treatment with hyperthermia. Path Res Pract. 1990;186: 247-253.
45. Zimmet SE, Min RJ. Temperature changes in perivenous tissue during endovenous laser treatment in a swine model. J Vasc Interv Radiol. 2003;14:911-915.
46. Lahl W. Thermometric investigations of perivenous temperature during endovenous laser therapy of varicose veins. Paper gepresenteerd op het 15e Wereldcongres van de Union Internationale de Phlébologie; 2-7 oktober 2005; Rio de Janeiro, Brazilië.
47. Beale RJ, Mavor AID, Gough MJ. Heat dissipation during endovenous laser treatment of varicose veins-is there a risk of nerve injury? Flebologie. 2006;21:32-35.
48. Chang CJ, Chua JJ. Endoveneuze laser fotocoagulatie (EVLP) voor spataderen. Lasers Surg Med. 2002;31:257-262.
49. Ricci S, Georgiev M, Jawien A, Zamboni P. nervus ischiadicus varices. Eur J Vasc Endovasc Surg. 2005;29:83-87.
50 Ricci S. Ultrasound observation of the sciatic nerve and its branches at the popliteal fossa: always visible, never seen. Eur J Vasc Endovasc Surg. 2005;30:659-663. 51 Mozes G, Kalra M, Carmo M, Swenson L, Gloviczki P. Extension of saphenous thrombus into the femoral vein: a potential complication of new endovenous ablation techniques. J Vasc Surg. 2005;41:130-135.
52 Timperman, PE. Arterioveneuze fistel na endoveneuze laserbehandeling van de korte vena saphena. J Vasc Interv Radiol. 2004;15:625-627.
53 Dunst KM, Huemer GM, Wayand W, Shamiyeh A. Diffuse phlegmonous phlebitis after endovenous laser treatment of the greater saphenous vein. J Vasc Surg. 2006;43:1056-1058.
54 Lurie F, Creton D, Eklof B, et al. Prospective randomized study of endovenous radiofrequency obliteration (closure procedure) versus ligation and stripping in a selected patient population (EVOLVeS Study). J Vasc Surg. 2003;38:207-214.
55 Merchant RF, DePalma RG, Kabnick LS. Endovascular obliteration of saphenous reflux: a multicenter study. J Vasc Surg. 2002;35:1190-1196.
56 Puggioni A, Kalra M, Carmo M, Mozes G, Gloviczki P. Endovenous laser therapy and radiofrequency ablation of the great saphenous vein: analysis of early efficacy and complications. J Vasc Surg. 2005;42; 488-493.
57 Forlee MV, Grouden M, Moore DJ, Shanik G. Stroke after varicose vein foam injection sclerotherapy. J Vasc Surg. 2006;43: 162-164.