US Pharm. 2017;42(6)(Generic Drugs suppl):38-42.
ABSTRACT: Os inibidores da bomba de prótons (PPIs) são uma classe de agentes anti-secretórios usados para tratar várias condições gastrointestinais, tais como doença do refluxo gastroesofágico, desordens relacionadas com Helicobacter pylori- e úlceras gástricas e duodenais. Embora estes agentes sejam supressores de ácido eficazes, o uso de PPIs é frequentemente debatido com base em relatos de novos potenciais eventos adversos. O uso excessivo e as interações medicamentosas são problemas associados aos PPIs. Além disso, como vários PPIs estão disponíveis no mercado de balcão, o uso inadequado desses agentes é uma preocupação significativa. Os farmacêuticos em todos os ambientes podem ter um impacto profundo no uso inadequado de PPIs, assegurando o início e a continuação apropriada da terapia, dosagem e duração do tratamento.
Inibidores de bomba de prótons (PPIs) são uma classe de medicamentos comumente usados para o tratamento de vários distúrbios gastrointestinais (GI), incluindo doença do refluxo gastroesofágico (DRGE), distúrbios relacionados com Helicobacter pylori- e úlceras gástricas e duodenais. Embora estes agentes anti-secretórios sejam o tratamento preferido para inúmeras patologias, a classe é flagelada pela utilização excessiva e relatos de efeitos adversos potencialmente graves e interacções medicamentosas.1 Além disso, o tratamento das patologias tratadas com PPIs é complicado pela disponibilidade OTC de vários destes agentes. Este artigo visa destacar o uso apropriado e fornecer uma descrição baseada em evidências de vários inconvenientes novos ou muito debatidos desses agentes.
Disponibilidade de PPIs
Seis PPIs únicos, cinco dos quais estão disponíveis genericamente, podem ser obtidos por prescrição médica (TABELA 1).2-7 Doses baixas de omeprazol, lansoprazol e uma versão de marca de magnésio esomeprazol estão disponíveis OTC. O omeprazol também é usado em um produto coformulado com bicarbonato de sódio. Este artigo irá focar principalmente nos PPIs dosados oralmente disponíveis.
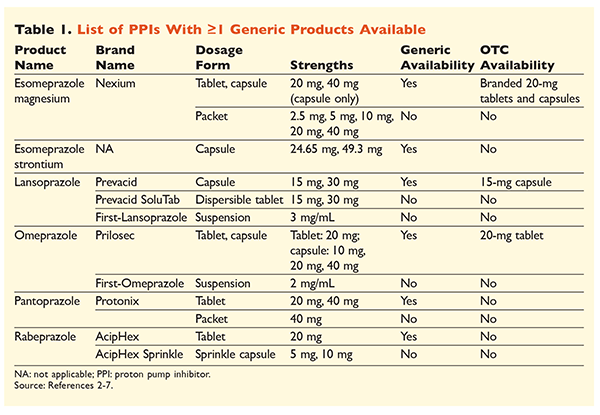
Esomeprazol estrôncio foi aprovado pelo FDA com base em sua bioequivalência ao esomeprazol magnésio.3 Embora a rotulagem do produto para estes dois agentes seja altamente similar, existem três diferenças notáveis. Primeiro, o esomeprazol estrôncio está disponível em cápsulas de 24,65 mg e 49,3 mg, que são equivalentes ao esomeprazol magnésio 20 mg e 40 mg, respectivamente. Segundo, o estrôncio do esomeprazol não é aprovado pelo FDA para uso em pacientes pediátricos, enquanto o magnésio do esomeprazol é aprovado para uso em pacientes com 1 mês de idade ou mais. Finalmente, o uso do esomeprazol estrôncio deve ser evitado em pacientes com insuficiência renal grave, pois não foi estudado nesta população. Nenhum ajuste de dosagem é recomendado para o esomeprazol magnésio.3 Para os propósitos deste artigo, o termo esomeprazol será usado para descrever o esomeprazol magnésio.
Administração
Todos os PPIs disponíveis genericamente, incluindo cápsulas e comprimidos, devem ser engolidos inteiros sem serem divididos, esmagados ou mastigados.2-7 As cápsulas de omeprazol, lansoprazol e esomeprazol podem ser abertas e o conteúdo polvilhado em molho de maçã para pacientes incapazes de engolir formas de dosagem oral. Adicionalmente, as cápsulas de lansoprazol podem ser polvilhadas em 2 oz. de sumo de maçã, tomate ou laranja. Qualquer mistura contendo o conteúdo das cápsulas abertas deve ser ingerida imediatamente e não deve ser armazenada para uso futuro.2,4,5
Lansoprazol, omeprazol e esomeprazol devem ser administrados antes das refeições, mas as recomendações específicas sobre os tempos de administração variam. O omeprazol deve ser administrado 30 a 60 minutos antes das refeições e o esomeprazol pelo menos 60 minutos antes das refeições; não é especificado um período de tempo para o lansoprazol.2,4,5 O pantoprazol pode ser administrado com ou sem alimentos.6 O rabeprazol deve ser tomado após uma refeição para úlceras duodenais e com uma refeição para a erradicação do H pylori; para todas as outras indicações, o rabeprazol pode ser tomado com ou sem alimentos.7
Dose e Duração da Terapia
Dada a reputação dos PPIs de serem muito eficazes e geralmente seguros, a sobreutilização significativa dos PPIs é uma grande preocupação.1 Não só os PPIs são frequentemente administrados para indicações sem evidências que apóiem o seu uso, mas estes medicamentos também são frequentemente prescritos em doses mais altas do que o necessário para durações de tratamento que se estendem além dos prazos recomendados.8,9 Cada dosagem aprovada de PPI e duração recomendada da terapia são dadas nas TABELAS 2 e 3. As recomendações de tratamento que diferem daquelas aprovadas pelo FDA, bem como as notáveis pérolas clínicas relacionadas ao início da PPI, dosagem e duração do tratamento, são descritas abaixo.
>
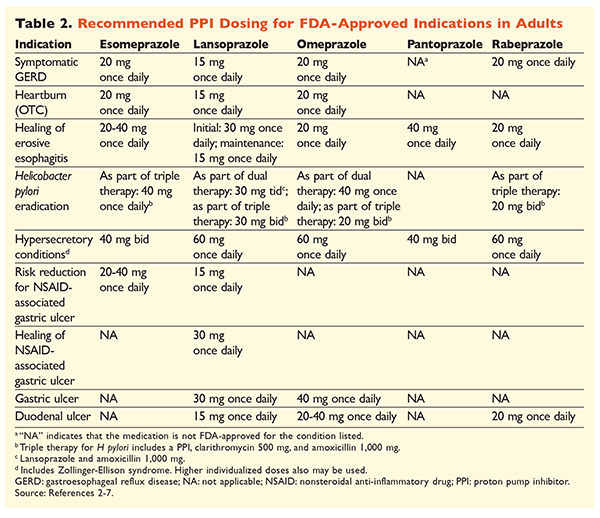
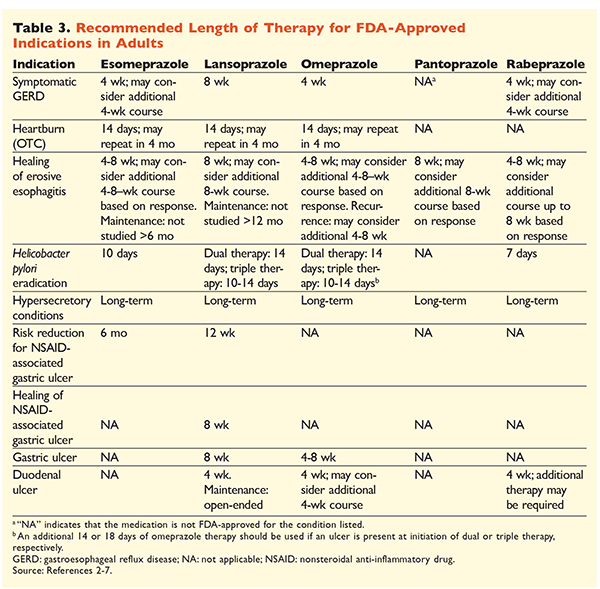
GERD: Em pacientes com DRGE, todas as PPIs são consideradas igualmente eficazes, sendo recomendado um tratamento de 8 semanas com qualquer agente disponível.10 Pacientes com sintomas refratários ao tratamento após 2 a 3 meses podem necessitar de uma terapia de manutenção a longo prazo com doses duplas por dia. Entretanto, a dose efetiva mais baixa deve ser usada, e uma PPI diferente deve ser considerada se o paciente não responder à terapia.10 Alternativamente, pode ser considerada a terapia com a PPI necessária ou uma abordagem de step-down para um antagonista do receptor de histamina2 (H2RA).10 O tratamento com uma PPI OTC deve ser limitado a 14 dias, com um novo tratamento não mais freqüente do que a cada 4 meses.11
H úlceras associadas à piloroaspiração: Dependendo do PPI utilizado, os regimes aprovados pelo FDA para a erradicação da pilori H incluem terapia dupla com amoxicilina ou claritromicina e terapia tripla com ambos os agentes durante 7 a 14 dias.2-5,7 Os regimes de tratamento específicos apoiados por diretrizes variam em comparação com os aprovados pelo FDA, mas a duração recomendada da terapia é semelhante, com todos os regimes tendo um período de tempo de dosagem de 10 a 14 dias.12 Após a erradicação do H pylori, a manutenção da terapia com PPI não é necessária.13 Uma discussão mais detalhada dos regimes específicos está além do escopo deste artigo.
Profilaxia e Tratamento de Úlceras Induzidas por AINE: Após o desenvolvimento de um medicamento anti-inflamatório não esteróide (AINE)-associado à úlcera, a necessidade de terapia com AINE deve ser reavaliada. Se a terapia continuada com AINSID for considerada apropriada, os pacientes devem ser mantidos em terapia seletiva com ciclooxigenase-2 na dose efetiva mais baixa possível pela menor duração possível em combinação com um PPI.13
Para a profilaxia, o início de um PPI é recomendado apenas em pacientes com risco moderado ou alto de toxicidade GI relacionada com AINSID. Fatores de risco incluem idade >65 anos, terapia com altas doses de AINE, história prévia de úlcera não complicada e uso simultâneo de aspirina (incluindo baixas doses), corticosteróides ou anticoagulantes. Pacientes considerados de risco moderado para toxicidade por AINE incluem aqueles com um ou dois desses fatores de risco, enquanto pacientes de alto risco têm mais de dois fatores de risco ou histórico de úlcera péptica previamente complicada, especialmente se recente.14 É razoável continuar a terapia com PPI enquanto o paciente de risco moderado ou alto permanecer em terapia com AINE.13
Ulcera idiopática: Úlceras sem causa claramente identificável são passíveis de recorrência em pacientes que não são tratados com terapia supressora de ácido. As diretrizes não recomendam claramente o tempo que os pacientes devem ser tratados com terapia de manutenção, mas sugerem que a terapia com PPI em andamento reduz o risco de formação de úlceras recorrentes.13
Segurança
PPIs são geralmente consideradas como uma classe bem tolerada de medicamentos.1 No entanto, várias preocupações com a segurança têm atormentado sua reputação há muito tempo, incluindo um risco aumentado de diarréia associada ao Clostridium difficile, pneumonia adquirida na comunidade e fraturas ósseas.15,16 Mais recentemente, preocupações com demência e doença renal crônica têm sido levantadas, e debates sobre hipomagnesemia e uma interação teórica entre droga e clopidogrel têm continuado.
Demência: Dois estudos recentes têm sugerido o potencial para um aumento do risco de demência com uso prolongado de PPI em idosos.17,18 Um mecanismo proposto por trás desta descoberta é que os PPIs promovem o desenvolvimento de placas beta-amilóides, uma proposta fisiopatológica da doença de Alzheimer.15 Entretanto, as limitações do estudo não suportam uma relação causal conclusiva entre o uso de PPI e um aumento da incidência de demência.19
Complicações Renais: Embora as PPIs tenham sido amplamente reconhecidas como uma causa comum de nefrite intersticial aguda, dados mais recentes também implicam no desenvolvimento de outras complicações renais.15,20 Três estudos recentes sugeriram que as PPIs podem ser responsáveis pelo aumento do risco de doença renal crônica e pela progressão até o estágio final da doença renal.20-22 Entretanto, esses estudos observacionais devem ser interpretados com cautela, pois a causalidade não pode ser confirmada.23
Hipomagnesemia: Em 2011, o FDA emitiu um alerta de que o uso prolongado de PPIs por períodos superiores a 1 ano pode resultar em hipomagnesemia.24 Desde então, vários estudos de grande porte têm apoiado este achado.25-29 A relação entre PPIs e hipomagnesemia não é definitiva, no entanto, e é complicada por fatores de risco externos.30-32 Atualmente, a hipomagnesemia induzida por PPI clinicamente significativa é vista como rara e ocorre mais comumente com uso diurético concomitante.31,32 A monitoração é recomendada apenas em pacientes com fatores de risco adicionais.32
Interação com Clopidogrel: Clopidogrel tem um papel importante na redução do risco cardiovascular, mas está associado a sangramentos gastrointestinais, especialmente em pacientes com risco aumentado. A proteção dos GI com PPIs é freqüentemente implementada em pacientes com maior probabilidade de sangramento GI, incluindo aqueles com sangramento GI superior prévio; idade avançada; uso simultâneo de anticoagulantes, corticosteróides ou AINEs (incluindo aspirina); e/ou infecção por H pylori.33
PPIs são considerados inibidores da enzima CYP2C19, o caminho primário através do qual o clopidogrel é ativado.33 Essa interação pode teoricamente diminuir os efeitos antiplaquetários do clopidogrel e aumentar o risco de resultados cardiovasculares adversos.33 Com base em resultados inconsistentes tanto de estudos farmacocinéticos quanto de estudos de desfechos, entretanto, a significância clínica dessa interação é incerta.34
Outras, há uma falta de consistência nas evidências sobre o verdadeiro impacto de PPIs individuais nos efeitos do clopidogrel.33 As últimas recomendações da FDA sugerem que o pantoprazol é uma escolha mais segura que outros PPIs, enquanto o omeprazol é considerado o mais arriscado.35 Os dados atuais continuam a apoiar esta conclusão, mas estudos adicionais são necessários para confirmar se existe uma diferença entre as PPIs.36
É importante pesar os benefícios e riscos da terapia antiplaquetária sozinha ou em combinação com uma PPI quando uma decisão sobre a adição de terapia protetora da IG está sendo tomada. Em pacientes com alto risco de complicações GI, os efeitos benéficos da terapia PPI podem ser maiores do que a diminuição da eficácia da terapia antiplaquetária, o que foi demonstrado de forma inconsistente. Para pacientes com menor risco de complicações GI, uma H2RA pode ser uma opção de tratamento razoável, embora esta classe tenha se mostrado menos eficaz que as PPIs para esta indicação.33
Conclusão
Farmacêuticos em todos os ambientes podem ter um impacto profundo no uso inadequado de PPI, assegurando o início e a continuação adequada da terapia, dosagem e duração do tratamento. Como dados conflitantes continuam a surgir em relação aos perfis de segurança desses medicamentos, o uso de PPIs a longo prazo torna-se mais complicado. Ao assegurar que a dose mais baixa apropriada é usada pela menor duração necessária, os farmacêuticos podem ajudar a prevenir a exposição desnecessária dos pacientes a danos potenciais.
1. Heidelbaugh JJ, Kim AH, Chang R, Walker PC. Sobreutilização dos inibidores da bomba de prótons: o que o clínico precisa saber. Terap Adv Gastroenterol. 2012;5:219-232.
2. Inserção da embalagem de Nexium (esomeprazol de magnésio). Wilmington, DE: AstraZeneca Pharmaceuticals LP; Dezembro de 2016.
3. Inserção da embalagem do esomeprazol estrôncio. Glasgow, KY: Amneal Pharmaceuticals; Dezembro 2014.
4. bula do Prevacid (lansoprazol). Deerfield, IL: Takeda Pharmaceuticals America, Inc.; Outubro 2016.
5. Pacote de produtos Prilosec (omeprazol). Wilmington, DE: AstraZeneca Pharmaceuticals LP; Dezembro 2016.
6. bula de Protonix (pantoprazol). Philadelphia, PA: Wyeth Pharmaceuticals Inc. (Wyeth Pharmaceuticals Inc.) Outubro 2016.
7. bula de AcipHex (rabeprazol). Woodcliff Lake, NJ: Eisai Inc.; Abril 2016.
8. Chia CT, Lim WP, Vu CK. Uso inapropriado de inibidores de bomba de prótons em um ambiente local. Singapore Med J. 2014;55:363-366.
9. Kelly OB, Dillane C, Patchett SE, et al. The inappropriate prescription of oral proton pump inhibitors in the hospital setting: a prospective cross-sectional study. Dig Dis Sci. 2015;60:2280-2286.
10. Katz PO, Gerson LB, Vela MF. Guidelines for the diagnosis and management of gastroesophageal reflux disease. Am J Gastroenterol. 2013;108:308-328.
11. FDA Drug Safety Communication: possible increased risk of fractures of the hip, wrist, and spine with the use of proton pump inhibitors. www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPatientsandProviders/ucm213206.htm. Acesso em 17 de fevereiro de 2017.
12. Chey WD, Leontiadis GI, Howden CW, Moss SF. Diretriz clínica do ACG: tratamento da infecção por Helicobacter pylori. Am J Gastroenterol. 2017;112:212-239.
13. Laine L, Jensen DM. Tratamento de pacientes com hemorragia ulcerosa. Am J Gastroenterol. 2012;107:345-360.
14. Lanza FL, Chan FK, Quigley EM. Guidelines for prevention of NSAID-related ulcer complications. Am J Gastroenterol. 2009;104:728-738.
15. Eusebi LH, Rabitti S, Artesiani ML, et al. Proton pump inhibitors: risks of long-term use. J Gastroenterol Hepatol. 2017; Jan 16 .
16. Abramowitz J, Thakkar P, Isa A, et al. Adverse event reporting for proton pump inhibitor therapy: an overview of systematic reviews. Otolaryngol Head Neck Surg. 2016;155:547-554.
17. Haenisch B, von Holt K, Wiese B, et al. Risco de demência em pacientes idosos com o uso de inibidores da bomba de protões. Eur Arch Psychiatry Clin Neurosci. 2015;265:419-428.
18. Gomm W, von Holt K, Thomé F, et al. Association of proton pump inhibitors with risk of dementia: a pharmacoepidemiological claims data analysis. JAMA Neurol. 2016;73:410-416.
19. Kuller LH. Os inibidores da bomba de protões aumentam o risco de demência? JAMA Neurol. 2016;73:379-381.
20. Arora P, Gupta A, Golzy M, et al. Os inibidores da bomba de prótons estão associados com o aumento do risco de desenvolvimento de doença renal crônica. BMC Nephrol. 2016;17:112.
21. Xie Y, Bowe B, Li T, et al. Inibidores da bomba de prótons e risco de CKD incidente e progressão para ESRD. J Am Soc Nephrol. 2016;27:3153-3163.
22. Lazarus B, Chen Y, Wilson FP, et al. Uso de inibidor de bomba de prótons e o risco de doença renal crônica. JAMA Intern Med. 2016;176:238-246.
23. Kia L, Kahrilas PJ. Terapia: riscos associados ao uso de PPI crônico – sinal ou ruído? Nat Rev Gastroenterol Hepatol. 2016;13(5):253-254.
24. Comunicação da FDA sobre segurança de medicamentos: baixos níveis de magnésio podem ser associados ao uso a longo prazo de drogas inibidoras da bomba de prótons (PPIs). www.fda.gov/Drugs/DrugSafety/ucm245011.htm. Acesso em 17 de fevereiro de 2017.
25. Kieboom BC, Kiefte-de Jong JC, Eijgelsheim M, et al. Inibidores da bomba de prótons e hipomagnesemia na população em geral: um estudo de coorte de base populacional. Am J Kidney Dis. 2015;66:775-782.
26. Park CH, Kim EH, Roh YH, et al. The association between the use of proton pump inhibitors and the risk of hypomagnesemia: a systematic review and meta-analysis. PLoS Um. 2014;9:e112558.
27. Luk CP, Parsons R, Lee YP, Hughes JD. Hipomagnesemia associada à bomba de prótons: o que nos dizem os dados da FDA? Ann Pharmacother. 2013;47:773-780.
28. Cheungpasitporn W, Thongprayoon C, Kittanamongkolchai W, et al. Inibidores da bomba de prótons ligados à hipomagnesemia: uma revisão sistemática e uma meta-análise de estudos observacionais. Ren Fail. 2015;37:1237-1241.
29. Markovits N, Loebstein R, Halkin H, et al. The association of proton pump inhibitors and hypomagnesemia in the community setting. J Clin Pharmacol. 2014;54:889-895.
30. Park SH, Lee SH, Lee JS, et al. Alterações na concentração sérica de magnésio após o uso de um inibidor da bomba de protões em pacientes submetidos a intervenção coronária percutânea. Prática Clínica de Res-Rim. 2015;34:98-102.
31. Danziger J, William JH, Scott DJ, et al. O uso do inibidor da bomba de prótons está associado a baixas concentrações séricas de magnésio. Rim Int. 2013;83:692-699.
32. Begley J, Smith T, Barnett K, et al. O inibidor da bomba de prótons associado à hipomagnesaemia – um motivo de preocupação? Br J Clin Pharmacol. 2016;81:753-758.
33. Abraham NS, Hlatky MA, Antman EM, et al. ACCF/ACG/AHA 2010 documento de consenso de especialistas sobre o uso concomitante de inibidores da bomba de protões e tienopiridinas: uma atualização focada do documento de consenso de especialistas ACCF/ACG/AHA 2008 sobre a redução dos riscos gastrointestinais da terapia antiplaquetária e do uso de AINEs. Am J Gastroenterol. 2010;105:2533-2549.
34. Melloni C, Washam JB, Jones WS, et al. Resultados conflitantes entre ensaios randomizados e estudos observacionais sobre o impacto dos inibidores da bomba de prótons nos eventos cardiovasculares quando coadministrados com terapia antiplaquetária dupla: revisão sistemática. Circ Cardiovasc Qual Outcomes. 2015;8:47-55.
35. Lembrete da FDA para evitar o uso concomitante de Plavix (clopidogrel) e omeprazol. www.fda.gov/Drugs/DrugSafety/ucm231161.htm. Acesso em 17 de fevereiro de 2017.
36. Bundhun PK, Teeluck AR, Bhurtu A, Huang WQ. O uso concomitante de inibidores de clopidogrel e bomba de prótons ainda está associado ao aumento de resultados cardiovasculares adversos após angioplastia coronária?: uma revisão sistemática e meta-análise de estudos recentemente publicados (2012-2016). BMC Cardiovasc Disord. 2017;17:3.