Výstupy z učení
- Popsat chování a umístění elektronů a vliv těchto faktorů na tvorbu vazeb mezi atomy
Elektronové obaly a Bohrův model

Obrázek 1. Bohrův model.
Je třeba zdůraznit, že existuje souvislost mezi počtem protonů v prvku, atomovým číslem, které odlišuje jeden prvek od druhého, a počtem elektronů, které má. Ve všech elektricky neutrálních atomech je počet elektronů stejný jako počet protonů. Každý prvek, alespoň pokud je elektricky neutrální, má tedy charakteristický počet elektronů rovný svému atomovému číslu.
Raný model atomu vypracoval v roce 1913 dánský vědec Niels Bohr (1885-1962). V tomto modelu elektrony existují v hlavních slupkách. Elektron obvykle existuje v nejnižší dostupné energetické slupce, která je nejblíže jádru. Energie z fotonu světla jej může posunout do vyšší energetické slupky, ale tato situace je nestabilní a elektron se rychle rozpadá zpět do základního stavu. Přitom se uvolní foton světla.
Bohrův model znázorňuje atom jako centrální jádro obsahující protony a neutrony, přičemž elektrony jsou na kruhových orbitalech v určitých vzdálenostech od jádra, jak je znázorněno na obrázku 1. Na obrázku 1 je znázorněno, že elektron je v kruhovém orbitalu. Tyto orbity tvoří elektronové slupky nebo energetické hladiny, které jsou způsobem vizualizace počtu elektronů ve vnějších slupkách. Tyto energetické hladiny se označují číslem a symbolem „n“. Například 1n představuje první energetickou hladinu, která se nachází nejblíže jádru.
Elektrony zaplňují orbitaly v důsledném pořadí: nejprve zaplňují orbitaly nejblíže jádru, poté pokračují v zaplňování orbitalů s rostoucí energií dále od jádra. Pokud existuje více orbitalů se stejnou energií, vyplní je v každé energetické hladině jeden elektron, než se přidá druhý elektron. Elektrony nejvzdálenější energetické hladiny určují energetickou stabilitu atomu a jeho tendenci vytvářet chemické vazby s jinými atomy za vzniku molekul.
Za standardních podmínek atomy nejprve zaplní vnitřní slupky, což často vede k proměnlivému počtu elektronů ve vnější slupce. Nejvnitřnější slupka má maximálně dva elektrony, ale další dvě elektronové slupky mohou mít každá maximálně osm elektronů. To je známé jako pravidlo oktetu, které říká, že s výjimkou nejvnitřnější slupky jsou atomy energeticky stabilnější, když mají osm elektronů ve své valenční slupce, nejvzdálenější elektronové slupce. Příklady některých neutrálních atomů a jejich elektronových konfigurací jsou uvedeny na obrázku 2. Všimněte si, že na tomto obrázku má helium úplnou vnější elektronovou slupku, jejíž první a jedinou slupku vyplňují dva elektrony. Podobně má neon úplný vnější obal 2n obsahující osm elektronů. Naproti tomu chlor a sodík mají ve svých vnějších slupkách sedm, respektive jeden elektron, ale teoreticky by byly energeticky stabilnější, kdyby se řídily pravidlem oktetu a měly jich osm.
Praktická otázka
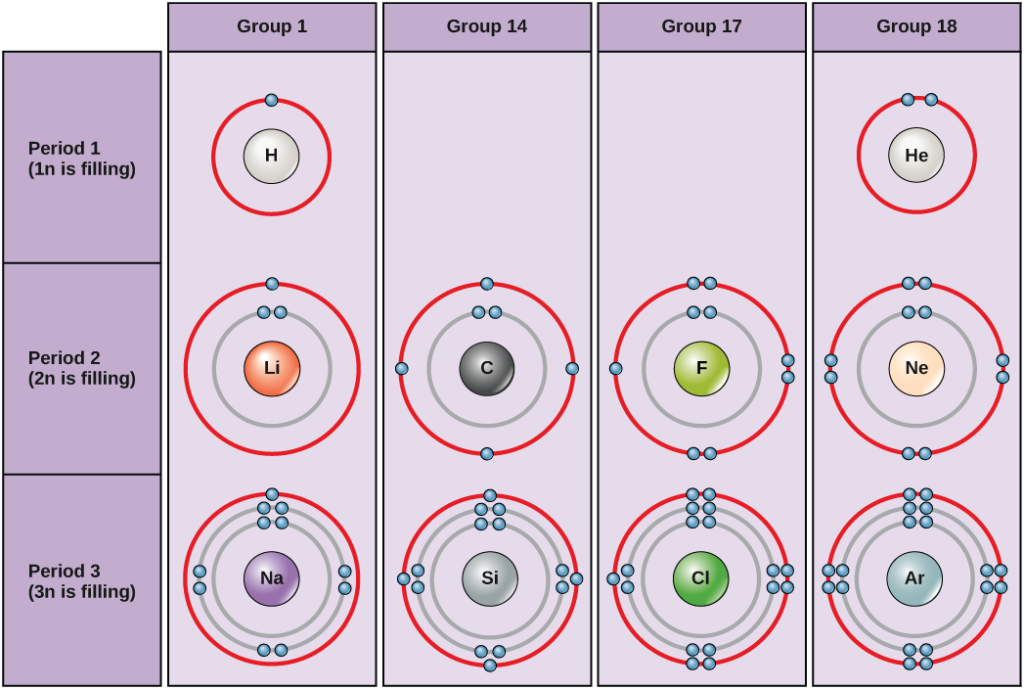
Obrázek 2. Obrázek 2: Chlor a sodík mají ve svých vnějších slupkách sedm elektronů. Bohrovy diagramy pro vodík, helium, lithium, uhlík, fluor, neon, sodík, křemík, chlor a argon.
Bohrovy diagramy udávají, kolik elektronů vyplňuje každou hlavní slupku. Prvky skupiny 18 (helium, neon a argon jsou zobrazeny na obrázku 2) mají plnou vnější neboli valenční slupku. Plná valenční slupka je nejstabilnější elektronová konfigurace. Prvky v ostatních skupinách mají částečně zaplněné valenční slupky a získávají nebo ztrácejí elektrony, aby dosáhly stabilní elektronové konfigurace.
Atom může odevzdat, přijmout nebo sdílet elektrony s jiným atomem, aby dosáhl plné valenční slupky, nejstabilnější elektronové konfigurace. Když se podíváte na tento obrázek, kolik elektronů musí prvky skupiny 1 ztratit, aby dosáhly stabilní elektronové konfigurace? Kolik elektronů musí získat prvky ve skupinách 14 a 17, aby dosáhly stabilní konfigurace?
Poznat, že uspořádání periodické tabulky je založeno na celkovém počtu protonů (a elektronů), nám pomáhá poznat, jak jsou elektrony rozděleny mezi vnější obaly. Periodická tabulka je uspořádána do sloupců a řádků podle počtu elektronů a podle toho, kde se tyto elektrony nacházejí. Podívejte se blíže na některé prvky v pravém sloupci periodické tabulky na obrázku 3.

Obrázek 3. Periodická tabulka zobrazuje atomovou hmotnost a atomové číslo každého prvku. Atomové číslo je uvedeno nad symbolem prvku a přibližná atomová hmotnost pod ním.
Atomy helia (He), neonu (Ne) a argonu (Ar) ze skupiny 18 mají zaplněné vnější elektronové obaly, takže pro dosažení stability není nutné, aby sdílely elektrony s jinými atomy; jako samostatné atomy jsou vysoce stabilní. Jejich nereaktivita vedla k jejich pojmenování inertní plyny (nebo vzácné plyny). Porovnejte je s prvky 1. skupiny v levém sloupci. Všechny tyto prvky, včetně vodíku (H), lithia (Li) a sodíku (Na), mají ve svých vnějších slupkách jeden elektron. To znamená, že mohou dosáhnout stabilní konfigurace a zaplněné vnější slupky tím, že darují nebo sdílejí jeden elektron s jiným atomem nebo molekulou, například s vodou. Vodík daruje nebo sdílí svůj elektron, aby dosáhl této konfigurace, zatímco lithium a sodík darují svůj elektron, aby se staly stabilními. V důsledku ztráty záporně nabitého elektronu se z nich stanou kladně nabité ionty. Prvky 17. skupiny, včetně fluoru a chloru, mají ve svých krajních slupkách sedm elektronů, takže mají tendenci zaplnit tuto slupku elektronem z jiných atomů nebo molekul, čímž se stávají záporně nabitými ionty. Prvky skupiny 14, z nichž je pro živé systémy nejdůležitější uhlík, mají ve své vnější slupce čtyři elektrony, což jim umožňuje vytvářet s jinými atomy několik kovalentních vazeb (o nichž pojednáváme níže). Sloupce periodické tabulky tedy představují potenciální společný stav vnějších elektronových obalů těchto prvků, který je zodpovědný za jejich podobné chemické vlastnosti.
Elektronové orbitaly
Ačkoli je užitečný pro vysvětlení reaktivity a chemických vazeb některých prvků, Bohrův model atomu přesně neodráží, jak jsou elektrony prostorově rozloženy kolem jádra. Neobíhají kolem jádra jako Země kolem Slunce, ale nacházejí se v elektronových orbitalech. Tyto poměrně složité tvary vyplývají ze skutečnosti, že elektrony se chovají nejen jako částice, ale také jako vlny. Matematické rovnice z kvantové mechaniky známé jako vlnové funkce mohou s určitou mírou pravděpodobnosti předpovědět, kde se elektron v daném okamžiku může nacházet. Oblast, kde se elektron s největší pravděpodobností nachází, se nazývá jeho orbital.

Obrázek 4. Kliknutím získáte větší obrázek. Podpouzdra s mají tvar koule. Obě hlavní slupky 1n i 2n mají orbital s, ale velikost koule je u orbitalu 2n větší. Každá sféra je jeden orbital. p podpouzdra jsou tvořena třemi orbitaly ve tvaru činky. Hlavní slupka 2n má podslupku p, ale slupka 1 ji nemá.
Připomeňte si, že Bohrův model znázorňuje konfiguraci elektronových slupek atomu. V každé elektronové slupce jsou podslupky a každá podslupka má určitý počet orbitalů obsahujících elektrony. I když nelze přesně vypočítat, kde se elektron nachází, vědci vědí, že se s největší pravděpodobností nachází v rámci své orbitální dráhy. Podpouzdra se označují písmeny s, p, d a f. Podpouzdro s má kulový tvar a jeden orbital. Hlavní slupka 1n má pouze jeden orbital s, který může obsahovat dva elektrony. Hlavní slupka 2n má jednu s a jednu p podslupku a může obsahovat celkem osm elektronů. Podpouzdro p má tři orbitaly ve tvaru činky, jak je znázorněno na obrázku 4. Podpouzdra d a f mají složitější tvary a obsahují pět, resp. sedm orbitalů. Ty nejsou na obrázku znázorněny. Hlavní slupka 3n má slupky s, p a d a může obsahovat 18 elektronů. Hlavní slupka 4n má orbitaly s, p, d a f a může obsahovat 32 elektronů. Směrem od jádra se počet elektronů a orbitalů nacházejících se v energetických hladinách zvyšuje. Postupujeme-li od jednoho atomu k dalšímu v periodické tabulce, můžeme elektronovou strukturu vypracovat tak, že do dalšího volného orbitalu umístíme další elektron.
Orbital nejblíže jádru, nazývaný 1s orbital, může pojmout až dva elektrony. Tento orbital odpovídá nejvnitřnějšímu elektronovému obalu Bohrova modelu atomu. Nazývá se 1s orbital, protože je kulový kolem jádra. Orbital 1s je nejblíže jádru a je vždy zaplněn jako první, dříve než může být zaplněn jakýkoli jiný orbital. Vodík má jeden elektron, proto má v orbitalu 1s obsazeno pouze jedno místo. To se označuje jako 1s1, kde horní index 1 označuje jeden elektron v orbitalu 1s. Helium má dva elektrony, proto může orbital 1s zcela zaplnit svými dvěma elektrony. Označuje se jako 1s2, což znamená dva elektrony helia v orbitalu 1s. Na obrázku 4 periodické tabulky jsou vodík a helium jedinými dvěma prvky v prvním řádku (periodě); je to proto, že mají elektrony pouze ve své první slupce, orbitalu 1s. Vodík a helium jsou jediné dva prvky, které mají v elektricky neutrálním stavu orbital 1s a žádný jiný elektronový orbital.
Druhý elektronový obal může obsahovat osm elektronů. Tato slupka obsahuje další sférický orbital s a tři orbitaly p ve tvaru „činky“, z nichž každý může obsahovat dva elektrony, jak je znázorněno na obrázku 4. Po zaplnění orbitalu 1s se zaplní druhá elektronová slupka, přičemž se nejprve zaplní její orbital 2s a poté její tři orbitaly p. Při zaplňování p orbitalů přijímá každý z nich jeden elektron; jakmile má každý p orbital elektron, může být přidán druhý. Lithium (Li) obsahuje tři elektrony, které obsazují první a druhou slupku. Dva elektrony vyplňují orbital 1s a třetí elektron pak vyplňuje orbital 2s. Jeho elektronová konfigurace je 1s22s1. Naproti tomu neon (Ne) má celkem deset elektronů: dva jsou v jeho nejvnitřnějším orbitalu 1s a osm vyplňuje jeho druhou slupku (po dvou v orbitalech 2s a třech p); je tedy inertním plynem a energeticky stabilní jako jediný atom, který jen zřídka vytvoří chemickou vazbu s jinými atomy. Větší prvky mají další orbitaly, které tvoří třetí elektronový obal. Ačkoli pojmy elektronový obal a orbitaly spolu úzce souvisejí, orbitaly poskytují přesnější zobrazení elektronové konfigurace atomu, protože orbitální model specifikuje různé tvary a speciální orientace všech míst, která mohou elektrony zaujímat.
Podívejte se na tuto vizuální animaci a prohlédněte si prostorové uspořádání p a s orbitalů. Všimněte si, že toto video neobsahuje žádný zvuk.
Zde si můžete prohlédnout text zvukového popisu k „Atomic Orbitals – Electron Configuration of Scandium“ (otevře se v novém okně).
Video Review
Toto video poskytuje další přehled elektronů:
Try It
Přispějte!
Vylepšete tuto stránkuZjistěte více