Learning Outcomes
- Beschrijf het gedrag en de plaats van elektronen, en hoe deze factoren van invloed zijn op de vorming van bindingen tussen atomen
Electron Shells and the Bohr Model

Figuur 1. Het Bohr-model.
Het moet worden benadrukt dat er een verband bestaat tussen het aantal protonen in een element, het atoomnummer dat het ene element van het andere onderscheidt, en het aantal elektronen dat het heeft. In alle elektrisch neutrale atomen is het aantal elektronen gelijk aan het aantal protonen. Elk element, althans wanneer het elektrisch neutraal is, heeft dus een karakteristiek aantal elektronen dat gelijk is aan zijn atoomnummer.
Een vroeg model van het atoom werd in 1913 ontwikkeld door de Deense wetenschapper Niels Bohr (1885-1962). In dit model bestaan de elektronen in hoofdschillen. Een elektron bevindt zich normaliter in de laagst beschikbare energieschil, die zich het dichtst bij de kern bevindt. Energie van een lichtfoton kan het elektron naar een hogere energieschil brengen, maar deze situatie is onstabiel en het elektron valt snel terug naar de grondtoestand. Daarbij komt een lichtfoton vrij.
Het Bohr-model toont het atoom als een centrale kern met protonen en neutronen, met de elektronen in cirkelvormige banen op specifieke afstanden van de kern, zoals geïllustreerd in figuur 1. Deze banen vormen elektronenschillen of energieniveaus, die een manier zijn om het aantal elektronen in de buitenste schillen weer te geven. Deze energieniveaus worden aangeduid met een getal en het symbool “n”. Bijvoorbeeld, 1n vertegenwoordigt het eerste energieniveau dat zich het dichtst bij de kern bevindt.
Elektronen vullen de banen in een consistente volgorde: eerst vullen zij de banen die zich het dichtst bij de kern bevinden, daarna gaan zij verder met het vullen van banen met toenemende energie die zich verder van de kern bevinden. Als er meerdere banen van gelijke energie zijn, zullen deze in elk energieniveau met één elektron worden gevuld voordat er een tweede elektron wordt toegevoegd. De elektronen van het buitenste energieniveau bepalen de energetische stabiliteit van het atoom en zijn neiging om chemische bindingen te vormen met andere atomen om moleculen te vormen.
Onder standaardomstandigheden vullen atomen eerst de binnenste schillen, wat vaak resulteert in een variabel aantal elektronen in de buitenste schil. De binnenste schil heeft maximaal twee elektronen, maar de volgende twee elektronenschillen kunnen elk maximaal acht elektronen hebben. Dit staat bekend als de octet-regel, die stelt dat, met uitzondering van de binnenste schil, atomen energetisch stabieler zijn wanneer zij acht elektronen in hun valentieschil, de buitenste elektronenschil, hebben. Voorbeelden van enkele neutrale atomen en hun elektronenconfiguraties zijn te zien in figuur 2. Merk op dat helium in deze figuur een volledige buitenste elektronenschil heeft, met twee elektronen die de eerste en enige schil vullen. Evenzo heeft neon een volledige buitenste 2n schil met acht elektronen. Daarentegen hebben chloor en natrium respectievelijk zeven en één in hun buitenste schil, maar theoretisch zouden ze energetisch stabieler zijn als ze de octetregel volgden en er acht hadden.
Praktijkvraag
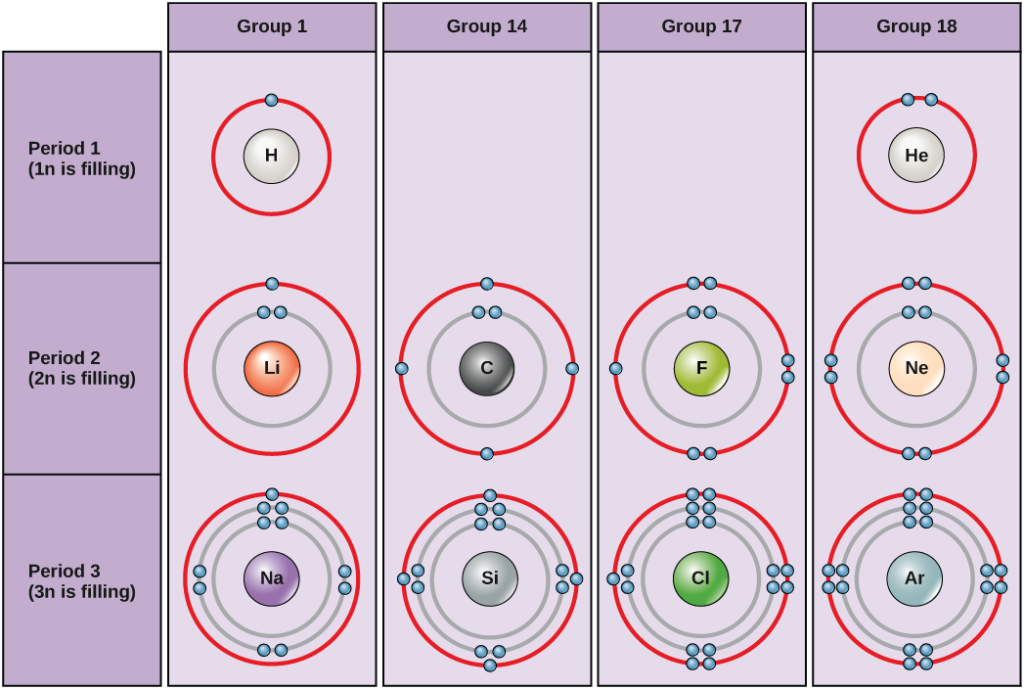
Figuur 2. Bohr-diagrammen voor waterstof, helium, lithium, koolstof, fluor, neon, natrium, silicium, chloor en argon.
Bohr-diagrammen geven aan met hoeveel elektronen elke hoofdschil is gevuld. De elementen van groep 18 (helium, neon en argon zijn afgebeeld in figuur 2) hebben een volle buitenste schil, de valentieschil. Een volle valentieschil is de meest stabiele elektronenconfiguratie. Elementen in andere groepen hebben gedeeltelijk gevulde valentieschillen en winnen of verliezen elektronen om een stabiele elektronenconfiguratie te bereiken.
Een atoom kan elektronen geven, nemen of delen met een ander atoom om een volle valentieschil te bereiken, de meest stabiele elektronenconfiguratie. Als je naar deze figuur kijkt, hoeveel elektronen moeten elementen in groep 1 dan verliezen om een stabiele elektronenconfiguratie te bereiken? Hoeveel elektronen moeten elementen uit de groepen 14 en 17 winnen om een stabiele elektronenconfiguratie te bereiken?
Weten dat de organisatie van het periodiek systeem gebaseerd is op het totaal aantal protonen (en elektronen) helpt ons te weten hoe de elektronen over de buitenste schil zijn verdeeld. Het periodiek systeem is gerangschikt in kolommen en rijen op basis van het aantal elektronen en waar deze elektronen zich bevinden. Bekijk enkele elementen in de meest rechtse kolom van het periodiek systeem in figuur 3.

Figuur 3. Het periodiek systeem toont de atoommassa en het atoomnummer van elk element. Het atoomnummer staat boven het symbool voor het element en de geschatte atoommassa staat eronder.
De groep 18-atomen helium (He), neon (Ne) en argon (Ar) hebben allemaal gevulde buitenste elektronenschillen, waardoor ze geen elektronen hoeven te delen met andere atomen om stabiliteit te bereiken; ze zijn zeer stabiel als afzonderlijke atomen. Omdat ze niet reactief zijn, worden ze de inerte gassen (of edelgassen) genoemd. Vergelijk dit met de elementen van groep 1 in de linkerkolom. Deze elementen, waaronder waterstof (H), lithium (Li), en natrium (Na), hebben allemaal één elektron in hun buitenste schil. Dat betekent dat zij een stabiele configuratie en een gevulde buitenste schil kunnen krijgen door een elektron af te staan of te delen met een ander atoom of een molecuul, zoals water. Waterstof zal zijn elektron afstaan of delen om deze configuratie te bereiken, terwijl lithium en natrium hun elektron zullen afstaan om stabiel te worden. Als gevolg van het verlies van een negatief geladen elektron, worden zij positief geladen ionen. Elementen van groep 17, waaronder fluor en chloor, hebben zeven elektronen in hun buitenste schil, zodat ze de neiging hebben deze schil te vullen met een elektron van andere atomen of moleculen, waardoor ze negatief geladen ionen worden. De elementen van groep 14, waarvan koolstof het belangrijkste is voor levende systemen, hebben vier elektronen in hun buitenste schil, waardoor ze verschillende covalente bindingen (die hieronder worden besproken) kunnen aangaan met andere atomen. De kolommen van het periodiek systeem geven dus de potentieel gedeelde toestand van de buitenste elektronenschillen van deze elementen weer, die verantwoordelijk is voor hun vergelijkbare chemische eigenschappen.
Elektronenbanen
Hoewel nuttig om de reactiviteit en chemische binding van bepaalde elementen te verklaren, geeft het Bohr-model van het atoom niet accuraat weer hoe elektronen ruimtelijk verdeeld zijn rond de kern. Zij omcirkelen de kern niet zoals de aarde om de zon draait, maar bevinden zich in elektronenbanen. Deze relatief complexe vormen zijn het gevolg van het feit dat elektronen zich niet alleen als deeltjes gedragen, maar ook als golven. Wiskundige vergelijkingen uit de kwantummechanica, bekend als golffuncties, kunnen met een bepaalde mate van waarschijnlijkheid voorspellen waar een elektron zich op een bepaald moment kan bevinden. Het gebied waar een elektron zich het meest waarschijnlijk bevindt, wordt zijn orbitaal genoemd.

Figuur 4. Klik voor een grotere afbeelding. De s-deelschalen hebben de vorm van bollen. Zowel de 1n- als de 2n-hoofdschil hebben een s-baan, maar de grootte van de bol is groter bij de 2n-baan. Elke bol is een enkele orbitaal. p deelschelpen bestaan uit drie haltervormige orbitalen. Hoofdschil 2n heeft een p-subschil, maar schil 1 niet.
Bedenk dat het Bohr-model de elektronenschilconfiguratie van een atoom weergeeft. Binnen elke elektronenschil zijn subschillen, en elke subschil heeft een bepaald aantal banen die elektronen bevatten. Hoewel het onmogelijk is precies te berekenen waar een elektron zich bevindt, weten wetenschappers dat het zich hoogstwaarschijnlijk binnen zijn baan bevindt. Subschillen worden aangeduid met de letters s, p, d en f. De s-subschil is bolvormig en heeft één orbitaal. Hoofdschil 1n heeft slechts één s-schil, die twee elektronen kan bevatten. Hoofdschil 2n heeft één s- en één p-subschil, en kan in totaal acht elektronen bevatten. De p-subschil heeft drie haltervormige orbitalen, zoals geïllustreerd in figuur 4. De d- en f-subschalen hebben een complexere vorm en bevatten respectievelijk vijf en zeven orbitalen. Deze zijn niet te zien in de illustratie. De hoofdschil 3n heeft s-, p- en d-subschillen en kan 18 elektronen bevatten. De hoofdschil 4n heeft s-, p-, d- en f-banen en kan 32 elektronen bevatten. Als men zich van de atoomkern verwijdert, neemt het aantal elektronen en banen in de energieniveaus toe. Van het ene atoom naar het volgende in het periodiek systeem kan de elektronenstructuur worden uitgewerkt door een extra elektron in te passen in de eerstvolgende beschikbare baan.
De baan die het dichtst bij de kern ligt, de 1s-baan genoemd, kan maximaal twee elektronen bevatten. Deze orbitaal komt overeen met de binnenste elektronenschil van het Bohr-model van het atoom. Hij wordt de 1s-baan genoemd omdat hij bolvormig is rond de atoomkern. De 1s-baan is de baan die het dichtst bij de atoomkern ligt, en wordt altijd als eerste gevuld, voordat een andere baan kan worden gevuld. Waterstof heeft één elektron; daarom is er maar één plek in de 1s-baan bezet. Dit wordt aangeduid als 1s1, waarbij de superscripted 1 verwijst naar het ene elektron in de 1s-baan. Helium heeft twee elektronen; daarom kan het de 1s-baan volledig vullen met zijn twee elektronen. Dit wordt aangeduid als 1s2, verwijzend naar de twee elektronen van helium in de 1s orbitaal. In het periodiek systeem Figuur 4 zijn waterstof en helium de enige twee elementen in de eerste rij (periode); dit komt omdat zij alleen elektronen hebben in hun eerste schil, de 1s-baan. Waterstof en helium zijn de enige twee elementen die de 1s en geen andere elektronenbanen hebben in de elektrisch neutrale toestand.
De tweede elektronenschil kan acht elektronen bevatten. Deze schil bevat nog een bolvormige s-baan en drie “halter”-vormige p-banen, die elk twee elektronen kunnen bevatten, zoals te zien is in figuur 4. Nadat de 1s-baan is gevuld, wordt de tweede elektronenschil gevuld, waarbij eerst de 2s-baan en daarna de drie p-banen worden opgevuld. Bij het vullen van de p-banen neemt elke p-baan een enkel elektron op; zodra elke p-baan een elektron heeft, kan een tweede worden toegevoegd. Lithium (Li) bevat drie elektronen die de eerste en tweede schil bezetten. Twee elektronen vullen de 1s orbitaal, en het derde elektron vult dan de 2s orbitaal. De elektronenconfiguratie is 1s22s1. Neon (Ne) daarentegen heeft in totaal tien elektronen: twee in de binnenste 1s-baan en acht in de tweede schil (elk twee in de 2s-baan en drie p-banen); het is dus een inert gas en energetisch stabiel als een enkel atoom dat zelden een chemische verbinding met andere atomen zal vormen. Grotere elementen hebben extra banen, die samen de derde elektronenschil vormen. Hoewel de concepten van elektronenschillen en orbitalen nauw verwant zijn, geven orbitalen een nauwkeuriger beeld van de elektronenconfiguratie van een atoom, omdat het orbitaalmodel de verschillende vormen en speciale oriëntaties specificeert van alle plaatsen die elektronen kunnen innemen.
Bekijk deze visuele animatie om de ruimtelijke rangschikking van de p- en s-banen te zien. Merk op dat deze video geen audio heeft.
U kunt de audiobeschrijvingstekst voor “Atomic Orbitals – Electron Configuration of Scandium” hier bekijken (opent in een nieuw venster).
Video Review
Deze video geeft nog een overzicht van het elektron:
Try It
Contribute!
Verbeter deze paginaLees meer