US Pharm. 2017;42(6)(Generic Drugs suppl):38-42.
ABSTRACT: Inhibitorii pompei de protoni (IPP) sunt o clasă de agenți antisecretori utilizați pentru a trata diverse afecțiuni gastrointestinale, cum ar fi boala de reflux gastroesofagian, tulburările legate de Helicobacter pylori și ulcerele gastrice și duodenale. Deși acești agenți sunt supresori acizi eficienți, utilizarea IPP-urilor este frecvent dezbătută pe baza rapoartelor privind noi evenimente adverse potențiale. Suprautilizarea și interacțiunile medicamentoase sunt probleme asociate cu IPP. În plus, deoarece mai multe IPP sunt disponibile OTC, utilizarea necorespunzătoare a acestor agenți reprezintă o preocupare semnificativă. Farmaciștii din toate mediile pot avea un impact profund asupra utilizării necorespunzătoare a IPP prin asigurarea inițierii și continuării adecvate a terapiei, a dozelor și a duratei tratamentului.
Inhibitorii pompei de protoni (IPP) sunt o clasă de medicamente utilizate în mod obișnuit pentru tratamentul diferitelor tulburări gastrointestinale (GI), inclusiv boala de reflux gastroesofagian (GERD), tulburările legate de Helicobacter pylori și ulcerul gastric și duodenal. Deși acești agenți antisecretori sunt tratamentul preferat pentru numeroase afecțiuni, această clasă este afectată de o utilizare excesivă și de rapoarte privind efecte adverse potențial grave și interacțiuni medicamentoase.1 În plus, gestionarea pacienților cu afecțiuni tratate cu IPP este complicată de disponibilitatea OTC a mai multor dintre acești agenți. Acest articol își propune să evidențieze utilizarea adecvată și să ofere o descriere bazată pe dovezi a mai multor dezavantaje noi sau puternic dezbătute ale acestor agenți.
Disponibilitatea IPP-urilor
Șase IPP-uri unice, dintre care cinci sunt disponibile sub formă generică, pot fi obținute pe bază de prescripție medicală (TABELUL 1).2-7 Doze mici de omeprazol, lansoprazol și o versiune de marcă a esomeprazolului de magneziu sunt disponibile OTC. Omeprazolul este utilizat, de asemenea, într-un produs coformulat cu bicarbonat de sodiu. Acest articol se va concentra în primul rând asupra IPP-urilor disponibile în mod generic, cu dozare orală.
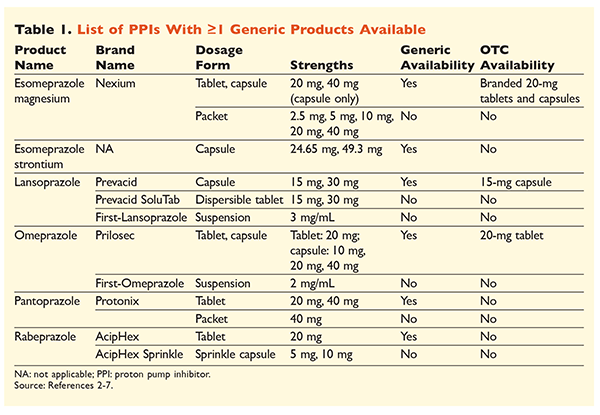
Esomeprazol stronțiu a fost aprobat de FDA pe baza bioechivalenței sale cu esomeprazol magneziu.3 Deși etichetarea produsului pentru acești doi agenți este foarte asemănătoare, există trei diferențe notabile. În primul rând, esomeprazolul stronțiu este disponibil în capsule de 24,65 mg și 49,3 mg, care sunt echivalente cu esomeprazolul de magneziu 20 mg și, respectiv, 40 mg. În al doilea rând, esomeprazol stronțiu nu este aprobat de FDA pentru utilizare la pacienții pediatrici, în timp ce esomeprazol magneziu este aprobat pentru utilizare la cei cu vârsta de 1 lună și peste. În cele din urmă, utilizarea esomeprazolului stronțiu trebuie evitată în cazul insuficienței renale severe, deoarece nu a fost studiat la această populație. Nu se recomandă nicio ajustare a dozei pentru esomeprazol magneziu.3 În scopul acestui articol, termenul esomeprazol va fi utilizat pentru a descrie esomeprazolul magneziu.
Administrare
Toate IPP-urile disponibile generic, inclusiv capsulele și comprimatele, trebuie înghițite întregi, fără a fi divizate, zdrobite sau mestecate.2-7 Capsulele de omeprazol, lansoprazol și esomeprazol pot fi deschise și conținutul poate fi presărat pe compot de mere pentru pacienții care nu pot înghiți formele farmaceutice orale. În plus, capsulele de lansoprazol pot fi stropite în 2 oz de suc de mere, roșii sau portocale. Orice amestec care conține conținutul capsulelor deschise trebuie înghițit imediat și nu trebuie păstrat pentru utilizare ulterioară.2,4,5
Lansoprazolul, omeprazolul și esomeprazolul trebuie administrate înainte de mese, dar recomandările specifice privind orele de administrare variază. Omeprazolul trebuie administrat cu 30 până la 60 de minute înainte de masă, iar esomeprazolul cu cel puțin 60 de minute înainte; pentru lansoprazol nu este specificat un interval de timp.2,4,5 Pantoprazolul poate fi administrat cu sau fără alimente.6 Rabeprazolul trebuie administrat după masă în cazul ulcerului duodenal și cu o masă pentru eradicarea H pylori; pentru toate celelalte indicații, rabeprazolul poate fi administrat cu sau fără alimente.7
Dosarea și durata tratamentului
Datorită reputației IPP de a fi foarte eficiente și, în general, sigure, suprautilizarea semnificativă a IPP reprezintă o preocupare majoră.1 Nu numai că IPP sunt adesea administrate pentru indicații fără dovezi care să le susțină utilizarea, dar aceste medicamente sunt, de asemenea, frecvent prescrise la doze mai mari decât este necesar pentru durate de tratament care se extind dincolo de intervalele de timp recomandate.8,9 Doza aprobată pentru fiecare IPP și durata recomandată a tratamentului sunt prezentate în TABELURILE 2 și 3. Recomandările de tratament care diferă de cele aprobate de FDA, precum și perlele clinice notabile legate de inițierea, dozarea și durata tratamentului cu IPP, sunt prezentate mai jos.
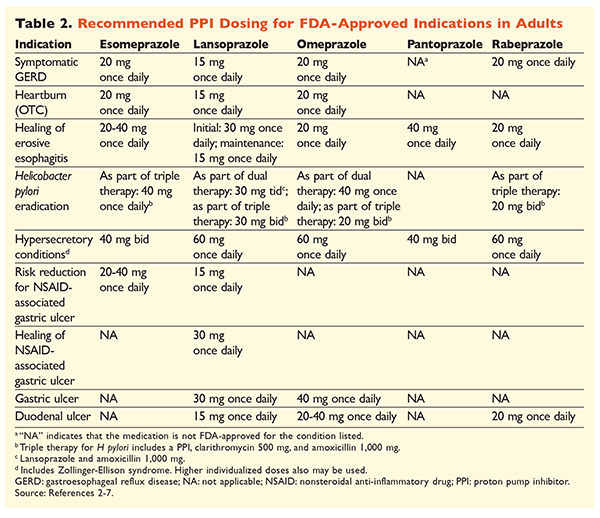
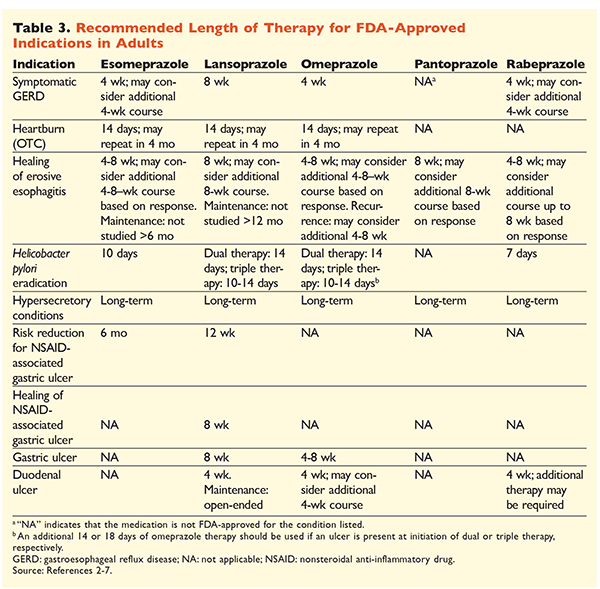
DROG: La pacienții cu RGE, toate IPP sunt considerate la fel de eficiente și se recomandă o cură de 8 săptămâni de tratament cu orice agent disponibil.10 Pacienții cu simptome refractare la tratament după 2 până la 3 luni pot necesita un tratament de întreținere pe termen lung cu doze de două ori pe zi. Cu toate acestea, trebuie utilizată cea mai mică doză eficientă, iar în cazul în care pacientul nu răspunde la terapie trebuie să se ia în considerare un alt IPP.10 Alternativ, se poate lua în considerare un tratament cu IPP la nevoie sau o abordare progresivă către un antagonist al receptorilor de histamină2 (H2RA).10 Tratamentul cu un IPP de vânzare fără prescripție medicală trebuie să se limiteze la 14 zile, iar retratamentul nu trebuie să aibă loc mai frecvent de o dată la 4 luni.11
Ulcer asociat cu H pylori: În funcție de IPP utilizat, regimurile aprobate de FDA pentru eradicarea H pylori includ terapia dublă cu amoxicilină sau claritromicină și terapia triplă cu ambii agenți timp de 7 până la 14 zile.2-5,7 Regimurile de tratament specifice susținute de ghiduri variază în comparație cu cele aprobate de FDA, dar durata recomandată a tratamentului este similară, toate regimurile având un interval de timp de administrare de 10 până la 14 zile.12 După eradicarea H pylori, tratamentul de întreținere cu IPP nu este necesar.13 O discuție mai detaliată a regimurilor specifice depășește scopul acestui articol.
Profilaxie și tratament al ulcerelor induse de AINS: După apariția unui ulcer asociat cu medicamente antiinflamatoare nesteroidiene (AINS), trebuie reevaluată necesitatea tratamentului cu AINS. Dacă se consideră că este adecvată continuarea tratamentului cu AINS, pacienții trebuie menținuți sub tratament selectiv cu ciclooxigenază-2 la cea mai mică doză eficientă, pe cea mai scurtă durată posibilă, în asociere cu un IPP.13
Pentru profilaxie, inițierea unui IPP este recomandată numai la pacienții cu risc moderat sau ridicat de toxicitate GI legată de AINS. Factorii de risc includ vârsta >65 de ani, tratamentul cu AINS în doze mari, un istoric anterior de ulcer necomplicat și utilizarea concomitentă de aspirină (inclusiv în doze mici), corticosteroizi sau anticoagulante. Pacienții considerați ca având un risc moderat de toxicitate gastro-intestinală indusă de AINS îi includ pe cei cu unul sau doi dintre acești factori de risc, în timp ce pacienții cu risc ridicat au mai mult de doi factori de risc sau antecedente de ulcer gastroduodenal complicat anterior, mai ales dacă acesta a fost recent.14 Este rezonabil să se continue tratamentul cu IPP atâta timp cât pacientul cu risc moderat sau ridicat rămâne sub tratament cu AINS.13
Ulcer idiopatic: Ulcerele fără o cauză clar identificabilă sunt susceptibile de a recidiva la pacienții care nu sunt tratați cu terapie supresoare de acid. Ghidurile nu recomandă în mod clar durata de timp în care pacienții ar trebui să fie tratați cu terapie de întreținere, dar sugerează că terapia continuă cu IPP reduce riscul de formare a ulcerului recurent.13
Siguranță
IpPPI sunt în general considerați ca fiind o clasă de medicamente bine tolerate.1 Cu toate acestea, mai multe preocupări legate de siguranță au afectat de mult timp reputația acestora, inclusiv un risc crescut de diaree asociată cu Clostridium difficile, pneumonie dobândită în comunitate și fracturi osoase.15,16 Mai recent, au apărut preocupări legate de demență și de boala cronică de rinichi, iar dezbaterile privind hipomagneziemia și o interacțiune teoretică medicament-medicament cu clopidogrelul au continuat.
Demența: Două studii recente au sugerat potențialul unui risc crescut de demență în cazul utilizării pe termen lung a IPP la vârstnici.17,18 Un mecanism propus în spatele acestei constatări este acela că IPP favorizează dezvoltarea plăcilor beta-amiloide, o fiziopatologie propusă pentru boala Alzheimer.15 Cu toate acestea, limitările studiilor nu susțin o relație cauzală concludentă între utilizarea IPP și o incidență crescută a demenței.19
Complicații renale: Deși IPP au fost recunoscute pe scară largă ca fiind o cauză frecventă a nefritei interstițiale acute, date mai noi implică, de asemenea, acești agenți în dezvoltarea altor complicații renale.15,20 Trei studii recente au sugerat că IPP ar putea fi responsabile de un risc crescut de boală renală cronică și de progresie către boala renală în stadiu terminal.20-22 Cu toate acestea, aceste studii observaționale trebuie interpretate cu prudență, deoarece cauzalitatea nu poate fi confirmată.23
Hipomagneziemia: În 2011, FDA a emis un avertisment conform căruia utilizarea prelungită a IPP pentru perioade care depășesc 1 an poate duce la hipomagneziemie.24 De atunci, mai multe studii considerabile au susținut această constatare.25-29 Relația dintre IPP și hipomagneziemie nu este însă definitivă și este complicată de factori de risc externi.30-32 În prezent, hipomagneziemia indusă de IPP semnificativă din punct de vedere clinic este văzută ca fiind rară și apare mai frecvent cu utilizarea concomitentă a diureticelor.31,32 Monitorizarea este recomandată doar la pacienții cu factori de risc suplimentari.32
Interacțiune medicamentoasă cu Clopidogrel: Clopidogrelul joacă un rol important în reducerea riscului cardiovascular, dar este asociat cu sângerări gastrointestinale, în special la pacienții cu risc crescut. Protecția GI cu IPP este adesea implementată la pacienții care au o probabilitate mai mare de a suferi o hemoragie GI, inclusiv la cei cu o hemoragie anterioară a intestinului digestiv superior; vârsta înaintată; utilizarea concomitentă de anticoagulante, corticosteroizi sau AINS (inclusiv aspirină); și/sau infecția cu H pylori.33
Se consideră că IPP inhibă enzima CYP2C19, calea principală prin care se activează clopidogrelul.33 Această interacțiune poate, teoretic, să diminueze efectele antiplachetare ale clopidogrelului și să crească riscul de rezultate cardiovasculare nefavorabile.33 Pe baza rezultatelor inconsecvente atât din studiile farmacocinetice, cât și din studiile privind rezultatele, totuși, semnificația clinică a acestei interacțiuni este incertă.34
În plus, există o lipsă de consecvență a dovezilor cu privire la adevăratul impact al IPP-urilor individuale asupra efectelor clopidogrelului.33 Cele mai recente recomandări ale FDA sugerează că pantoprazolul este o alegere mai sigură decât alte IPP-uri, în timp ce omeprazolul este considerat a fi cea mai riscantă.35 Datele actuale continuă să susțină această concluzie, dar sunt necesare studii suplimentare pentru a confirma dacă există o diferență între IPP.36
Este important să se cântărească beneficiile și riscurile terapiei antiplachetare singure sau în asociere cu un IPP atunci când se ia o decizie privind adăugarea unui tratament de protecție gastrointestinală. La pacienții cu risc ridicat de complicații gastrointestinale, efectele benefice ale tratamentului cu IPP pot fi mai mari decât scăderea eficacității terapiei antiplachetare, care a fost demonstrată în mod inconsecvent. Pentru pacienții cu risc mai scăzut de complicații GI, un H2RA poate fi o opțiune rezonabilă de tratament, deși această clasă s-a dovedit a fi mai puțin eficientă decât IPP pentru această indicație.33
Concluzie
Farmaciștii din toate mediile pot avea un impact profund asupra utilizării inadecvate a IPP prin asigurarea inițierii și continuării corecte a terapiei, a dozelor și a duratei tratamentului. Pe măsură ce continuă să apară date contradictorii cu privire la profilurile de siguranță ale acestor medicamente, utilizarea pe termen lung a IPP-urilor devine mai complicată. Asigurându-se că cea mai mică doză adecvată este utilizată pentru cea mai scurtă durată necesară, farmaciștii pot contribui la prevenirea expunerii inutile a pacienților la potențiale efecte nocive.
1. Heidelbaugh JJ, Kim AH, Chang R, Walker PC. Suprautilizarea inhibitorilor de pompă de protoni: ce trebuie să știe clinicianul. Therap Adv Gastroenterol. 2012;5:219-232.
2. Nexium (esomeprazol de magneziu) prospect. Wilmington, DE: AstraZeneca Pharmaceuticals LP; decembrie 2016.
3. Esomeprazol stronțiu prospect. Glasgow, KY: Amneal Pharmaceuticals; decembrie 2014.
4. Prevacid (lansoprazol) prospect. Deerfield, IL: Takeda Pharmaceuticals America, Inc; octombrie 2016.
5. Prospectul Prilosec (omeprazol). Wilmington, DE: AstraZeneca Pharmaceuticals LP; decembrie 2016.
6. Protonix (pantoprazol) prospect. Philadelphia, PA: Wyeth Pharmaceuticals Inc. Octombrie 2016.
7. Prospectul AcipHex (rabeprazol). Woodcliff Lake, NJ: Eisai Inc; aprilie 2016.
8. Chia CT, Lim WP, Vu CK. Utilizarea necorespunzătoare a inhibitorilor pompei de protoni într-un cadru local. Singapore Med J. 2014;55:363-366.
9. Kelly OB, Dillane C, Patchett SE, et al. Prescrierea necorespunzătoare a inhibitorilor de pompă de protoni pe cale orală în mediul spitalicesc: un studiu transversal prospectiv. Dig Dis Sci. 2015;60:2280-2286.
10. Katz PO, Gerson LB, Vela MF. Linii directoare pentru diagnosticul și managementul bolii de reflux gastroesofagian. Am J Gastroenterol. 2013;108:308-328.
11. Comunicarea FDA privind siguranța medicamentelor: posibil risc crescut de fracturi ale șoldului, încheieturii mâinii și coloanei vertebrale în cazul utilizării inhibitorilor pompei de protoni. www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPatientsandProviders/ucm213206.htm. Accesat la 17 februarie 2017.
12. Chey WD, Leontiadis GI, Howden CW, Moss SF. Ghidul clinic ACG: tratamentul infecției cu Helicobacter pylori. Am J Gastroenterol. 2017;112:212-239.
13. Laine L, Jensen DM. Managementul pacienților cu sângerare ulceroasă. Am J Gastroenterol. 2012;107:345-360.
14. Lanza FL, Chan FK, Chan FK, Quigley EM. Orientări pentru prevenirea complicațiilor ulcerului legate de AINS. Am J Gastroenterol. 2009;104:728-738.
15. Eusebi LH, Rabitti S, Artesiani ML, et al. Inhibitori ai pompei de protoni: riscuri ale utilizării pe termen lung. J Gastroenterol Hepatol. 2017; Jan 16 .
16. Abramowitz J, Thakkar P, Isa A, et al. Raportarea evenimentelor adverse pentru tratamentul cu inhibitori de pompă de protoni: o prezentare generală a analizelor sistematice. Otolaryngol Head Neck Surg. 2016;155:547-554.
17. Haenisch B, von Holt K, Wiese B, et al. Riscul de demență la pacienții vârstnici în cazul utilizării inhibitorilor de pompă de protoni. Eur Arch Psychiatry Clin Neurosci. 2015;265:419-428.
18. Gomm W, von Holt K, Thomé F, et al. Asocierea inhibitorilor de pompă de protoni cu riscul de demență: o analiză farmacoepidemiologică a datelor privind cererile de rambursare. JAMA Neurol. 2016;73:410-416.
19. Kuller LH. Inhibitorii pompei de protoni cresc riscul de demență? JAMA Neurol. 2016;73:379-381.
20. Arora P, Gupta A, Golzy M, et al. Inhibitorii de pompă de protoni sunt asociați cu un risc crescut de dezvoltare a bolii renale cronice. BMC Nephrol. 2016;17:112.
21. Xie Y, Bowe B, Li T, et al. Inhibitorii de pompă de protoni și riscul de apariție a bolii cronice cronice cronice incidente și de progresie spre ESRD. J Am Soc Nephrol. 2016;27:3153-3163.
22. Lazarus B, Chen Y, Wilson FP, et al. Utilizarea inhibitorilor de pompă de protoni și riscul de boală renală cronică. JAMA Intern Med. 2016;176:238-246.
23. Kia L, Kahrilas PJ. Terapie: riscurile asociate cu utilizarea cronică a IPP – semnal sau zgomot? Nat Rev Gastroenterol Hepatol. 2016;13(5):253-254.
24. Comunicarea FDA privind siguranța medicamentelor: nivelurile scăzute de magneziu pot fi asociate cu utilizarea pe termen lung a medicamentelor inhibitoare ale pompei de protoni (IPP). www.fda.gov/Drugs/DrugSafety/ucm245011.htm. Accesat la 17 februarie 2017.
25. Kieboom BC, Kiefte-de Jong JC, Eijgelsheim M, et al. Inhibitorii de pompă de protoni și hipomagneziemia în populația generală: un studiu de cohortă bazat pe populație. Am J Kidney Dis. 2015;66:775-782.
26. Park CH, Kim EH, Roh YH, et al. Asocierea dintre utilizarea inhibitorilor de pompă de protoni și riscul de hipomagneziemie: o revizuire sistematică și o meta-analiză. PLoS One. 2014;9:e112558.
27. Luk CP, Parsons R, Lee YP, Hughes JD. Hipomagneziemia asociată inhibitorilor de pompă de protoni: ce ne spun datele FDA? Ann Pharmacother. 2013;47:773-780.
28. Cheungpasitporn W, Thongprayoon C, Kittanamongkolchai W, et al. Inhibitori ai pompei de protoni legați de hipomagneziemie: o revizuire sistematică și o meta-analiză a studiilor observaționale. Ren Fail. 2015;37:1237-1241.
29. Markovits N, Loebstein R, Halkin H, et al. Asocierea dintre inhibitorii de pompă de protoni și hipomagneziemia în mediul comunitar. J Clin Pharmacol. 2014;54:889-895.
30. Park SH, Lee SH, Lee SH, Lee JS, et al. Modificări ale concentrației de magneziu seric după utilizarea unui inhibitor al pompei de protoni la pacienții supuși unei intervenții coronariene percutanate. Kidney Res Clin Pract. 2015;34:98-102.
31. Danziger J, William JH, Scott DJ, et al. Utilizarea inhibitorilor de pompă de protoni este asociată cu concentrații scăzute de magneziu seric. Kidney Int. 2013;83:692-699.
32. Begley J, Smith T, Barnett K, et al. Hipomagneziemia asociată inhibitorilor de pompă de protoni – un motiv de îngrijorare? Br J Clin Pharmacol. 2016;81:753-758.
33. Abraham NS, Hlatky MA, Antman EM, et al. Document de consens al experților ACCF/ACG/AHA 2010 privind utilizarea concomitentă a inhibitorilor de pompă de protoni și a thienopiridinelor: o actualizare concentrată a documentului de consens al experților ACCF/ACG/AHA 2008 privind reducerea riscurilor gastrointestinale ale terapiei antiplachetare și ale utilizării AINS. Am J Gastroenterol. 2010;105:2533-2549.
34. Melloni C, Washam JB, Jones WS, et al. Rezultate contradictorii între studiile randomizate și studiile observaționale cu privire la impactul inhibitorilor de pompă de protoni asupra evenimentelor cardiovasculare atunci când sunt coadministrați cu terapie antiplachetară dublă: revizuire sistematică. Circ Cardiovasc Qual Outcomes. 2015;8:47-55.
35. Amintește FDA să evite utilizarea concomitentă a Plavix (clopidogrel) și omeprazol. www.fda.gov/Drugs/DrugSafety/ucm231161.htm. Accesat la 17 februarie 2017.
36. Bundhun PK, Teeluck AR, Bhurtu A, Huang WQ. Este utilizarea concomitentă a clopidogrelului și a inhibitorilor de pompă de protoni încă asociată cu rezultate cardiovasculare adverse crescute după angioplastia coronariană?: o revizuire sistematică și o meta-analiză a studiilor publicate recent (2012-2016). BMC Cardiovasc Disord. 2017;17:3.